摘要:11.常温下.用0.1 mol/L的HCl溶液滴定a mL NaOH稀溶液.反应恰好完全时.消耗HCl溶液b mL.此时溶液中氢氧根离子的浓度c(OH-)是( ) A.1×10-7 mol/L B.1×107 mol/L C. mol/L D. mol/L 答案:A
网址:http://m.1010jiajiao.com/timu3_id_75404[举报]
常温下,用 0.1 mol·L—1HCl溶液滴定10.0 mL浓度为0.1 mol·L—1 Na2CO3溶液,所得滴定曲线如右图所示。下列说法正确的是

A.当V=0时:c(H+)+c(HCO 3-)+c(H2CO3)=c(OH-)
B.当V=5时:c(CO32—)+c(HCO 3-)+c(H2CO3)=2c(Cl-)
C.当V=10时:c(Na+)>c(HCO 3-)>c(CO32—)>c(H2CO3)
D.当V=a时:c(Na+)>c(Cl-)>c(H+)=c(OH-)
查看习题详情和答案>>
|
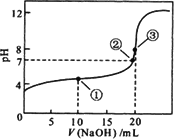
常温下,用0.1 mol/L NaOH溶液滴定20.00 mL 0.1 mol/L CH3COOH溶液滴定曲线如图.下列说法正确的是
| |
| [ ] | |
A. |
点①所示溶液中:c(CH3COO-)+c(OH-) |
B. |
点②所示溶液中:c(Na+)=c(CH3COOH)+c(CH3COO-) |
C. |
点③所示溶液中:c(Na+)>c(OH-)>c(CH3COO-)>c(H+) |
D. |
滴定过程中可能出现:c(CH3COOH)>c(CH3COO-)>c(H+)>c(Na+)>c(OH-) |