摘要:1.A:CmH2m+2.B:CnH2n.x L A.=2.5.即x=. ① m=1:n=3.x=0.25,n=4.x=0.5.② m=2:n=3.x=0.5,n=4.x=0.75.
网址:http://m.1010jiajiao.com/timu3_id_68573[举报]
在一固定容积为2L的密闭容器内加入0.2mol的N2和0.6mol的H2,在一定条件下发生如下反应:
N2(g)+3H2(g)?2NH3(g)△H<0
(1)该反应450℃的平衡常数
(2)下列描述中能说明上述反应已达平衡的是
a.3v正(H2)=2v逆(NH3) b.容器中气体的平均相对分子量不随时间而变化
c.容器中气体的密度不随时间而变化 d.容器中气体的分子总数不随时间而变化
(3)上述反应若第5分钟时达到平衡,测得NH3的物质的量为0.2mol计算从反应开始到平衡时,平均反应速率v(N2)为
(4)保持其他条件不变,若初始投入量为amolN2、bmolH2、cmolNH3,也可得到与上述相同的平衡,则a、b、c需满足关系式:
(5)第5分钟末,保持其它条件不变,若继续通入0.2mol的N2和0.6mol的H2,则平衡
查看习题详情和答案>>
N2(g)+3H2(g)?2NH3(g)△H<0
(1)该反应450℃的平衡常数
>
>
500℃时的平衡常数(填“>”、“<”或“=”);(2)下列描述中能说明上述反应已达平衡的是
bd
bd
a.3v正(H2)=2v逆(NH3) b.容器中气体的平均相对分子量不随时间而变化
c.容器中气体的密度不随时间而变化 d.容器中气体的分子总数不随时间而变化
(3)上述反应若第5分钟时达到平衡,测得NH3的物质的量为0.2mol计算从反应开始到平衡时,平均反应速率v(N2)为
0.01
0.01
mol/(L?min)(4)保持其他条件不变,若初始投入量为amolN2、bmolH2、cmolNH3,也可得到与上述相同的平衡,则a、b、c需满足关系式:
a+
=0.2,b+
=0.6
| c |
| 2 |
| 3c |
| 2 |
a+
=0.2,b+
=0.6
;| c |
| 2 |
| 3c |
| 2 |
(5)第5分钟末,保持其它条件不变,若继续通入0.2mol的N2和0.6mol的H2,则平衡
正反应方向
正反应方向
移动(填“向正反应方向”“向逆反应方向”或“不”).近来,制备和利用氢气这一清洁能源已有多项成果.
(1)德国克莱斯公司成功研制了利用甲醇(CH3OH)车载制氢燃料电池工艺,其原理如图所示,请观察此图回答:
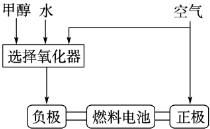
①燃料电池的正极反应式为 ;
②甲醇与流程图中任一反应物反应制取氢气的化学方程式 .
(2)美国Bay等工厂使用石油热裂解的副产物甲烷来制取氢气,其生产流程如图:
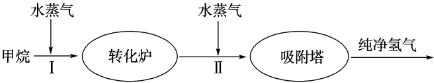
①此流程的第Ⅱ步反应为:CO(g)+H2O(g)?H2(g)+CO2(g),该反应的化学平衡常数表达式为K= ;
②此流程的第Ⅱ步反应的平衡常数随温度的变化如表1,在830℃,以表2的物质的量(单位为mol)投入恒容反应器发生上述反应,其中反应开始时,向正反应方向进行的有 (填实验编号);
表1
表2
③若400℃时,第Ⅱ步反应生成1 mol氢气的热效应值为33.2(单位为kJ),第1步反应的热化学方程式为:
CH4(g)+H2O(g)═3H2(g)+CO(g)△H=-103.3kJ?mol-1
则400℃时,甲烷和水蒸气反应生成二氧化碳和氢气的热化学方程式为 .
(3)我国科学家研究了常温下利用Pt等催化剂在可见光作用下使水分解制氢气的方法,如图是三种催化剂在光照分解水实验中的效果比较图.能得出如图结果的实验方案是 .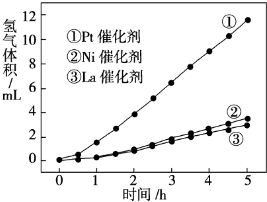
查看习题详情和答案>>
(1)德国克莱斯公司成功研制了利用甲醇(CH3OH)车载制氢燃料电池工艺,其原理如图所示,请观察此图回答:

①燃料电池的正极反应式为
②甲醇与流程图中任一反应物反应制取氢气的化学方程式
(2)美国Bay等工厂使用石油热裂解的副产物甲烷来制取氢气,其生产流程如图:

①此流程的第Ⅱ步反应为:CO(g)+H2O(g)?H2(g)+CO2(g),该反应的化学平衡常数表达式为K=
②此流程的第Ⅱ步反应的平衡常数随温度的变化如表1,在830℃,以表2的物质的量(单位为mol)投入恒容反应器发生上述反应,其中反应开始时,向正反应方向进行的有
表1
| 温度/℃ | 400 | 500 | 830 | 1000 |
| 平衡常数K | 10 | 9 | 1 | 0.6 |
| 实验编号 | n(CO) | n(H2O) | n(H2) | n(CO2) |
| A | 1 | 5 | 2 | 3 |
| B | 2 | 2 | 1 | 1 |
| C | 3 | 3 | 0 | 0 |
| D | 0.5 | 2 | 1 | 1 |
CH4(g)+H2O(g)═3H2(g)+CO(g)△H=-103.3kJ?mol-1
则400℃时,甲烷和水蒸气反应生成二氧化碳和氢气的热化学方程式为
(3)我国科学家研究了常温下利用Pt等催化剂在可见光作用下使水分解制氢气的方法,如图是三种催化剂在光照分解水实验中的效果比较图.能得出如图结果的实验方案是

可逆反应:3A(g)+B(g)?2C(g)+2D(g) 在不同条件下的反应速率分别为:
(1)v(A)=0.6mol?L-1?min-1
(2)v(B)=0.45mol?L-1?min-1
(3)v(C)=0.4mol?L-1?min-1
(4)v(D)=0.48mol?L-1?min-1
此反应在不同条件下进行最快的是( )
(1)v(A)=0.6mol?L-1?min-1
(2)v(B)=0.45mol?L-1?min-1
(3)v(C)=0.4mol?L-1?min-1
(4)v(D)=0.48mol?L-1?min-1
此反应在不同条件下进行最快的是( )
查看习题详情和答案>>
现有五种可溶性物质A、B、C、D、E,它们所含的阴、阳离子互不相同,分别含有 五种阳离子Na+、Al3+、Mg2+、Ba2+、Fe3+和五种阴离子Cl-、OH-、NO
、CO
、X中 的一种.
(1)某同学通过比较分析,认为无需检验就可判断其中必有的两种物质是 、 (填化学式).
(2)为了确定X,现将(1)中的两种物质记为A和B.当含X离子的C与A的溶液混 合时,产生红褐色沉淀和无色无味气体;当C与B的溶液混合时产生两种沉淀,向该沉淀中滴入足量的稀HNO3,沉淀部分溶解,最后留有白色沉淀.则:
①X为 (填序号).
A.SiO
B.CH3COO-C.SO
②A的水溶液中所有离子的浓度由大到小的顺序为 .
③化合物B的电子式 .
④将0.02mol的B与0.01mol的C同时溶解在足量的蒸馏水中,充分反应后,最终 所得沉淀的质量为 g(精确到0.1g).
⑤利用上述已经确定的一种物质,可以检验出D、E中的阳离子.请简述实验操作步 骤、现象及结论 .
(3)将Cu片投入到装有D溶液的试管中,Cu片不溶解;再滴加稀H2SO4,Cu片逐渐 溶解,试管口附近有红棕色气体出现,有关反应的离子方程式为 .
查看习题详情和答案>>
- 3 |
2- 3 |
(1)某同学通过比较分析,认为无需检验就可判断其中必有的两种物质是
(2)为了确定X,现将(1)中的两种物质记为A和B.当含X离子的C与A的溶液混 合时,产生红褐色沉淀和无色无味气体;当C与B的溶液混合时产生两种沉淀,向该沉淀中滴入足量的稀HNO3,沉淀部分溶解,最后留有白色沉淀.则:
①X为
A.SiO
2- 3 |
2- 4 |
②A的水溶液中所有离子的浓度由大到小的顺序为
③化合物B的电子式
④将0.02mol的B与0.01mol的C同时溶解在足量的蒸馏水中,充分反应后,最终 所得沉淀的质量为
⑤利用上述已经确定的一种物质,可以检验出D、E中的阳离子.请简述实验操作步 骤、现象及结论
(3)将Cu片投入到装有D溶液的试管中,Cu片不溶解;再滴加稀H2SO4,Cu片逐渐 溶解,试管口附近有红棕色气体出现,有关反应的离子方程式为
 美国Bay等工厂使用石油热裂解的副产物甲烷来制取氢气,其生产流程如图1:
美国Bay等工厂使用石油热裂解的副产物甲烷来制取氢气,其生产流程如图1:(1)此流程的第Ⅱ步反应为:CO(g)+H2O(g)?H2(g)+CO2(g),该反应的化学平衡常数表达式为K=
| c(H2)c(CO2) |
| c(CO)c(H2O) |
| c(H2)c(CO2) |
| c(CO)c(H2O) |
| 温度/℃ | 400 | 500 | 830 | 1000 |
| 平衡常数K | 10 | 9 | 1 | 0.6 |
放
放
(填“吸”、“放”)热反应.在830℃下,若开始时向恒容密闭容器中充入CO与HzO均为1mol,则达到平衡后CO的转化率为50%
50%
.(2)此流程的第Ⅱ步反应CO(g)+H2O(g)?H2(g)+CO2(g),在830℃,以表二的物质的量(单位为mol)投入恒容反应器发生上述反应,其中反应开始时,向正反应方向进行的有
B
B
(填实验编号);| 实验编号 | n(CO) | n(H2O) | n(H2) | n(CO2) |
| A | 1 | 5 | 2 | 3 |
| B | 2 | 2 | 1 | 1 |
| C | 0.5 | 2 | 1 | 1 |
④⑤⑥
④⑤⑥
①体系的压强不再发生变化 ②混合气体的密度不变 ③混合气体的平均相对分子质量不变 ④各组分的物质的量浓度不再改变 ⑤体系的温度不再发生变化 ⑥v正(CO2)=v逆(H2O)
(4)图2表示该反应此流程的第Ⅱ步反应在时刻t1达到平衡、在时刻t2分别因改变某个条件而发生变化的情况:图中时刻t2发生改变的条件是
降低温度或增加水蒸汽的量或减少氢气的量
降低温度或增加水蒸汽的量或减少氢气的量
.(写出两种)(5)若400℃时,第Ⅱ步反应生成1mol氢气的热量数值为33.2(单位为kJ),第Ⅰ步反应的热化学方程式为:
CH4(g)+H2O(g)=3H2(g)+CO(g)△H=-103.3kJ?mol-1.
则400℃时,甲烷和水蒸气反应生成二氧化碳和氢气的热化学方程式为
CH4(g)+2H2O(g)=CO2(g)+4H2(g)△H=-136.5kJ?mol-1
CH4(g)+2H2O(g)=CO2(g)+4H2(g)△H=-136.5kJ?mol-1
.