摘要:9.一种含MgO.Mg3N2的混合物.若其中Mg的质量分数为62.4%.则氮的质量分数为 .5.6%.
网址:http://m.1010jiajiao.com/timu3_id_68437[举报]
现在有一种含氧酸盐的固体试样,经测定,该固体含2种金属元素和两种非金属元素.其中酸根由一种金属元素和氧元素组成,且两种元素质量比为7:8.为进一步确定该固体成分,现将4.68g该固体试样溶于水,滴加适量稀硫酸后,再加入2.24g铁粉,铁粉与酸根恰好完全反应生成Fe2+.向反应后的溶液中加入一定量的KOH溶液至刚好将Fe2+沉淀完全,过滤;将沉淀充分加热后得到Fe2O3 4.8g.将滤液在一定条件下蒸发可得到一种纯净的不含结晶水的含氧酸正盐(不是复盐)A,测得其质量为13.92g.
(1)A的化学式为 .
(2)该盐含有的金属元素是 .
(3)通过计算推断该盐的化学式. 查看习题详情和答案>>
(1)A的化学式为
(2)该盐含有的金属元素是
(3)通过计算推断该盐的化学式. 查看习题详情和答案>>
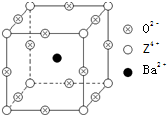 (2011?江西二模)已知X、Y和Z三种元素的原子序数之和等于48.X的一种1:1型氢化物分子中既有σ键又有π键.Z是金属元素,Z的单质和化合物有广泛的用途.已知Z的核电荷数小于28,且次外层有2个未成对电子.工业上利用ZO2和碳酸钡在熔融状态下制取化合物M(M可看做一种含氧酸盐).M有显著的“压电性能”,应用于超声波的发生装置.经X射线分析,M晶体的最小重复单位为正方体(如图),边长为4.03×10-10m,顶点位置为Z4+所占,体心位置为Ba2+所占,所有棱心位置为O2-所占.
(2011?江西二模)已知X、Y和Z三种元素的原子序数之和等于48.X的一种1:1型氢化物分子中既有σ键又有π键.Z是金属元素,Z的单质和化合物有广泛的用途.已知Z的核电荷数小于28,且次外层有2个未成对电子.工业上利用ZO2和碳酸钡在熔融状态下制取化合物M(M可看做一种含氧酸盐).M有显著的“压电性能”,应用于超声波的发生装置.经X射线分析,M晶体的最小重复单位为正方体(如图),边长为4.03×10-10m,顶点位置为Z4+所占,体心位置为Ba2+所占,所有棱心位置为O2-所占.(1)Y在周期表中位于
第四周期第ⅡA族
第四周期第ⅡA族
;Z4+的核外电子排布式为1s22s22p63s23p6
1s22s22p63s23p6
;(2)X的该种氢化物分子构型为
直线型
直线型
,X在该氢化物中以sp
sp
方式杂化.X和Y形成的化合物的熔点应该高于
高于
(填“高于”或“低于”)X氢化物的熔点.(3)①制备M的化学反应方程式是
TiO2+BaCO3═BaTiO3+CO2↑
TiO2+BaCO3═BaTiO3+CO2↑
;②在M晶体中,若将Z4+置于立方体的体心,Ba2+置于立方体的顶点,则O2-处于立方体的
面心
面心
;③在M晶体中,Z4+的氧配位数为
6
6
;④已知O2-半径为1.40×10-10 m,则Z4+半径为
6.15×10-11
6.15×10-11
m.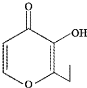 俗称“一滴香”的有毒物质被人食用后会损伤肝脏,还能致癌.“一滴香”的分子结构如图所示,下列说法正确的是( )
俗称“一滴香”的有毒物质被人食用后会损伤肝脏,还能致癌.“一滴香”的分子结构如图所示,下列说法正确的是( )| A、该有机物的分子式为C7H7O3 | B、该有机物能发生取代、加成和氧化反应 | C、1mol该有机物最多能与2mol H2发生加成反应 | D、该有机物的一种含苯环的同分异构体能发生银镜反应 |
 [化学-选修物质结构与性质]
[化学-选修物质结构与性质]Q、R、X、Y、Z为周期表前四周期元素,原子序数依次递增.已知:
①Q为周期表中原子半径最小的元素;
②R的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;
③Y的基态原子的核外成对电子数是未成对电子数的3倍;
④Z有“生物金属”之称,Z4+离子和氩原子的核外电子排布相同.
请回答下列问题:(答题时,Q、R、X、Y、Z用所对应的元素符号表示)
(1)RQ4Y分子的某中心原子采用的杂化轨道类型是
sp3
sp3
杂化.(2)R、X、Y三种元素的第一电离能由小到大的顺序为
C<O<N
C<O<N
.(3)已知:原子数目和电子总数(或价电子总数)相同的微粒互为等电子体,等电子体具有相似的结构特征.与RY分子互为等电子体的分子和离子分别为
N2
N2
和CN-
CN-
(填化学式).(4)Z元素位于周期表的
d
d
分区.Z原子基态时的外围电子排布式为3d24s2
3d24s2
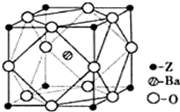
,Z的一种含氧酸钡盐的晶胞结构如图所示,晶体内与每个“Z”原子等距离且最近的氧原子数为6
6
.