摘要:2.P+1.8Cl2¾®0.7PCl3+0.3PCl5.
网址:http://m.1010jiajiao.com/timu3_id_68350[举报]
 硫酸生产主要有硫磺法和硫铁矿法等,这两种制法均经过催化氧化步骤.
硫酸生产主要有硫磺法和硫铁矿法等,这两种制法均经过催化氧化步骤.(1)钒触媒(V2O5)能加快SO2的氧化速率,此过程中SO2先与V2O5反应生成V2O4.该过程的化学方程式可表示为
SO2+V2O5?V2O4+SO3
SO2+V2O5?V2O4+SO3
.(2)为测定过程中混合气的SO2体积分数,选用0.0500mol/LI2的标准溶液、淀粉溶液进行测定.已知:V(耗用I2标准溶液)=10.00mL,V(采集烟气)=100.0mL(已折算为标准状况),则烟气中SO2的体积分数为
0.112
0.112
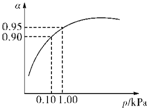
.(3)一定温度时,SO2的平衡转化率(α)与体系总压强(p)的关系如图所示.试分析工业生产中采用常压的原因是
在常压时,SO2的转化率已很高,若加压,则对设备、能源等有较高的要求,经济上不划算
在常压时,SO2的转化率已很高,若加压,则对设备、能源等有较高的要求,经济上不划算
.(4)在温度相同、体积均为1L的三个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下.
已知:2SO2(g)+O2(g)?2SO3(g);△H=-98.3kJ?mol-1.
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 2molSO2、1molO2 | 2molSO3 | mmolSO2、nmolO2、pmolSO3 |
| c(SO3)/mol?L-1 | 1.4 | 1.4 | 1.4 |
| 能量变化 | 放出akJ | 吸收bkJ | 吸收ckJ |
| SO2或SO3的转化率 | α1 | α2 | 12.5% |
1
1
,p=1.6
1.6
mol,b+c=39.32
39.32
kJ.下列做法正确的是( )
| A、用分液漏斗分离乙醇和苯酚的混合物 | B、实验室用加热饱和FeCl3溶液制Fe(OH)3胶体 | C、中和滴定时滴定管用所盛溶液润洗,锥形瓶不用所盛溶液润洗 | D、用37%(p=1.19 g?cm-3)的浓盐酸配制100 mL 1 mol?L-1的盐酸溶液,用到的量器为100 mL的量筒和100 mL的容量瓶 |
有四组物质,它们的沸点(℃,P=1.01×105Pa)如下表所示:
试根据上表回答下列问题:
(1)物质b的分子式为: ,物质 (填a或b)易溶于苯.
(2)除极少数情况外,上述四种系列中物质的沸点与相对分子质量之间均存在一定的关系,该关系是 .
(3)上表中, 和 两种物质的沸点较同系列其它物质反常,反常的主要原因是 .
查看习题详情和答案>>
| ① | He-268.8 | Ne-249.5 | Ar(x) | Kr-151.7 |
| ② | F2-187.0 | Cl2-33.6 | (a)58.7 | I2-184.0 |
| ③ | HF(Y) | HCl-84.0 | HBr-67.0 | HI-35.3 |
| ④ | H2O(Z) | H2S-60.2 | (b)-42.0 | H2Te-1.8 |
(1)物质b的分子式为:
(2)除极少数情况外,上述四种系列中物质的沸点与相对分子质量之间均存在一定的关系,该关系是
(3)上表中,
硼镁泥是一种工业废料,主要成分是MgO(约占40%),还有CaO、MnO、Fe2O3、FeO、Al2O3、SiO2等杂质,以此为原料制取的硫酸镁,可用于印染、造纸、医药等工业.从硼镁泥中提取MgSO4?7H2O的流程如图:

(1)实验中需要1.00mol/L的硫酸1000mL,若用98%的浓硫酸(p=1.84g/mL)来配制.下列所给的容器中,属于配制该硫酸溶液必须使用的有
A.容量瓶B.分液漏斗C.蒸馏烧瓶D.烧杯E.玻璃棒F.天平
(2)加入的NaClO可与Mn2+反应:Mn2++ClO-+H2O=MnO2↓+2H++Cl+,还有一种离子也会被NaClO氧化,该反应的离子方程式为
(3)滤渣的主要成分除含有Fe(OH)3、Al(OH)3外,还含有
(4)除去滤渣之前,往往还要加入一定量的硼镁泥,其原因可能是
(5)已知MgSO4、CaSO4的溶解度如下表
“除钙”是将MgSO4和CaSO4混合溶液中的CaSO4除去,根据上表数据简要说明操作步骤
(6)“操作Ⅰ”是将滤液继续蒸发浓缩,冷却结晶,
查看习题详情和答案>>

(1)实验中需要1.00mol/L的硫酸1000mL,若用98%的浓硫酸(p=1.84g/mL)来配制.下列所给的容器中,属于配制该硫酸溶液必须使用的有
A、D、E
A、D、E
(填写选项字母)A.容量瓶B.分液漏斗C.蒸馏烧瓶D.烧杯E.玻璃棒F.天平
(2)加入的NaClO可与Mn2+反应:Mn2++ClO-+H2O=MnO2↓+2H++Cl+,还有一种离子也会被NaClO氧化,该反应的离子方程式为
2Fe2++ClO-+2H+=2Fe3++Cl-+H2O或2Fe2++HClO+H+=2Fe3++Cl-+H2O
2Fe2++ClO-+2H+=2Fe3++Cl-+H2O或2Fe2++HClO+H+=2Fe3++Cl-+H2O
(3)滤渣的主要成分除含有Fe(OH)3、Al(OH)3外,还含有
MnO2、SiO2
MnO2、SiO2
(4)除去滤渣之前,往往还要加入一定量的硼镁泥,其原因可能是
调节溶液pH,使Fe3+、Al3+水解完全,除去多余的NaClO
调节溶液pH,使Fe3+、Al3+水解完全,除去多余的NaClO
(5)已知MgSO4、CaSO4的溶解度如下表
| 温度(°C) | 40 | 50 | 60 | 70 |
| MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
| CaSO4 | 0.210 | 0.207 | 0.201 | 0.197 |
蒸发浓缩,趁热过滤
蒸发浓缩,趁热过滤
(6)“操作Ⅰ”是将滤液继续蒸发浓缩,冷却结晶,
过滤(或过滤洗涤)
过滤(或过滤洗涤)
,便得到了MgSO4?7H2O.