摘要:( 19((((( 江苏省盐城中学2009届高三) (1)3d54s2 , Mn2+转化为Mn3+时.3d能级由较稳定的3d5半充满状态转变为不稳定的3d4状态(或Fe2+转化为Fe3+时.3d能级由不稳定的3d6状态转变为较稳定的3d5半充满状态) (2)① 具有孤对电子 , N≡N 2∶1
网址:http://m.1010jiajiao.com/timu3_id_66096[举报]
教材中给出的各物质的第一电离能的数据如下:
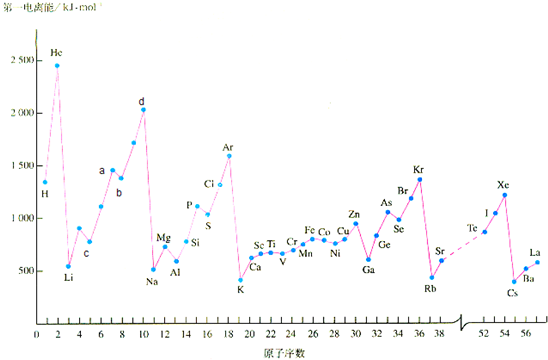
请回答下列问题:
(1)a点代表的元素是 .a点的第一电离能比b点高理由是: .
(2)d点代表的元素的第一电离能处在峰顶原因是: .稀有气体中的Xe能形成氧化物XeO3,已知该氙原子上有1对孤对电子,则XeO3分子构型为 型结构;Xe的杂化类型为 .
(3)上图中也给出了过渡元素的第一电离能数据,他们都与核外电子的排布有关,则Cu的外围电子排布式为: .
(4)Mn 元素的外围电子排布式为3d54s2,Fe元素的外围电子排布式为3d64s2,请解释Mn的第三电离能比Fe的第三电离能大的原因是: .
查看习题详情和答案>>

请回答下列问题:
(1)a点代表的元素是
(2)d点代表的元素的第一电离能处在峰顶原因是:
(3)上图中也给出了过渡元素的第一电离能数据,他们都与核外电子的排布有关,则Cu的外围电子排布式为:
(4)Mn 元素的外围电子排布式为3d54s2,Fe元素的外围电子排布式为3d64s2,请解释Mn的第三电离能比Fe的第三电离能大的原因是:
[ ]
A.Fe
B.Co
C.Mn
D.Ni
查看习题详情和答案>>
B.Co
C.Mn
D.Ni