网址:http://m.1010jiajiao.com/timu3_id_65927[举报]
①CO(g)+2H2(g)═CH3OH(g)△H1=-90.7kJ?mol-1
②2CH3OH(g)═CH3OCH3(g)+H2O(g)△H2=-23.5kJ?mol-1
③CO(g)+H2O(g)═CO2(g)+H2(g)△H3=-41.2kJ?mol-1
(1)若要增大反应①中H2的转化率,在其它条件不变的情况下可以采取的措施为
A.加入某物质作催化剂
B.加入一定量CO
C.反应温度降低
D.增大容器体积
(2)在某温度下,若反应①的起始浓度分别为:c(CO)=1mol/L,c(H2)=2.4mol/L,5min后达到平衡,CO的转化率为50%,则5min内CO的平均反应速率为
(3)催化反应室中总反应3CO(g)+3H2(g)═CH3OCH3(g)+CO2(g)的△H=
(4)二甲醚的燃烧热为1455kJ?mol-1,则二甲醚燃烧的热化学方程式为
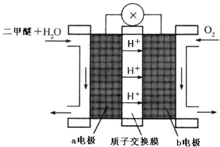
(5)“二甲醚燃料电池”是一种绿色电源,其工作原理如图所示.写出a电极上发生的电极反应式

请填空:
(1)工业上一般采用下列两种反应成甲醇:
反应Ⅰ:CO(g)+2H2(g)═CH3OH(g)△H1
反应Ⅱ:CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H2
上述反应符合“原子经济”原则的是
(2)在一定条件下,已知反应室2的可逆反应除生成二甲醚外还生成了气体CO2,其化学方程式为
(3)若利用水煤气合成二甲醚的三步反应如下:
①2H2(g)+CO(g)?CH3OH(g)△H=-90.8kJ?mol-1
②2CH3OH(g)?CH3OCH3(g)+H2O(g)△H=-23.5kJ?mol-1
③CO(g)+H2O(g)?CO2(g)+H2(g)△H=-41.3kJ?mol-1
则反应:3H2(g)+3CO(g)?CH3OCH3(g)+CO2 (g)△H=
(4)某实验小组依据甲醇燃烧的反应原理,设计如图1所示的电池装置.则该电池正极的电极反应为:

(5)甲醇质子交换膜燃料电池(如图2所示)是以酸性溶液为电解质溶液,甲醇从一个电极通入,O2从另一电极通入,中间为质子交换膜,通入甲醇的一极电极反应式为:
已知在1×105 Pa,298 K条件下,2 mol氢气燃烧生成水蒸气放出484 kJ热量,下列热化学方程式正确的是
A.H2O ( g ) = H2 ( g ) + 1/2O2 ( g ) △H = +242 kJ/mol
B.2H2 ( g ) + O2 ( g ) = 2H2O ( l ) △H = -484 kJ/mol
C.H2 ( g ) + 1/2O2 ( g ) = H2O ( g ) △H = +242 kJ/mo
D.2H2 ( g ) + O2 ( g ) = 2H2O ( g ) △H = +484 kJ/mol
查看习题详情和答案>>
能源短缺是人类面临的重大问题。甲醇是一种可再生能源,具有广泛的开发和应用前景。因此甲醇被称为21世纪的新型燃料。
(1)已知在常温常压下:
① 2CH3OH(l)+3O2(g)
2CO2(g)+4H2O(g) △H= -1275.6 kJ·mol—1
② H2O(l) H2O(g)
△H=+ 44.0 kJ.mo—1
写出表示甲醇燃烧热的热化学方程式 。
(2)工业上用CO生产燃料甲醇。一定条件下发生反应:CO(g)+2H2(g) CH3OH(g)。图1表示反应中能量的变化;图2表示一定温度下,在体积为2L的密闭容器中加入4mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化图。
CH3OH(g)。图1表示反应中能量的变化;图2表示一定温度下,在体积为2L的密闭容器中加入4mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化图。

①在“图1”中,曲线 (填“a”或“b”)表示使用了催化剂。
②能判断该反应在“图2”所在条件下是否已达化学平衡状态的依据是 。(双选)
A.容器中压强不变 B.体系的密度不随时间改变
C.v正(H2)=2v逆(CH3OH) D.CO与H2的物质的量的比不随时间改变
③计算该温度下CO(g)+2H2(g) CH3OH(g)的化学平衡常数K=
。
CH3OH(g)的化学平衡常数K=
。
④请在“图3”中画出平衡时甲醇百分含量(纵坐标)随温度(横坐标)变化的曲线,要求画压强不同的2条曲线(在曲线上标出P1、P2,且P1<P2)。
(3)CaSO4是一种微溶物质,已知Ksp(CaSO4)=9.10×10-6。现将c mol·L-1 CaCl2溶液与2.00×10-2 mol·L-1 Na2SO4溶液等体积混合生成沉淀,则c的最小值是 (结果保留3位有效数字)。
查看习题详情和答案>>