摘要: 某种铁的氧化物20克.在加热条件下通入足量的一氧化碳完全反应.将生成的气体用石灰水完全吸收.得到沉淀37.5克.则该氧化物中铁元素和氧元素的质量比为 7∶2 21∶8
网址:http://m.1010jiajiao.com/timu3_id_653[举报]
浓硫酸与乙二酸(H2C2O4)在加热条件下反应的化学方程式为:H2C2O4
CO2↑+CO↑+H2O
有人利用这个反应产生的CO还原某种铁的氧化物,并设计了如图所示的装置.

其中A和F中各盛有浓H2SO4,B中盛有乙二酸(H2C2O4),D中盛有Na0H浓溶液,E和I中各盛有澄清石灰水,H中装有铁的氧化物粉末.
(一)(1)D装置的作用
(2)E装置的作用
(二)甲同学用上述装置,取不同质量的铁的氧化物进行实验.所得实验数据如下:
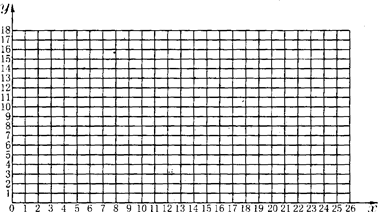
(1)如果以y轴表示生成铁的质量,x轴表示铁的氧化物质量,请用铅笔在坐标图上依次描出相应的实验数据的点.
(2)从上图可以看出甲进行第二次实验时,所得数据十分不可靠,故舍去.请分析造成此种结果的原因主要可能是
(3)请利用上图回答,第二次实验时生成的铁的质量约为
(4)如果另一同学乙取了25g铁的氧化物样品,而来不及做实验,但根据上述图示,可以求出所生成的铁的质量为
(5)同学丙看了甲、乙两同学所做的方法后,认为只要认真进行两次实验,就可回答上述问题.请用甲同学的两组实验数据用数学方法写出丙同学的分析过程.
(6)丁同学看了上述分析过程后,认为只要一组准确的实验数据就能解决问题.他是怎样分析的?
查看习题详情和答案>>
| ||
| △ |
有人利用这个反应产生的CO还原某种铁的氧化物,并设计了如图所示的装置.

其中A和F中各盛有浓H2SO4,B中盛有乙二酸(H2C2O4),D中盛有Na0H浓溶液,E和I中各盛有澄清石灰水,H中装有铁的氧化物粉末.
(一)(1)D装置的作用
除去混合气中的CO2
除去混合气中的CO2
.(2)E装置的作用
检验混合气中CO2是否已全部吸收
检验混合气中CO2是否已全部吸收
.(二)甲同学用上述装置,取不同质量的铁的氧化物进行实验.所得实验数据如下:
| 实验序号 | l | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 铁的氧化物质量(g) | 4.00 | 8.00 | 10.00 | 12.00 | 14.00 | 16.00 | 18.00 | 20.00 |
| 生成铁的质量(g) | 2.8l | 5.62 | 7.01 | 8.42 | 9.81 | 11.22 | 12.63 | 14.03 |

(1)如果以y轴表示生成铁的质量,x轴表示铁的氧化物质量,请用铅笔在坐标图上依次描出相应的实验数据的点.
(2)从上图可以看出甲进行第二次实验时,所得数据十分不可靠,故舍去.请分析造成此种结果的原因主要可能是
反应时间太短
反应时间太短
或温度太低
温度太低
.(3)请利用上图回答,第二次实验时生成的铁的质量约为
5.6
5.6
g(保留小数点后一位).(4)如果另一同学乙取了25g铁的氧化物样品,而来不及做实验,但根据上述图示,可以求出所生成的铁的质量为
17.5
17.5
g.(保留小数点后一位).将你所用的方法在上图中画出.(5)同学丙看了甲、乙两同学所做的方法后,认为只要认真进行两次实验,就可回答上述问题.请用甲同学的两组实验数据用数学方法写出丙同学的分析过程.
(6)丁同学看了上述分析过程后,认为只要一组准确的实验数据就能解决问题.他是怎样分析的?
浓硫酸与乙二酸(H2C2O4)在加热条件下反应的化学方程式为:H2C2O4 CO2↑+CO↑+H2O
CO2↑+CO↑+H2O
有人利用这个反应产生的CO还原某种铁的氧化物,并设计了如图所示的装置.
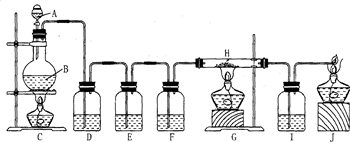
其中A和F中各盛有浓H2SO4,B中盛有乙二酸(H2C2O4),D中盛有Na0H浓溶液,E和I中各盛有澄清石灰水,H中装有铁的氧化物粉末.
(一)(1)D装置的作用______.
(2)E装置的作用______.
(二)甲同学用上述装置,取不同质量的铁的氧化物进行实验.所得实验数据如下:
| 实验序号 | l | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 铁的氧化物质量(g) | 4.00 | 8.00 | 10.00 | 12.00 | 14.00 | 16.00 | 18.00 | 20.00 |
| 生成铁的质量(g) | 2.8l | 5.62 | 7.01 | 8.42 | 9.81 | 11.22 | 12.63 | 14.03 |
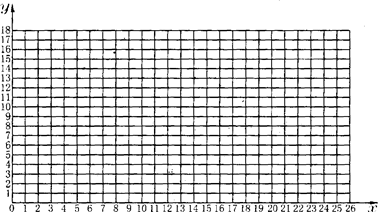
(1)如果以y轴表示生成铁的质量,x轴表示铁的氧化物质量,请用铅笔在坐标图上依次描出相应的实验数据的点.
(2)从上图可以看出甲进行第二次实验时,所得数据十分不可靠,故舍去.请分析造成此种结果的原因主要可能是______ 或______.
(3)请利用上图回答,第二次实验时生成的铁的质量约为______g(保留小数点后一位).
(4)如果另一同学乙取了25g铁的氧化物样品,而来不及做实验,但根据上述图示,可以求出所生成的铁的质量为______ g.(保留小数点后一位).将你所用的方法在上图中画出.
(5)同学丙看了甲、乙两同学所做的方法后,认为只要认真进行两次实验,就可回答上述问题.请用甲同学的两组实验数据用数学方法写出丙同学的分析过程.
(6)丁同学看了上述分析过程后,认为只要一组准确的实验数据就能解决问题.他是怎样分析的? 查看习题详情和答案>>