摘要:6.下图是铝热反应(2Al+Fe2O3高温Al2O3 +2Fe)的实验装置.有关该反应的下列说法中正确的是 ( ) A.a 为镁条 B.b为氧化铁与铝粉混合物 C.2mol氧化剂参与反应则电子转移6NA个电子 D.还原剂与氧化产物的物质的量之比为1:2
网址:http://m.1010jiajiao.com/timu3_id_64436[举报]
图是铝热反应(2Al+Fe2O3
Al2O3+2Fe)的实验装置,有关该反应的下列说法中正确的是
( )

查看习题详情和答案>>
| ||
( )
| A.a 为镁条 |
| B.b为氧化铁与铝粉混合物 |
| C.2mol氧化剂参与反应则电子转移6NA个电子 |
| D.还原剂与氧化产物的物质的量之比为1:2 |

如图1是某同学在实验室中进行铝热反应(铝过量)的实验装置,实验中他观察到的现象之一为“纸漏斗的下部被烧穿,有熔融物落入沙中”.

(1)写出该反应的化学方程式:
(2)为检验铝热反应后的固体成分,请填写下表:
(3)探究铝热反应后固体的性质:
将反应后容器中的固体残余物置于烧杯中,加入一定量的稀硝酸,固体完全溶解,反应过程中无气体放出(活泼金属可把稀HNO3还原为NH4NO3).在反应后的溶液中缓慢滴加4mol?L-1的NaOH溶液,产生沉淀的物质的量(mol)与加入NaOH溶液的体积(mL)的关系如图2所示:
①写出DE段发生反应的离子方程式:
②B与A的差值为
查看习题详情和答案>>

(1)写出该反应的化学方程式:
2Al+Fe2O3
Al2O3+2Fe
| ||
2Al+Fe2O3
Al2O3+2Fe
.
| ||
(2)为检验铝热反应后的固体成分,请填写下表:
| 检验成分 | 操作步骤 | 实验现象与结论 |
| 铝 | 取少量固体样品加入NaOH溶液中 取少量固体样品加入NaOH溶液中 |
若有(无)气泡产生,说明该样品中含有(不含)铝 若有(无)气泡产生,说明该样品中含有(不含)铝 |
| 氧化铁 | 取少量样品加入稀硫酸中,滴加KSCN溶液 取少量样品加入稀硫酸中,滴加KSCN溶液 |
若溶液变红色,说明原样品中含有Fe2O3,反之,则不含Fe2O3 若溶液变红色,说明原样品中含有Fe2O3,反之,则不含Fe2O3 |
将反应后容器中的固体残余物置于烧杯中,加入一定量的稀硝酸,固体完全溶解,反应过程中无气体放出(活泼金属可把稀HNO3还原为NH4NO3).在反应后的溶液中缓慢滴加4mol?L-1的NaOH溶液,产生沉淀的物质的量(mol)与加入NaOH溶液的体积(mL)的关系如图2所示:
①写出DE段发生反应的离子方程式:
NH4++OH-═NH3?H2O
NH4++OH-═NH3?H2O
.②B与A的差值为
0.008
0.008
. 绝大部分金属的冶炼都是通过再高温下发生的氧化还原反应来完成的,实验室利用铝热反应来模拟这种冶炼方法,实验装置如图.
绝大部分金属的冶炼都是通过再高温下发生的氧化还原反应来完成的,实验室利用铝热反应来模拟这种冶炼方法,实验装置如图.(1)铝热反应的化学方程式为
Fe2O3+2Al
2Fe+Al2O3
| ||
Fe2O3+2Al
2Fe+Al2O3
.
| ||
(2)描述“铝热反应”的现象
反应放出大量的热,并发出耀眼的光,纸漏斗的下部被烧穿,有熔融物落入沙中
反应放出大量的热,并发出耀眼的光,纸漏斗的下部被烧穿,有熔融物落入沙中
.(3)有的同学推测,铝热反应所得到的生成物是铁铝合金.设计一个简单的实验方案,证明所得的物质中含有金属铝.该实验所用的试剂是
NaOH溶液
NaOH溶液
,当观察到有气泡生成
有气泡生成
现象时,说明生成物中含有金属铝.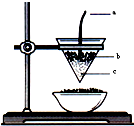 图是铝热反应(2Al+Fe2O3
图是铝热反应(2Al+Fe2O3