网址:http://m.1010jiajiao.com/timu3_id_64303[举报]
甲、乙两同学分别设计了如图所示的两套实验装置(所取的铁粉均为a g):

请回答下列问题:
(一)装置的评价
(1)在水蒸气的生成装置中乙同学在烧瓶底部放置了几片碎瓷片,其作用是___________;
(2)在反应装置中甲同学在硬质玻璃管中放入的是还原铁粉和石棉绒,石棉绒的作用是___
__________________;
(3)在收集装置中甲同学用的是排水集气法,这种方法存在的安全隐患是___________。
(二)实验过程
(4)甲同学可以证明两者发生反应的现象是______________________;
(5)从反应物元素的种类分析,生成的气体可能是氢气,进一步验证的方法是_________;
(6)当玻璃管中的铁粉充分反应后,停止实验,称量反应后固体产物质量为b,则固体产物的化学式为___________(用字母表示)。
(三)问题讨论
(7)酒精灯和酒精喷灯点燃的顺序是_____________。
(8)为了防止甲中气体收集装置发生的安全问题,可以在不增减仪器种类、数量,不改变其连接方式的前提下进行简单的改造,请在甲中画出你改造之处的示意图。
查看习题详情和答案>>常温下,在没有氧气存在时,铁与水几乎不反应,但高温下,铁能与水蒸气反应。
(1)铁粉与水蒸气反应的化学方程式是:
(2)停止反应,待装置冷却后,取出反应过的铁粉混合物,加入过量的稀硫酸充分反应。过滤。简述检验所得滤液中Fe3+的操作方法:
(3)经检验上述滤液中不含Fe3+,这不能说明铁粉与水蒸气反应所得产物中不含+3价的铁。原因是(结合化学方程式说明):
(4)某同学利用上述滤液制取白色的Fe(OH)2沉淀,向滤液中加入NaOH溶液后,观察到生成的白色沉淀迅速变成灰绿色,最后变成红褐色。
①沉淀由白色变为红褐色的化学方程式是:
②为了得到白色的Fe(OH)2沉淀,并尽可能使沉淀长时间保持白色,有人设计如下图所示的装置: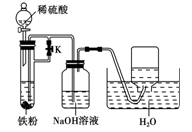
请简述实验操作及原理:
常温下,在没有氧气存在时,铁与水几乎不反应,但高温下,铁能与水蒸气反应。
(1)铁粉与水蒸气反应的化学方程式是: 。
(2)停止反应,待装置冷却后,取出反应过的还原铁粉混合物,加入过量的稀硫酸充分反应,过滤。简述检验所得滤液中Fe3+的操作方法: 。
(3)经检验上述滤液中不含Fe3+,这不能说明还原铁粉与水蒸气反应所得产物中不含+3价的Fe元素。原因是(结合化学方程式说明) : 。
(4)某同学利用上述滤液制取白色的Fe(OH)2、沉淀,向滤液中加入NaOH溶液后,观察至生成的白色的沉淀迅速变成灰绿色,最后变成红褐色。
①沉淀由白色→红褐色的化学方程式是: 。
②为了得到白色的Fe(OH)2沉淀,并尽可能长时间保持其白色,有人设计如下图所示装置:
请简述实验操作及原理: 。

(1)铁粉与水蒸气反应的化学方程式是:
(2)停止反应,待装置冷却后,取出反应过的铁粉混合物,加入过量的稀硫酸充分反应。过滤。简述检验所得滤液中Fe3+的操作方法:
(3)经检验上述滤液中不含Fe3+,这不能说明铁粉与水蒸气反应所得产物中不含+3价的铁。原因是(结合化学方程式说明):
(4)某同学利用上述滤液制取白色的Fe(OH)2沉淀,向滤液中加入NaOH溶液后,观察到生成的白色沉淀迅速变成灰绿色,最后变成红褐色。
①沉淀由白色变为红褐色的化学方程式是:
②为了得到白色的Fe(OH)2沉淀,并尽可能使沉淀长时间保持白色,有人设计如下图所示的装置:
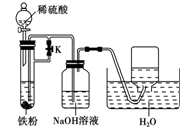
请简述实验操作及原理:
常温下,在没有氧气存在时,铁与水几乎不反应,但高温下,铁能与水蒸气反应.
(1)铁粉与水蒸气反应的化学方程式是:________
(2)停止反应,待装置冷却后,取出反应过的铁粉混合物,加入过量的稀硫酸充分反应.过滤.简述检验所得滤液中Fe3+的操作方法:________
(3)经检验上述滤液中不含Fe3+,这不能说明铁粉与水蒸气反应所得产物中不含+3价的铁.原因是(结合化学方程式说明):________
(4)某同学利用上述滤液制取白色的Fe(OH)2沉淀,向滤液中加入NaOH溶液后,观察到生成的白色沉淀迅速变成灰绿色,最后变成红褐色.
①沉淀由白色变为红褐色的化学方程式是:________
②为了得到白色的Fe(OH)2沉淀,并尽可能使沉淀长时间保持白色,有人设计如下图所示的装置:
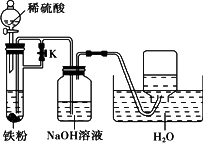
请简述实验操作及原理:________