摘要:24.(2009·理综浙江卷.10.6分)已知:25 ℃时.Ksp[Mg(OH)2] = 5.61×10-12.Ksp[MgF2] = 7.42×10-11.下列说法正确的是( ) A.25 ℃时.饱和Mg(OH)2溶液与饱和MgF2溶液相比.前者的c(Mg2+)大 B.25 ℃时.在Mg(OH)2的悬浊液加入少量的NH4Cl固体.c(Mg2+)增大 C.25 ℃时.Mg(OH)2固体在 20 mL 0.01 mol·L-1氨水中的Ksp比在20 mL 0.01 mol·L-1 NH4Cl溶液中的Ksp小 D.25 ℃时.在Mg(OH)2的悬浊液加入NaF溶液后.Mg(OH)2不可能转化成为MgF2
网址:http://m.1010jiajiao.com/timu3_id_60002[举报]
 运用化学反应原理研究氮、硫、氯等单质及其化合物的反应有重要的意义.
运用化学反应原理研究氮、硫、氯等单质及其化合物的反应有重要的意义.(1)放热反应2SO2(g)+O2(g)=2SO3(g)是硫酸工业上的重要反应,在体积不变的条件下,下列措施有利于提高SO2平衡转化率的有
A、升高温度 B、降低温度 C、减小压强 D、加入催化剂 E.移出氧气
(2)氮是大气中含量最多的一种元素,氮及其化合物在工农业生产、生活中有着重要应用.用CH4将氮氧化物(用NOx表示)催化还原为N2可以消除氮氧化物带来的污染,该反应的化学方程式为
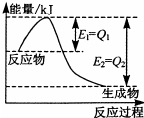
(3)如图是一定的温度和压强下,N2和H2反应生成1mol NH3过程中的能量变化图,请写出工业合成氨的热化学方程式
(4)在25℃下,将xmol/L的氨水与y mol/L的盐酸等体积混合,反应后溶液显中性,则c(NH4+ )
(5)已知:25℃时,Ksp(AgCl)=1.8×10-10、Ksp(AgBr)=4.9×10 -13.现在向0.001mol/L KBr和0.01mol/L KCl混合溶液中滴加0.1mol/L AgNO3溶液(反应过程中溶液体积变化忽略不计),当出现AgCl沉淀时.c(Br-)=
 已知:Cu(OH)2是二元弱碱;亚磷酸(H3PO3)是二元弱酸,与NaOH溶液反应,生成Na2HPO3.
已知:Cu(OH)2是二元弱碱;亚磷酸(H3PO3)是二元弱酸,与NaOH溶液反应,生成Na2HPO3.(1)在铜盐溶液中Cu2+发生水解反应的离子方程式为
(2)根据H3PO3的性质可推测Na2HPO3稀溶液的pH
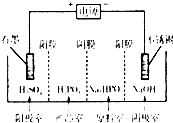
(3)电解Na2HPO3溶液可得到亚磷酸,装置如图(说明:阳膜只允许阳离子通过,阴膜只允许阴离子通过)
①阳极的电极反应式为
②产品室中反应的离子方程式为
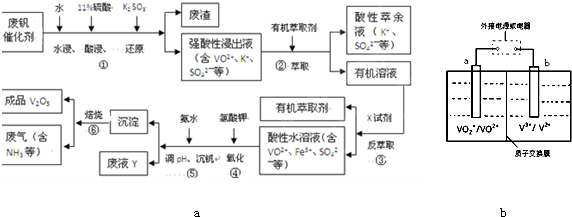
从废钒催化剂(主要成分V2O5、VOSO4、K2SO4、SiO2和Fe2O3等)中回收V2O5的一种生产工艺流程示意图如图a:
回答下列问题:
(1)①中废渣的主要成分是 .
(2)完成④中反应的离子方程式:
ClO3-+ VO2++ H+= VO3++ ( )+ ( )
(3)25℃时,取样进行实验分析,得到钒沉淀率和溶液pH之间的关系如下表
试判断在实际生产时,⑤中加入氨水调节溶液的最佳pH为 ;若钒沉淀率为93.1%时不产生Fe(OH)3沉淀,则溶液中c(Fe3+)< .(已知:25℃时,Ksp(Fe(OH)3)=2.6×10-39)
(4)全矾液流电池是一种新型电能储存和高效转化装置(如图b所示,a、b均为惰性电极),已知:全矾液流电池的工作原理为:
VO2++V2++2H+
VO2++H2O+V3+
V2+为紫色,V3+为绿色,VO2+为蓝色,VO2+为黄色.则:
①放电过程中,当转移1.0mol电子时共有1.0mol H+从 槽迁移进 槽(填“左”、“右”)
②当充电时,右槽溶液颜色由 色变为 色.
查看习题详情和答案>>

回答下列问题:
(1)①中废渣的主要成分是
(2)完成④中反应的离子方程式:
(3)25℃时,取样进行实验分析,得到钒沉淀率和溶液pH之间的关系如下表
| pH | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
| 钒沉淀率/% | 88.1 | 94.8 | 96.5 | 98.0 | 98.8 | 98.8 | 96.4 | 93.1 | 89.3 |
(4)全矾液流电池是一种新型电能储存和高效转化装置(如图b所示,a、b均为惰性电极),已知:全矾液流电池的工作原理为:
VO2++V2++2H+
| 放电 |
| 充电 |
V2+为紫色,V3+为绿色,VO2+为蓝色,VO2+为黄色.则:
①放电过程中,当转移1.0mol电子时共有1.0mol H+从
②当充电时,右槽溶液颜色由
运用反应原理研究氮、硫、氯、碘及其化合物的反应有重要意义.
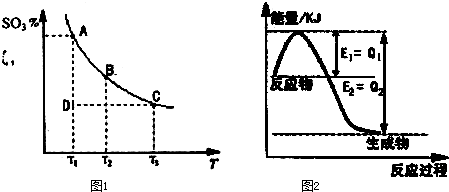
(1 )在反应:2SO2(g)+O2(g)?2SO3(g)的混合体系中,SO3的百分含量和温度的关系如图1(曲线上任何一点都表示平衡状态):
①2SO2(g)+O2(g)?2SO3(g)的△H 0 (填“>”或“<”);若在恒温、恒压时,向该平衡体系中通入氦气,平衡将 移动(填“向左”、“向右”或“不”);
②当温度为T1,反应进行到状态D时,V正 V逆(填“>”、“<”或“=).
(2 )①图2是一定条件下,N2和H2发生可逆反应生成1mol NH3的能量变化图,该反应的热化学反应方程式 .
(△H用含Q1、Q2的代数式表示) ②25°C时,将a mol?L-1的氨水与b mol?L-1的盐酸等体积混合,所得溶液的PH=7,则c ( NH+4) c (Cl-),a b,(填“>”、“<”或“=”);
(3)海水中含有大量以化合态形式存在的氯、碘元素.
已知:25℃时,Ksp[AgCl]=1.6×10-10 mol2?L-2、Ksp[AgI]=1.5×10-16mol2?L-2).在 25℃时,向 10mL0.002mol?l-1 的 NaCl 溶液中滴入 10mL0.002mol.l-1AgNO3溶液,有白色沉淀生成,向所得浊液中继续滴入O.1mol l-1的NaI溶液,白色沉淀逐渐转化为黄色沉淀,其原因是 ,该反应的离子方程式 .
查看习题详情和答案>>
(1 )在反应:2SO2(g)+O2(g)?2SO3(g)的混合体系中,SO3的百分含量和温度的关系如图1(曲线上任何一点都表示平衡状态):
①2SO2(g)+O2(g)?2SO3(g)的△H
②当温度为T1,反应进行到状态D时,V正
(2 )①图2是一定条件下,N2和H2发生可逆反应生成1mol NH3的能量变化图,该反应的热化学反应方程式
(△H用含Q1、Q2的代数式表示) ②25°C时,将a mol?L-1的氨水与b mol?L-1的盐酸等体积混合,所得溶液的PH=7,则c ( NH+4)

(3)海水中含有大量以化合态形式存在的氯、碘元素.
已知:25℃时,Ksp[AgCl]=1.6×10-10 mol2?L-2、Ksp[AgI]=1.5×10-16mol2?L-2).在 25℃时,向 10mL0.002mol?l-1 的 NaCl 溶液中滴入 10mL0.002mol.l-1AgNO3溶液,有白色沉淀生成,向所得浊液中继续滴入O.1mol l-1的NaI溶液,白色沉淀逐渐转化为黄色沉淀,其原因是