摘要:2.(江苏省淮安中学2008~2009学年度高三12分)元素周期律是20世纪科学技术发展的重要理论依据之一.已知A.B.C.D.E五种元素都是元素周期表中前20号元素.A.B.C.D四种元素在元素周期表中的相对位置如下图所示.B.C.D的最高价氧化物的水化物两两混合.均能发生反应生成盐和水.E元素原子序数均大于A.B.C.D元素.且不与A.B.C.D元素位于同主族. -- A B C D 根据以上信息.回答下列问题: (1)上述五种元素中电负性最大的是 . (2)请写出D的电子排布式: (3)A和D的氢化物中.沸点较高的是 ,其原因是 . (4)请写出B.C的最高价氧化物的水化物相混合反应的离子方程式: (5)A和E可组成离子化合物.其晶胞(在晶体中具有代表性的最小重复单元)结构如下图所示. 阳离子位于该正方体的顶点或面心,阴离子均位于小正方体中心.该化合物的电子式为 . 答案.. , (2)1S22S22P63S23P4 .因为HF分子间存在氢键, 3+OH-=AlO2-+2H2O .
网址:http://m.1010jiajiao.com/timu3_id_59282[举报]
[化学选修-物质结构与性质]
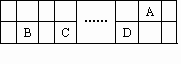
元素周期律是20世纪科学技术发展的重要理论依据之一.已知A、B、C、D、E五种元素都是元素周期表中前20号元素.A、B、C、D四种元素在元素周期表(长式)中的相对位置如下图所示,B、C、D的最高价氧化物的水化物两两混合,均能发生反应生成盐和水.E元素的原子序数均大于A、B、C、D元素,且不与A、B、C、D元素位于同主族.
根据以上信息,回答下列问题:
(1)上述A、B、C、D四种元素中第一电离能最小的是 ,电负性最大的是 .(填相关元素的元素符号)
(2)A和D的氢化物中,沸点较高的是 (填相关物质的分子式);其原因是 .
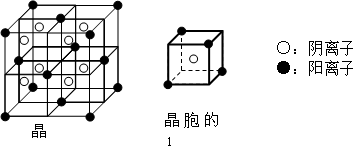
(3)A和E可组成离子化合物,其晶胞(在晶体中具有代表性的最小重复单元)结构如下图所示:
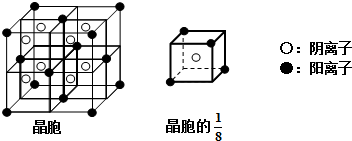
阳离子位于该正方体的顶点或面心;阴离子均位于小正方体中心.该化合物化学式为 .
查看习题详情和答案>>
元素周期律是20世纪科学技术发展的重要理论依据之一.已知A、B、C、D、E五种元素都是元素周期表中前20号元素.A、B、C、D四种元素在元素周期表(长式)中的相对位置如下图所示,B、C、D的最高价氧化物的水化物两两混合,均能发生反应生成盐和水.E元素的原子序数均大于A、B、C、D元素,且不与A、B、C、D元素位于同主族.
| … | A | |||||
| B | C | D |
(1)上述A、B、C、D四种元素中第一电离能最小的是
(2)A和D的氢化物中,沸点较高的是
(3)A和E可组成离子化合物,其晶胞(在晶体中具有代表性的最小重复单元)结构如下图所示:

阳离子位于该正方体的顶点或面心;阴离子均位于小正方体中心.该化合物化学式为
元素周期律是20世纪科学技术发展的重要理论依据之一.已知A、B、C、D、E五种元素都是元素周期表中前20号元素.A、B、C、D四种元素在元素周期表(长式)中的相对位置如下图所示,B、C、D的最高价氧化物的水化物两两混合,均能发生反应生成盐和水.E元素原子序数均大于A、B、C、D元素,且不与A、B、C、D元素位于同主族.
根据以上信息,回答下列问题:
(1)上述五种元素中电负性最大的是 .(填相关元素的元素符号)
(2)请写出E的电子排布式: .
(3)A和D的氢化物中,沸点较高的是 (填相关物质的分子式);其原因是 .
(4)请写出B、C的最高价氧化物的水化物相混合反应的离子方程式: .
(5)D和B形成的化合物的水溶液的pH 7(填“>”、“=”、“<”),其原因是 (用离子方程式表示).
查看习题详情和答案>>
| … | A | ||||||
| B | C | D |
(1)上述五种元素中电负性最大的是
(2)请写出E的电子排布式:
(3)A和D的氢化物中,沸点较高的是
(4)请写出B、C的最高价氧化物的水化物相混合反应的离子方程式:
(5)D和B形成的化合物的水溶液的pH
(2010?天津一模)元素周期表是20世纪科学技术发展的重要理论依据之一,是我们学习化学的重要工具.假设NH4+是“元素”NH4的阳离子,则“元素”NH4在周期表中的位置应该是第
查看习题详情和答案>>
三
三
周期第IA
IA
族;“元素”NH4的单质常温常压下应为固
固
(填“固”、“液”或“气”)体;熔点低
低
(填“高”或“低”);能
能
(填“能”或“不能”)导电;NH4的碳酸盐应易
易
(填“易”或“不易”)溶于水.元素周期表是20世纪科学技术发展的重要理论依据之一,是我们学习化学的重要工具.假设NH4+是“元素”NH4的阳离子,则“元素”NH4在周期表中的位置应该是第______周期第______族;“元素”NH4的单质常温常压下应为______(填“固”、“液”或“气”)体;熔点______(填“高”或“低”);______(填“能”或“不能”)导电;NH4的碳酸盐应______(填“易”或“不易”)溶于水.
查看习题详情和答案>>
| |||||||||||||||