摘要:在一密闭容器中.CO和H2O 混合加热到800℃达到下列平衡: CO(g)+H2O(g)CO2(g)+H2(g) .K=1.0.若反应开始时CO和H2O的浓度分别为0.20mol/L和1.00mol/L.则CO转化为CO2的转化率为( ) A.80% B.83% C.75% D.91%
网址:http://m.1010jiajiao.com/timu3_id_58569[举报]
在一密闭容器中,CO和H2O混合加热到800℃达到下列平衡:CO(g)+H2O(g)?CO2(g)+H2(g) K=1.0,若反应开始时CO和H2O的浓度均为1.00mol?L-1,则CO的转化率为( )
| A、40% | B、50% | C、75% | D、80% |
在一密闭容器中,CO和H2O混合加热到800℃达到下列平衡:CO(g)+H2O(g)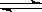 CO2(g)+H2(g) ,K=1.0,若反应开始时CO和H2O的浓度分别为0.20mol/L和1.00mol/L,则CO转化为CO2的转化率为
CO2(g)+H2(g) ,K=1.0,若反应开始时CO和H2O的浓度分别为0.20mol/L和1.00mol/L,则CO转化为CO2的转化率为
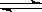 CO2(g)+H2(g) ,K=1.0,若反应开始时CO和H2O的浓度分别为0.20mol/L和1.00mol/L,则CO转化为CO2的转化率为
CO2(g)+H2(g) ,K=1.0,若反应开始时CO和H2O的浓度分别为0.20mol/L和1.00mol/L,则CO转化为CO2的转化率为| A.80% | B.83% | C.75% | D.91% |
在一密闭容器中,CO和H2O混合加热到800℃达到下列平衡:
![]() K=1.0,若反应开始时CO和H2O的浓度均为1.00 mol?L-1,则CO的转化率为
K=1.0,若反应开始时CO和H2O的浓度均为1.00 mol?L-1,则CO的转化率为
A.40% B.50% C.75% D.80%
查看习题详情和答案>>在一密闭容器中,CO和H2O混合加热到800℃达到下列平衡:CO(g)+H2O(g) CO2(g)+H2(g) ,K=1.0,若反应开始时CO和H2O的浓度分别为0.20mol/L和1.00mol/L,则CO转化为CO2的转化率为
CO2(g)+H2(g) ,K=1.0,若反应开始时CO和H2O的浓度分别为0.20mol/L和1.00mol/L,则CO转化为CO2的转化率为
| A.80% | B.83% | C.75% | D.91% |
在一个容积为0.5L的密闭容器中,将 2mol CO和6mol H2O混合加热到800℃,发生反应:CO(g)+H2O(g)  CO2(g)+H2(g),经过5min后达到平衡状态.若此时测得H2的浓度为3mol?L-1,求:
CO2(g)+H2(g),经过5min后达到平衡状态.若此时测得H2的浓度为3mol?L-1,求:
(1)以CO的浓度变化表示的该反应的速率.
(2)达平衡时H2O的转化率.
(3)已知:在一定温度下,该反应达平衡时,各物质的平衡浓度之间存在以下关系:
K=
且当温度不变时K为常数,K不随反应物、生成物浓度的改变而改变.求:
①在800℃下,该反应的K=
查看习题详情和答案>>
 CO2(g)+H2(g),经过5min后达到平衡状态.若此时测得H2的浓度为3mol?L-1,求:
CO2(g)+H2(g),经过5min后达到平衡状态.若此时测得H2的浓度为3mol?L-1,求:(1)以CO的浓度变化表示的该反应的速率.
(2)达平衡时H2O的转化率.
(3)已知:在一定温度下,该反应达平衡时,各物质的平衡浓度之间存在以下关系:
K=
| c(CO2)? c(H2) | c(CO)?c(H2O) |
且当温度不变时K为常数,K不随反应物、生成物浓度的改变而改变.求:
①在800℃下,该反应的K=
1
1
;②在800℃下,当投入1mol CO和4mol H2O混合加热到平衡时,H2浓度是多少.