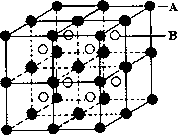
摘要:14.(山东省淄博市09届高三检测题)(1)由A.B两元素组成的离子晶体结构(甲)如图所示.则该晶体的化学式是: . (2)C原子的最外层电子排布为nsnnpm.其某一激发态可使这两个亚层的每一个轨道都处于充满状态.1个C原子与2个D原子结合.使双方都达到8电子稳定结构.则在C与D形成的分子中.C原 子发生轨道的杂化方式是 .分子构型是 .从成键方式看.该分子中含有的共价键的类型和数目分别是 . (3)C与D形成的常见晶体(乙).与甲晶体的熔点相比.乙 甲.其原因是 .
网址:http://m.1010jiajiao.com/timu3_id_57531[举报]
(1)由A、B两元素组成的离子晶体结构(甲)如图所示,则该晶体的化学式是:___________。
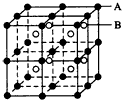
(2)C原子的最外层电子排布为nsnnpm,其某一激发态可使这两个亚层的每一个轨道都处于全满状态,1个C原子与2个D原子结合,使双方都达到8电子稳定结构。则在C与D形成的分子中,C原子发生轨道的杂化方式是________,分子构型是________,从成键方式看,该分子中含有的共价键的类型和数目分别是________________
(3)C与D形成的常见晶体(乙),与甲晶体的熔点相比,乙____甲,其原因是___________________。
查看习题详情和答案>>
(3)C与D形成的常见晶体(乙),与甲晶体的熔点相比,乙____甲,其原因是___________________。
(1)由A、B两元素组成的离子晶体结构(甲)如图所示,则该晶体的化学式是: 。
(2)C原子的最外层电子排布为nsnnpm,其某一激发态可使这两个亚层的每一个轨道都处于充满状态,1个C原子与2个D原子结合,使双方都达到8电子稳定结构。则在C与D形成的分子中,C原子发生轨道的杂化方式是 ,分子构
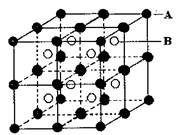
型是 ,从成键方式看,该分子中含有的共价键的类型和数目分别是 。
(3)C与D形成的常见晶体(乙),与甲晶体的熔点相比,乙 甲,其原因是
。
查看习题详情和答案>>