摘要: A.B.C三种元素的原子具有相同的电子层数.它们相同物质的量的原子获得相同物质的量的电子时释放出的能量是A 〉C 〉B.则它们的原子序数大小顺序是 ( ) A.B 〉C 〉A B.A 〉B 〉C C.C 〉A 〉B D.A 〉C 〉B
网址:http://m.1010jiajiao.com/timu3_id_56737[举报]
A、B、C三种元素的原子具有相同的电子层数,而B的核电荷数比A大2,C原子的电子总数比B原子电子总数多4.1molA单质跟盐酸反应可置换出11.2L(标准状况下)氢气,这时A转变成与氖原子具有相同电子层结构的离子.试回答:
(1)A是
(2)写出A元素的单质在氧气燃烧时生成物的电子式: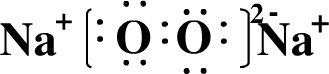
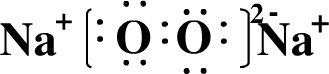 .
.
(3)写出由A元素和C元素组成化合物的形成过程:
 .
.
(4)分别写出A、B最高价氧化物对应水化物分别跟C的气态氢化物水溶液反应的离子方程式:
(5)A离子的氧化性比B离子的氧化性
查看习题详情和答案>>
(1)A是
Na
Na
元素,B是Al
Al
元素,C是Cl
Cl
元素.(2)写出A元素的单质在氧气燃烧时生成物的电子式:
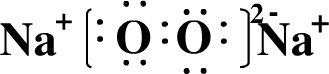
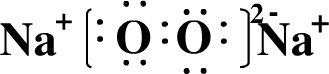
(3)写出由A元素和C元素组成化合物的形成过程:


(4)分别写出A、B最高价氧化物对应水化物分别跟C的气态氢化物水溶液反应的离子方程式:
OH-+H+═H2O、Al(OH)3+3H+═Al3++3H2O
OH-+H+═H2O、Al(OH)3+3H+═Al3++3H2O
.(5)A离子的氧化性比B离子的氧化性
弱
弱
,这是由于A单质的还原性强或A元素的金属性强
A单质的还原性强或A元素的金属性强
.A、B、C三种元素的原子具有相同的电子层数,且B的核外电子数比A多2个,C的质子数比B多4个,1molA的单质与酸反应,能置换出1gH2,这时,A转化为具有氖原子相同的电子层结构的离子.请回答下列问题:
(1)写出A、B、C的元素符号
(2)写出A的单质与水反应的离子方程式
(3)写出A与C单质化合的化学方程式.
查看习题详情和答案>>
(1)写出A、B、C的元素符号
(2)写出A的单质与水反应的离子方程式
(3)写出A与C单质化合的化学方程式.
A、B、C三种元素的原子具有相同的电子层数,而B的核电荷数比A大1,C原子的电子总数比B原子的电子总数多4; 1molA的单质能跟足量的盐酸反应,在标准状况下可置换出22.4L的H2,这时A转变为与氖原子具有相同电子层结构的离子.试回答:
(1)写出A和C组成的化合物的电子式
 ;
;
(2)B的离子结构示意图是
 ,与B的离子具有相同电子数的分子中,有一种分子可与盐酸化合生成一种盐,该盐的电子式是
,与B的离子具有相同电子数的分子中,有一种分子可与盐酸化合生成一种盐,该盐的电子式是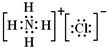
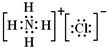 ;
;
(3)写出C元素的单质和甲烷发生一元取代反应的化学方程式
(4)写出A最高价氧化物的水化物和C最高价氧化物的水化物之间反应的离子方程式:
查看习题详情和答案>>
(1)写出A和C组成的化合物的电子式


(2)B的离子结构示意图是


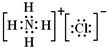
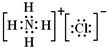
(3)写出C元素的单质和甲烷发生一元取代反应的化学方程式
CH4+Cl2
CH3Cl+HCl
| 光照 |
CH4+Cl2
CH3Cl+HCl
;| 光照 |
(4)写出A最高价氧化物的水化物和C最高价氧化物的水化物之间反应的离子方程式:
Mg(OH)2+2H+=Mg2++2H2O
Mg(OH)2+2H+=Mg2++2H2O
.A、B、C三种元素的原子具有相同的电子层数,而B的核电荷数比A大两个单位,C的质子数比B多4个,1mol A的单质与酸反应,能置换出1g H2,这时A转化为具有与氖原子相同的电子层结构的离子.则A的原子结构示意图为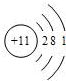
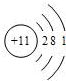 ,B离子的核外电子排布式为
,B离子的核外电子排布式为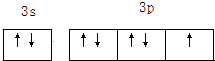
 .
.
查看习题详情和答案>>
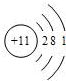
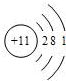
1s22s22p6
1s22s22p6
,C原子外围电子的轨道表示式为

A、B、C三种元素的原子具有相同的电子层数,而B的核电荷数比A大2,C原子的电子总数比B原子的电子总数多4; 1molA的单质能跟盐酸反应,在标准状况下可置换出11.2L的H2,这时A转变为与氖原子具有相同电子层结构的离子.试回答:
(1)A是
(2)B的离子结构示意图是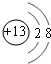
 ,与B的离子具有相同电子数的微粒中,有一种分子可与盐酸化合生成一种盐,该反应的化学方程式是
,与B的离子具有相同电子数的微粒中,有一种分子可与盐酸化合生成一种盐,该反应的化学方程式是
(3)A、C元素形成化合物的电子式是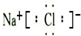
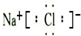 ,周期表中与C上下相邻的同主族元素形成的气态氢化物中,稳定性最强的是
,周期表中与C上下相邻的同主族元素形成的气态氢化物中,稳定性最强的是
(4)写出A、B最高正价氧化物对应的水化物之间反应的离子方程式:
查看习题详情和答案>>
(1)A是
Na
Na
元素,B是Al
Al
元素,C是Cl
Cl
元素;(2)B的离子结构示意图是


NH3+HCl═NH4Cl
NH3+HCl═NH4Cl
;(3)A、C元素形成化合物的电子式是
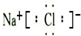
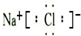
HF
HF
(填氢化物化学式).(4)写出A、B最高正价氧化物对应的水化物之间反应的离子方程式:
Al(OH)3+OH-=AlO2-+2H2O
Al(OH)3+OH-=AlO2-+2H2O
.