网址:http://m.1010jiajiao.com/timu3_id_56205[举报]
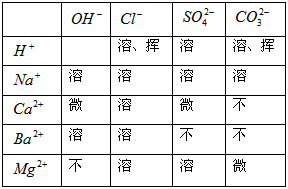
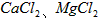 及一些硫酸盐,应加入什么试剂?可参考资料卡片中相应物质的溶解性。
及一些硫酸盐,应加入什么试剂?可参考资料卡片中相应物质的溶解性。 
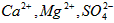 及泥沙,得到纯净的
及泥沙,得到纯净的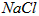 ,可将粗盐溶于水,然后在下列操作中选取必要的步骤和正确的操作顺序____________。(填序号)
,可将粗盐溶于水,然后在下列操作中选取必要的步骤和正确的操作顺序____________。(填序号) ① 过滤;② 加过量NaOH溶液;③ 加适量盐酸;④ 加过量
 溶液;⑤ 加过量
溶液;⑤ 加过量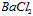 溶液
溶液(2)甲、乙两相邻的化工厂,排放的污水经处理后,仍然溶有以下八种离子
(
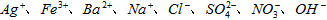 )中各不相同的4种,若单独排放,则造成环境污染,如果将甲、乙两厂的污水按适当比例充分混合,再经沉淀后,排放的污水转变为无色澄清的
)中各不相同的4种,若单独排放,则造成环境污染,如果将甲、乙两厂的污水按适当比例充分混合,再经沉淀后,排放的污水转变为无色澄清的________________,污染程度大为降低,又经测定,甲厂污水的pH大于7,试推断:
甲厂污水中含有的4种离子是________________;乙厂污水中含有的4种离子是_______________。
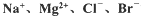 等)中模拟工业生产来提取镁,主要过程如下,回答下列问题:
等)中模拟工业生产来提取镁,主要过程如下,回答下列问题: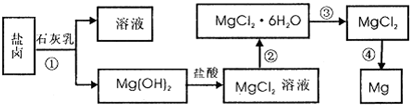
(2)写出转化④中发生反应的化学方程式__________________
(3)已知转化③的反应原理与制取无水AlCl3相同,下图是制取无水AlCl3实验装置图。装置A中的两液体分别是浓硫酸和浓盐酸。请回答:
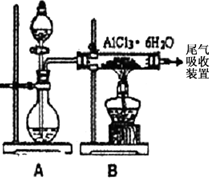
②分液漏斗中应盛装的试剂是_________;
③由分液漏斗向烧瓶中加试剂时应注意的事项是_________
(4)含有铝元素的另一物质明矾作为膨化剂炸油条(饼)或膨化食品时,若在面粉里加入小苏打后,再加入明矾,则会使等量的小苏打释放出比单放小苏打多一倍的二氧化碳,这样就可以使油条(饼)在热油锅中一下子就鼓起来,得到香脆可口的油条(饼)了。请用化学反应方程式解释得到香脆可口的油条(饼)的原因:_____________________。
某研究小组在实验室探究氨基甲酸铵(H2NCOONH4)水解反应速率的测定和分解反应平衡常数。
(1)已知:H2NCOONH4+2H2O![]() NH4HCO3+NH3·H2O。该研究小组分别用三份不同初始浓度的氨基甲酸铵溶液测定水解反应速率,得到c(H2NCOO-)随时间变化趋势如图所示。
NH4HCO3+NH3·H2O。该研究小组分别用三份不同初始浓度的氨基甲酸铵溶液测定水解反应速率,得到c(H2NCOO-)随时间变化趋势如图所示。
![]()

①25℃时,0~6min氨基甲酸铵水解反应的平均速率为 。
②对比图中哪两条曲线,能得出“水解反应速率随温度升高而增大”的结论? 。
(2)将一定量纯净的氨基甲酸铵置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:H2NCOONH4(s)![]() 2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据列于下表:
2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据列于下表:
| 温度(℃) | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡总压强(kPa) | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
| 平衡气体总浓度 (×10-3mol/L) | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
③能标志该分解反应已经达到化学平衡状态的是 。
A.单位时间内生成1 mol CO2的同时消耗2 mol NH3
B.容器内气体压强保持不变
C.容器中CO2与NH3的物质的量之比保持不变
D.容器中混合气体的密度保持不变
④根据表中数据计算,15.0℃时的分解平衡常数(Kc)为 。
⑤氨基甲酸铵分解反应属于 反应(填放热或吸热),理由是 。
⑥氨基甲酸铵分解反应的熵变△S 0(填>、<或=)。
查看习题详情和答案>>硫酸亚铁铵是一种浅蓝绿色晶体,俗称摩尔盐,其化学式为FeSO4·(NH4)2SO4·6H2O.硫酸亚铁在空气中易被氧化,而形成摩尔盐后就稳定了.硫酸亚铁铵可由硫酸亚铁与硫酸铵等物质的量混合制得.三种盐的溶解度(单位为g/100 g水)如下表:

下图是模拟工业制备硫酸亚铁铵晶体的实验装置.

回答下列问题:
Ⅰ.(1)先用30%的氢氧化钠溶液煮沸废铁屑(含少量油污、铁锈、FeS等),再用清水洗净.用氢氧化钠溶液煮沸的目的是________________.
(2)将处理好的铁屑放人锥形瓶中,加人稀硫酸.锥形瓶中发生反应的离子方程式可能为________________ (填序号).
A.Fe+2H+=Fe2++H2↑
B.Fe2O3+6H+=2Fe3++3H2O
C.2Fe3++S2-=2Fe2++S↓
D.2Fe3++Fe=3Fe2+
(3)利用容器②的反应,向容器①中通入氢气,应关闭活塞________,打开活塞________(填字母).容器③中NaOH溶液的作用是________________;向容器①中通入氢气的目的是________________.
Ⅱ.待锥形瓶中的铁屑快反应完时,关闭活塞B、C,打开活塞A,继续产生的氢气会将锥形瓶中的硫酸亚铁(含极少部分未反应的稀硫酸)压到饱和硫酸铵溶液的底部.在常温下放置一段时间,试剂瓶底部将结晶出硫酸亚铁铵.
硫酸亚铁与硫酸铵溶液混合就能得到硫酸亚铁铵晶体,其原因是_____________;从容器①中分离并得到纯净硫酸亚铁铵晶体的操作方法是________、________、________________.
Ⅲ.制得的硫酸亚铁铵晶体中往往含有极少量的Fe3+.为测定晶体中Fe2+的含量,称取一份质量为20.0 g的硫酸亚铁铵晶体样品,制成溶液.用0.5 mol·L-1 KMnO4溶液滴定,当溶液中Fe2+全部被氧化,MnO4-被还原成Mn2+时,耗KMnO4溶液体积20.00 mL.
滴定时,将KMnO4溶液装在________(酸式或碱式)滴定管中,判断反应到达滴定终点的现象为________________;晶体中FeSO4的质量分数为________.
(4分)铁的氧化物有多种用途。请解答下面有关问题:
(1)赤铁矿的主要成分是Fe2O3,是工业炼铁的主要原料之一。写出由Fe2O3制得单质铁的化学方程式 。某赤铁矿除了含Fe2O3之处,还含有少量的SiO2和Al2O3。将试样溶于NaOH溶液,充分反应过滤,即可得到较纯净的Fe2O3。发生反应的离子方程式是 。
(2)Fe2O3可以与铝粉组成铝热剂用于焊接钢轨或定向爆破。某同学猜测,该反应所得熔融物中含有Fe2O3。他设计如下实验来验证自己的猜想:取少量试样,加入足量 稀盐酸,然后滴加KSCN溶液,若出现血红色,证明含有Fe2O3。否则,不含有Fe2O3。
你认为该方案合理吗?为什么? 。
(3)合成氨工业中所用的α―Fe催化剂的主要成分是FeO、Fe2O3。已知当催化剂中Fe2+和Fe3+的物质的量之比为1:2时,其催化活性最高。某化学小组试图以Fe2O3为原料制备该催化剂,方法之一是向其中加入炭粉高温反应:
![]()
实验教师提供了12g炭粉。请你计算,若要制取这种活性最高的催化剂,加入的Fe2O3的质量为 g。 该小组设计了多个实验方案来测定所得产品是否符合要求。其中一个实验方案是用氢气还原加热的混合物,测定铁的质量分数。在用锌跟稀硫酸反应制取氢气时,该小组的同学向稀硫酸中加入少量硫酸铜溶液,目的是 。当混合物中铁的质量分数为 (用化简的分数表示)时,该产品合格。
查看习题详情和答案>>