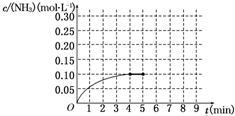
摘要:22. 在一容积为2L的密闭容器中.加入0.2mol的N2和0.6mol的H2.在一定条件下发生如下反应: N2(g)+3H2(g) 2NH3(g),△H<0 反应中NH3的物质的量浓度的变化情况如右图所示.请回答下列问题: (1)根据右图.计算从反应开始到平衡时.平均反应速率v(NH3)为 . (2)该反应到平衡时H2的转化率 . (3)反应达到平衡后.第5分钟末.保持其它条件不变.若改变反应温度.则NH3的物质的量浓度不可能为 .. a 0.20mol·L-1 b 0.12 mol·L-1 c 0.10 mol·L-1 d 0.08 mol·L-1 (4)反应达到平衡后.第5分钟末.保持其它条件不变.若只把容器的体积缩小一半.平衡向 移动(填“向逆反应方向 .“向正反应方向 或“不 ).化学平衡常数 (填“增大 .“减少 或“不变 ). (5)在第5分钟末将容器的体积缩小一半后.若在第8分钟末达到新的平衡(此时NH3的浓度约为0.25 mol·L-1 ).请在上图中画出第5分钟末到此平衡时NH3浓度的变化曲线.
网址:http://m.1010jiajiao.com/timu3_id_56039[举报]
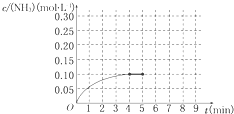 在一容积为2L的密闭容器中,加入0.2mol的N2和0.6mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g)?2NH3(g)△H<0反应中NH3的物质的量浓度的变化情况如图所示,请回答下列问题:
在一容积为2L的密闭容器中,加入0.2mol的N2和0.6mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g)?2NH3(g)△H<0反应中NH3的物质的量浓度的变化情况如图所示,请回答下列问题:(1)根据如图,计算从反应开始到平衡时,平衡反应速率v(NH3)为
0.025
0.025
mol/(L?min).(2)该反应达到平衡时H2的转化率
50%
50%
.(3)反应达到平衡后,第5分钟末,保持其它条件不变,若改变反应温度,则NH3的物质的量浓度不可能为
a
a
.(填序号)a.0.20mol?L-1 b.0.12mol?L-1 c.0.10mol?L-1 d.0.08mol?L-1
(4)反应达到平衡后,第5分钟末,保持其它条件不变,若只把容器的体积缩小一半,平衡
向正反应方向
向正反应方向
移动(填“向逆反应方向”、“向正反应方向”或“不”).(5)在第5分钟末将容器的体积缩小一半后,若在第8分钟末达到新的平衡(此时NH3的浓度约为0.25mol?L-1),请在图中画出第5分钟末到此平衡时NH3浓度的变化曲线.
 在一容积为2L的密闭容器中,加入0.2mol的N2和0.6mol的H2,在一定条件下发生反应:N2(g)+3H2(g)?2NH3(g)△H<0.反应中NH3的物质的量浓度的变化情况如下图所示,请回答下列问题:
在一容积为2L的密闭容器中,加入0.2mol的N2和0.6mol的H2,在一定条件下发生反应:N2(g)+3H2(g)?2NH3(g)△H<0.反应中NH3的物质的量浓度的变化情况如下图所示,请回答下列问题:(1)根据上图,计算从反应开始到平衡时,氢气的平均反应速率v(H2)为
0.0375mol/(L.min)
0.0375mol/(L.min)
.(2)该反应达到平衡时N2的转化率
50%
50%
.(3)反应达到平衡后,第5分钟末,保持其它条件不变,若改变反应温度,则NH3的物质的量浓度不可能为
a
a
.(填序号)a.0.20mol?L-1 b.0.12mol?L-1 c.0.10mol?L-1 d.0.08mol?L-1
(4)请写出该反应的平衡常数表达式
K=
| c2(NH3) |
| c(N2)×c3(H2) |
K=
,若该反应在298K、398K时的化学平衡常数分别为K1、K2,则K1| c2(NH3) |
| c(N2)×c3(H2) |
>
>
K2(填“>”、“=”或“<”).(5)在第5分钟末将容器的体积缩小一半后,若在第8分钟末达到新的平衡(此时NH3的浓度约为0.25mol?L-1),请在上图中画出第5分钟末到此平衡时NH3浓度的变化曲线.
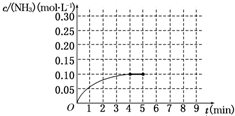 在一容积为2L的密闭容器中,加入0.2mol的N2和0.6mol的H2,在一定条件下发生反应:N2(g)+3H2(g)?2NH3(g)△H<0.反应中NH3的物质的量浓度的变化情况如图所示.反应达到平衡后,第5分钟末,保持其它条件不变,若改变反应温度,则NH3的物质的量浓度不可能为( )
在一容积为2L的密闭容器中,加入0.2mol的N2和0.6mol的H2,在一定条件下发生反应:N2(g)+3H2(g)?2NH3(g)△H<0.反应中NH3的物质的量浓度的变化情况如图所示.反应达到平衡后,第5分钟末,保持其它条件不变,若改变反应温度,则NH3的物质的量浓度不可能为( )
查看习题详情和答案>>
在一容积为2L的密闭容器中,加入0.2mol的N2和0.6mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g) 2NH3(g);△H<0
2NH3(g);△H<0
反应中NH3的物质的量浓度的变化情况如右图所示,请回答下列问题: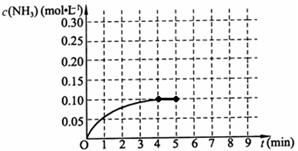
(1)根据右图,写出该反应达到平衡时H2的转化率 。
(2)反应达到平衡后,第5分钟末,保持其它条件不变,若改变反应温度,则NH3的物质的量浓度不可能为 。(填序号)。
a 0.20mol·L-1 b 0.12 mol·L-1
c 0.10 mol·L-1 d 0.08 mol·L-1
(3)反应达到平衡后,第5分钟末,保持其它条件不变,若只把容器的体积缩小一半,平衡向 移动(填“向逆反应方向”、“向正反应方向”或“不”),化学平衡常数 (填“增大”、“减少”或“不变”)。
(4)在第5分钟末将容器的体积缩小一半后,若在第8分钟末达到新的平衡(此时NH3的浓度约为0.25 mol·L-1 ),请在上图中画出第5分钟末到此平衡时NH3浓度的变化曲线。