摘要:9.下列实验或操作不能达到目的的是 A.为提高KMnO4溶液的氧化能力用盐酸将KMnO4溶液酸化 B.从含I的溶液中提取碘.应先加入适量的稀硫酸和稀H2O2溶液.再用苯萃取 C.称取0.4 g的NaOH固体配成1000 mL.浓度为0.010 mol·L的NaOH溶液 D.检验溴乙烷中的溴时.应先加入NaOH溶液并加热.再加入稀硝酸.最后加入硝 酸银溶液
网址:http://m.1010jiajiao.com/timu3_id_55468[举报]
下列实验或操作不能达到目的的是
A.为提高KMnO4溶液的氧化能力用盐酸将KMnO4溶液酸化
B.从含I![]() 的溶液中提取碘,应先加入适量的稀硫酸和稀H2O2溶液,再用苯萃取
的溶液中提取碘,应先加入适量的稀硫酸和稀H2O2溶液,再用苯萃取
C.称取0.4 g的NaOH固体配成1000 mL,浓度为0.010 mol?L![]() 的NaOH溶
的NaOH溶
D.检验溴乙烷中的溴时,应先加入NaOH溶液并加热,再加入稀硝酸,最后加入硝酸银溶液
查看习题详情和答案>>
据新闻报道有全国最“绿”省份之称的福建,近年来却频频受到酸雨的困扰.在饮用水源地水质状况方面,福建9个设区市的34个集中式生活饮用水源地水质达标率为73.3%,较上年同期有所下降.所以保护环境是我们刻不容缓的责任.
Ⅰ、烟气脱硫是控制二氧化硫污染的主要技术手段.
(1)利用海水脱硫是一种有效的方法,其工艺流程如图1所示:
某研究小组为探究提高含硫烟气中SO2的吸收效率的措施,进行了天然海水(pH≈8)吸收含硫烟气的模拟实验,实验结果如图2所示.
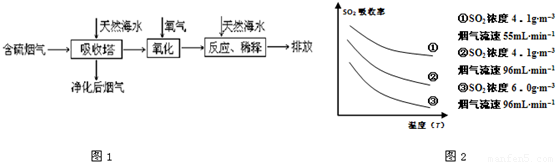
①根据图示实验结果,为了提高一定浓度含硫烟气中SO2的吸收效率,下列措施正确的是______.(填字母序号)
A.降低通入含硫烟气的温度 B.减小通入含硫烟气的流速
C.减少天然海水的进入量 D.在天然海水中加入生石灰
②天然海水吸收了含硫烟气后会溶有H2SO3,使用空气中的氧气将其氧化,写出该反应的化学方程式:______.氧化后的“海水”需要用大量的天然海水与之混合后才能排放,该操作的主要目的是______.
(2)石灰石-石膏湿法烟气脱硫工艺技术的工作原理是烟气中的二氧化硫与浆液中的碳酸钙以及鼓入的空气反应生成石膏.写出该反应的化学方程式:______.
Ⅱ.重金属离子对河流及海洋造成严重污染.某化工厂废水(pH≈2)中含有Ag+、Pb2+等重金属离子,其浓度各约为0.01mol?L-1.排放前拟用沉淀法除去这两种离子,查找有关数据如下:
(3)你认为往废水中投入______(填字母序号),沉淀效果最好.
A.NaOH B.Na2S C.KI D.Ca(OH)2
(4)如果只用生石灰处理含有Pb2+的废水,使溶液的pH=8.0,处理后的废水中,c(Pb2+)=______.若环境要求污水综合排放标准为c(Pb2+)低于1.0×l0-8mol?L-1,问处理后的废水是否符合排放标准?______ (填“是”或“否”).
查看习题详情和答案>>
Ⅰ、烟气脱硫是控制二氧化硫污染的主要技术手段.
(1)利用海水脱硫是一种有效的方法,其工艺流程如图1所示:
某研究小组为探究提高含硫烟气中SO2的吸收效率的措施,进行了天然海水(pH≈8)吸收含硫烟气的模拟实验,实验结果如图2所示.

①根据图示实验结果,为了提高一定浓度含硫烟气中SO2的吸收效率,下列措施正确的是______.(填字母序号)
A.降低通入含硫烟气的温度 B.减小通入含硫烟气的流速
C.减少天然海水的进入量 D.在天然海水中加入生石灰
②天然海水吸收了含硫烟气后会溶有H2SO3,使用空气中的氧气将其氧化,写出该反应的化学方程式:______.氧化后的“海水”需要用大量的天然海水与之混合后才能排放,该操作的主要目的是______.
(2)石灰石-石膏湿法烟气脱硫工艺技术的工作原理是烟气中的二氧化硫与浆液中的碳酸钙以及鼓入的空气反应生成石膏.写出该反应的化学方程式:______.
Ⅱ.重金属离子对河流及海洋造成严重污染.某化工厂废水(pH≈2)中含有Ag+、Pb2+等重金属离子,其浓度各约为0.01mol?L-1.排放前拟用沉淀法除去这两种离子,查找有关数据如下:
| 难溶电解质 | AgI | AgOH | Ag2S | PbI2 | Pb(OH)2 | PbS |
| Ksp | 8.3×10-17 | 5.6×10-8 | 6.3×10-50 | 7.1×10-9 | 1.2×10-15 | 3.4×10-28 |
A.NaOH B.Na2S C.KI D.Ca(OH)2
(4)如果只用生石灰处理含有Pb2+的废水,使溶液的pH=8.0,处理后的废水中,c(Pb2+)=______.若环境要求污水综合排放标准为c(Pb2+)低于1.0×l0-8mol?L-1,问处理后的废水是否符合排放标准?______ (填“是”或“否”).
查看习题详情和答案>>
据新闻报道有全国最“绿”省份之称的福建,近年来却频频受到酸雨的困扰.在饮用水源地水质状况方面,福建9个设区市的34个集中式生活饮用水源地水质达标率为73.3%,较上年同期有所下降.所以保护环境是我们刻不容缓的责任.
Ⅰ、烟气脱硫是控制二氧化硫污染的主要技术手段.
(1)利用海水脱硫是一种有效的方法,其工艺流程如图1所示:
某研究小组为探究提高含硫烟气中SO2的吸收效率的措施,进行了天然海水(pH≈8)吸收含硫烟气的模拟实验,实验结果如图2所示.

①根据图示实验结果,为了提高一定浓度含硫烟气中SO2的吸收效率,下列措施正确的是______.(填字母序号)
A.降低通入含硫烟气的温度 B.减小通入含硫烟气的流速
C.减少天然海水的进入量 D.在天然海水中加入生石灰
②天然海水吸收了含硫烟气后会溶有H2SO3,使用空气中的氧气将其氧化,写出该反应的化学方程式:______.氧化后的“海水”需要用大量的天然海水与之混合后才能排放,该操作的主要目的是______.
(2)石灰石-石膏湿法烟气脱硫工艺技术的工作原理是烟气中的二氧化硫与浆液中的碳酸钙以及鼓入的空气反应生成石膏(CaSO4?2H2O).写出该反应的化学方程式:______.
Ⅱ.重金属离子对河流及海洋造成严重污染.某化工厂废水(pH≈2)中含有Ag+、Pb2+等重金属离子,其浓度各约为0.01mol?L-1.排放前拟用沉淀法除去这两种离子,查找有关数据如下:
| 难溶电解质 | AgI | AgOH | Ag2S | PbI2 | Pb(OH)2 | PbS |
| Ksp | 8.3×10-17 | 5.6×10-8 | 6.3×10-50 | 7.1×10-9 | 1.2×10-15 | 3.4×10-28 |
A.NaOH B.Na2S C.KI D.Ca(OH)2
(4)如果只用生石灰处理含有Pb2+的废水,使溶液的pH=8.0,处理后的废水中,c(Pb2+)=______.若环境要求污水综合排放标准为c(Pb2+)低于1.0×l0-8mol?L-1,问处理后的废水是否符合排放标准?______ (填“是”或“否”). 查看习题详情和答案>>
三农问题是政府和社会关注的问题,化肥是土地的营养品.某农资商店出售一种化肥,其有效成分为氯化铵,现欲测定该种化肥中氮元素的质量分数,设计实验步骤如下(杂质中不含氮元素,且杂质均不与盐酸或氢氧化钠溶液反应):
①配制1.00mol/L的HCl溶液和1.00mol/L的NaOH溶液;
②每次取1.00g此化肥样品,溶于20mL蒸馏水中;
③加入30.00mL1.00mol/L的NaOH溶液,将反应后的溶液加热煮沸约1分钟,冷却至常温;
④…;
⑤重复②③④步操作1-2次;
⑥记录整理实验所得数据,计算该化肥中氮元素的质量分数.
请回答下列问题:
(1)写出步骤④中的实验内容
(2)下列仪器中,配制盐酸和氢氧化钠溶液都能用到的是
A.玻璃棒 B.托盘天平 C.烧杯 D.漏斗
(3)步骤⑤的实验目的是
(4)配制本实验所需的1.00mol/L的盐酸和1.00mol/L的NaOH溶液从节约化学药品的角度出发,最好应选用的容量瓶规格分别为
A.50mL,50mL B.150mL,100mL C.100mL,150mL D.250mL,500mL
(5)若以Vx(mL)表示实验所测定消耗盐酸数据的平均值,该化肥样品中氮元素的质量分数计算表达式为
×100%
×100%.(不需要化简)
查看习题详情和答案>>
①配制1.00mol/L的HCl溶液和1.00mol/L的NaOH溶液;
②每次取1.00g此化肥样品,溶于20mL蒸馏水中;
③加入30.00mL1.00mol/L的NaOH溶液,将反应后的溶液加热煮沸约1分钟,冷却至常温;
④…;
⑤重复②③④步操作1-2次;
⑥记录整理实验所得数据,计算该化肥中氮元素的质量分数.
请回答下列问题:
(1)写出步骤④中的实验内容
以酚酞为指示剂,用1.00mol/L的HCl溶液滴定,达到滴定终点用去V(mL)
以酚酞为指示剂,用1.00mol/L的HCl溶液滴定,达到滴定终点用去V(mL)
,写出实验步骤④中的离子方程式:OH-+H+═H2O
OH-+H+═H2O
.(2)下列仪器中,配制盐酸和氢氧化钠溶液都能用到的是
AC
AC
A.玻璃棒 B.托盘天平 C.烧杯 D.漏斗
(3)步骤⑤的实验目的是
减小误差,提高实验结果的准确度
减小误差,提高实验结果的准确度
.(4)配制本实验所需的1.00mol/L的盐酸和1.00mol/L的NaOH溶液从节约化学药品的角度出发,最好应选用的容量瓶规格分别为
C
C
(填字母选项).A.50mL,50mL B.150mL,100mL C.100mL,150mL D.250mL,500mL
(5)若以Vx(mL)表示实验所测定消耗盐酸数据的平均值,该化肥样品中氮元素的质量分数计算表达式为
| (30×10-3L×1mol/L-Vx×10-3L×1mol/L)×14g/mol |
| 1g |
| (30×10-3L×1mol/L-Vx×10-3L×1mol/L)×14g/mol |
| 1g |
据新闻报道有全国最“绿”省份之称的福建,近年来却频频受到酸雨的困扰.在饮用水源地水质状况方面,福建9个设区市的34个集中式生活饮用水源地水质达标率为73.3%,较上年同期有所下降.所以保护环境是我们刻不容缓的责任.
Ⅰ、烟气脱硫是控制二氧化硫污染的主要技术手段.
(1)利用海水脱硫是一种有效的方法,其工艺流程如图1所示:
某研究小组为探究提高含硫烟气中SO2的吸收效率的措施,进行了天然海水(pH≈8)吸收含硫烟气的模拟实验,实验结果如图2所示.
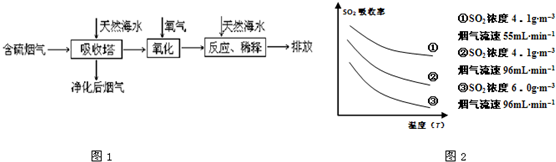
①根据图示实验结果,为了提高一定浓度含硫烟气中SO2的吸收效率,下列措施正确的是
A.降低通入含硫烟气的温度 B.减小通入含硫烟气的流速
C.减少天然海水的进入量 D.在天然海水中加入生石灰
②天然海水吸收了含硫烟气后会溶有H2SO3,使用空气中的氧气将其氧化,写出该反应的化学方程式:
(2)石灰石-石膏湿法烟气脱硫工艺技术的工作原理是烟气中的二氧化硫与浆液中的碳酸钙以及鼓入的空气反应生成石膏(CaSO4?2H2O).写出该反应的化学方程式:
Ⅱ.重金属离子对河流及海洋造成严重污染.某化工厂废水(pH≈2)中含有Ag+、Pb2+等重金属离子,其浓度各约为0.01mol?L-1.排放前拟用沉淀法除去这两种离子,查找有关数据如下:
(3)你认为往废水中投入
A.NaOH B.Na2S C.KI D.Ca(OH)2
(4)如果只用生石灰处理含有Pb2+的废水,使溶液的pH=8.0,处理后的废水中,c(Pb2+)=
查看习题详情和答案>>
Ⅰ、烟气脱硫是控制二氧化硫污染的主要技术手段.
(1)利用海水脱硫是一种有效的方法,其工艺流程如图1所示:
某研究小组为探究提高含硫烟气中SO2的吸收效率的措施,进行了天然海水(pH≈8)吸收含硫烟气的模拟实验,实验结果如图2所示.

①根据图示实验结果,为了提高一定浓度含硫烟气中SO2的吸收效率,下列措施正确的是
AB
AB
.(填字母序号)A.降低通入含硫烟气的温度 B.减小通入含硫烟气的流速
C.减少天然海水的进入量 D.在天然海水中加入生石灰
②天然海水吸收了含硫烟气后会溶有H2SO3,使用空气中的氧气将其氧化,写出该反应的化学方程式:
2H2SO3+O2=2H2SO4
2H2SO3+O2=2H2SO4
.氧化后的“海水”需要用大量的天然海水与之混合后才能排放,该操作的主要目的是中和、稀释经氧气氧化后海水中生成的酸(H+)
中和、稀释经氧气氧化后海水中生成的酸(H+)
.(2)石灰石-石膏湿法烟气脱硫工艺技术的工作原理是烟气中的二氧化硫与浆液中的碳酸钙以及鼓入的空气反应生成石膏(CaSO4?2H2O).写出该反应的化学方程式:
2CaCO3+2SO2+O2+4H2O═2CaSO4?2H2O+2CO2
2CaCO3+2SO2+O2+4H2O═2CaSO4?2H2O+2CO2
.Ⅱ.重金属离子对河流及海洋造成严重污染.某化工厂废水(pH≈2)中含有Ag+、Pb2+等重金属离子,其浓度各约为0.01mol?L-1.排放前拟用沉淀法除去这两种离子,查找有关数据如下:
| 难溶电解质 | AgI | AgOH | Ag2S | PbI2 | Pb(OH)2 | PbS |
| Ksp | 8.3×10-17 | 5.6×10-8 | 6.3×10-50 | 7.1×10-9 | 1.2×10-15 | 3.4×10-28 |
B
B
(填字母序号),沉淀效果最好.A.NaOH B.Na2S C.KI D.Ca(OH)2
(4)如果只用生石灰处理含有Pb2+的废水,使溶液的pH=8.0,处理后的废水中,c(Pb2+)=
1.2×10-3mol?L-1
1.2×10-3mol?L-1
.若环境要求污水综合排放标准为c(Pb2+)低于1.0×l0-8mol?L-1,问处理后的废水是否符合排放标准?否
否
(填“是”或“否”).