网址:http://m.1010jiajiao.com/timu3_id_53770[举报]
 分别回答下列问题.
分别回答下列问题.(1)从H+、Na+、Cu2+、Cl-、S
| O | 2- 4 |
①电解过程中溶液颜色变浅且水量不变
②电解过程中电解质含量不变,水量减少
③电解过程中,两极析出气体的体积比为1:1
(2)①用惰性电极电解硫酸铜溶液,若阴极上有1.6克铜析出,则阳极上产生的气体在标准状况下的体积约为
②用铂电极电解0.02mol/L硫酸铜溶液,直至铜完全析出,所得溶液中氢离子浓度为(忽略溶液体积的变化)
③已知下列两个热化学方程式2H2(g)+O2(g)=2H2O(1)△H=-571.6KJ;C3H8(g)+5O2(g)=3CO2(g)+4H2O(1)△H=-2220.0kJ实验测得,5mol氢气和丙烷的混合气体完全燃烧时放热3847kJ,则混合气体中氢气与丙烷的体积比是
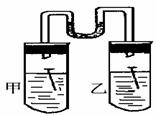
(3)如图所示,甲、乙两试管中各放一枚铁钉,甲试管中为NaCl溶液,乙试管为稀醋酸溶液,数天后观察到的现象
是
分别回答下列问题。(10分)
(1)从H+、Na+、Cu2+、Cl-、![]() 中选出两种离子组成电解质,按下列要求进行电解(使用惰性电极),将电解质的化学式填空:(只写出一种即可)
中选出两种离子组成电解质,按下列要求进行电解(使用惰性电极),将电解质的化学式填空:(只写出一种即可)
①电解过程中溶液颜色变浅且水量不变_______________________;
②电解过程中电解质含量不变,水量减少_______________________;
③电解过程中,两极析出气体的体积比为1∶1__________。
(2)①用惰性电极电解硫酸铜溶液,若阴极上有1.6克铜析出,则阳极上产生的气体
在标准状况下的体积约为 ;
②用铂电极电解0.02 mol/L硫酸铜溶液,直至铜完全析出,所得溶液中氢离子浓度为
(忽略溶液体积的变化) ;
③已知下列两个热化学方程式2H2(g)+O2(g)=2H2O(1) △H= -571.6KJ
 C3H8(g) +5O2(g)=3CO2(g)+4H2O(1) △H=-2220.0kJ
C3H8(g) +5O2(g)=3CO2(g)+4H2O(1) △H=-2220.0kJ
实验测得,5mol氢气和丙烷的混合气体完全燃烧时放热
3847kJ,则混合气体中氢气与丙烷的体积比是 。
(3)如右图所示,甲、乙两试管中各放一枚铁钉,甲试管中
为NaCl溶液,乙试管为稀醋酸溶液,数天后观察到的现象
是 ,甲中正极反应为
,负极反应式为,乙中正极反应为 ,负极反应式为 。
查看习题详情和答案>>