摘要:6.谨防因一字之差落入“陷阱 在审题时.看清题干中的每一个字.特别是关键信息.谨防粗心大意.而落人“陷阱 . 例1 在25℃时.将2个铜电极插入到一定的Na2S04饱和溶液中.通直流电电解并不断搅拌.当阴极上收集到a mol的气体的同时.溶液中析出了b mol的结晶水合物Na2S04·10H20.若保持温度不变.则所剩溶液中溶质的质量分数是( ). A. B. C. D. 通电 分析:电解发生的电极反应:阳极为Cu-2e=Cu2+.阴极为2H++2e=H2↑. 电解时总的化学反应方程式为:Cu十2H20=====Cu(OH)2↓十H2↑ 阴极逸出a molH2.水被电解了2a mol.根据溶解度知识.不难求出答案为C.如果将 电解 题中的铜电极换作铂电极.只改一个字.其电解的总方程式即为: 2H20=====2H2↑+O2↑ 阴极逸出a mol H2.水被电解了a mol.其答案为D. 可见因一字之差.答案各异.
网址:http://m.1010jiajiao.com/timu3_id_53676[举报]
HIV能通过细胞表面的CD4(一种受体蛋白)识别T细胞(如图甲),如果给AIDS患者大量注射用CD4修饰过的红细胞,红细胞也会被HIV识别、入侵(如图乙)。因HIV在红细胞内无法增殖,红细胞成为HIV的“陷阱细胞”。这为治疗AIDS提供了新的思路。据材料分析,下列叙述不正确的是 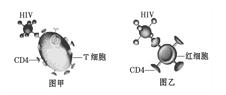
A.CD4与双缩脲试剂反应呈紫色
B.HIV通过攻击红细胞可使人的免疫功能全部丧失
C.红细胞可作为“陷阱细胞”与其结构有关
D.入侵到红细胞的HIV随红细胞凋亡后可被免疫系统清除
查看习题详情和答案>>(2013?闸北区二模)氯气是一种重要的化工原料.某学习小组在实验室中利用如图所示装置制取氯气并探究其性质.
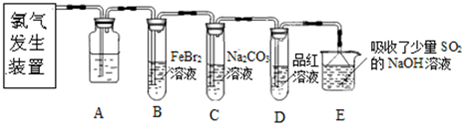
(1)实验室用二氧化锰和浓盐酸加热制取氯气,发生装置中除圆底烧瓶和导管外还需用到的玻璃仪器有
(2)装置A中盛有的试剂是
(3)若D中品红溶液褪色,则B装置中发生反应的离子方程式是
(4)证明FeBr2与Cl2发生了氧化还原反应的实验方法是
某研究性学习小组用刚吸收过少量SO2的NaOH溶液吸收处理上述实验后的尾气.经分析吸收尾气一段时间后,吸收液(呈强碱性)中肯定存在Cl-、OH-、CO32-和SO42-,对于可能存在的其他阴离子,研究小组提出以下3种假设.假设1:只存在SO32-;假设2:只存在ClO-;假设3:既不存在SO32-,也不存在ClO-.
(5)学习小组判断同时存在SO32-和ClO-是不可能的理由是
(6)现限选以下试剂,设计实验方案,进行实验,请写出实验步骤以及预期现象和结论.
a.3mol/L H2SO4 b.0.01mol/L KMnO4c.1mol/L BaCl2溶液
d.淀粉碘化钾溶液 e.酚酞试液
步骤一;取少量吸收液于试管中,滴加3mol/L H2SO4至溶液呈酸性,然后将所得溶液分装于A、B两试管中.
步骤二:向A试管中滴加少量
步骤三:向B试管中滴加少量
查看习题详情和答案>>

(1)实验室用二氧化锰和浓盐酸加热制取氯气,发生装置中除圆底烧瓶和导管外还需用到的玻璃仪器有
分液漏斗、酒精灯
分液漏斗、酒精灯
;(2)装置A中盛有的试剂是
饱和食盐水
饱和食盐水
,作用是除去氯气中的氯化氢
除去氯气中的氯化氢
.(3)若D中品红溶液褪色,则B装置中发生反应的离子方程式是
2Fe2++4Br-+3Cl2═2Fe3++6Cl-+2Br2
2Fe2++4Br-+3Cl2═2Fe3++6Cl-+2Br2
(4)证明FeBr2与Cl2发生了氧化还原反应的实验方法是
实验后,取少量B中溶液,滴加KSCN溶液;另取少量B中溶液,加入CCl4溶液萃取
实验后,取少量B中溶液,滴加KSCN溶液;另取少量B中溶液,加入CCl4溶液萃取
(填操作方法).某研究性学习小组用刚吸收过少量SO2的NaOH溶液吸收处理上述实验后的尾气.经分析吸收尾气一段时间后,吸收液(呈强碱性)中肯定存在Cl-、OH-、CO32-和SO42-,对于可能存在的其他阴离子,研究小组提出以下3种假设.假设1:只存在SO32-;假设2:只存在ClO-;假设3:既不存在SO32-,也不存在ClO-.
(5)学习小组判断同时存在SO32-和ClO-是不可能的理由是
SO32-和ClO-因发生氧化还原反应,故不能共存
SO32-和ClO-因发生氧化还原反应,故不能共存
.(6)现限选以下试剂,设计实验方案,进行实验,请写出实验步骤以及预期现象和结论.
a.3mol/L H2SO4 b.0.01mol/L KMnO4c.1mol/L BaCl2溶液
d.淀粉碘化钾溶液 e.酚酞试液
步骤一;取少量吸收液于试管中,滴加3mol/L H2SO4至溶液呈酸性,然后将所得溶液分装于A、B两试管中.
步骤二:向A试管中滴加少量
b
b
(填序号),若溶液褪色
褪色
(填现象),则假设1成立.步骤三:向B试管中滴加少量
d
d
(填序号),若溶液变蓝色
变蓝色
(填现象),则假设2成立.
近年来运用有机合成的方法制备出了许多具有下图所示立体结构的环状化合物,如
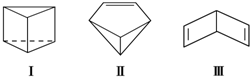
(1)写出上述物质Ⅱ的分子式 .
(2)Ⅰ、Ⅱ、Ⅲ之间的关系是
A.同素异形体 B.同系物 C.同分异构体 D.同种物质
(3)利用结构Ⅰ能解释苯的下列事实的是 ,利用结构Ⅱ或Ⅲ不能解释苯的下列事实的是 .
A.苯不能使酸性KMnO4溶液褪色
B.苯不能与溴水因发生化学反应而使溴水褪色
C.在一定条件下能和H2发生加成反应. 查看习题详情和答案>>

(1)写出上述物质Ⅱ的分子式
(2)Ⅰ、Ⅱ、Ⅲ之间的关系是
A.同素异形体 B.同系物 C.同分异构体 D.同种物质
(3)利用结构Ⅰ能解释苯的下列事实的是
A.苯不能使酸性KMnO4溶液褪色
B.苯不能与溴水因发生化学反应而使溴水褪色
C.在一定条件下能和H2发生加成反应. 查看习题详情和答案>>
 (2010?江苏一模)开发具有广谱、高效、低毒的杀菌、消毒剂是今后发展的趋势.
(2010?江苏一模)开发具有广谱、高效、低毒的杀菌、消毒剂是今后发展的趋势.(1)Cl2、H2O2、ClO2(还原产物为Cl-)、O3(1mol O3转化为 1mol O2和1mol H2O)等物质常被用作消毒剂.等物质的量的上述物质消毒效率最高的是
C
C
.(填序号)A.Cl2 B.H2O2 C.ClO2 D.O3
(2)氯氨(NH2Cl)可作为杀菌剂,请用化学方程式表示氯氨在水中的杀菌机理:
NH2Cl+H2O=NH3+HClO
NH2Cl+H2O=NH3+HClO
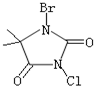
.(3)氯溴海因(C5H6BrClN2O2)是一种比较安全的氯气和氯制剂的替代产品,其结构式如右图所示:
氯溴海因在水中的水解过程比较复杂,主要是水解生成次卤酸和海因,请画出海因的结构式:
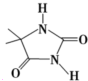

(4)以铂(Pt)和铁为电极,以KOH溶液为电解液,用电解法可制备高铁酸钾(K2FeO4).
写出阳极的电极反应式:
Fe+8OH--6e-=FeO42-+4H2O
Fe+8OH--6e-=FeO42-+4H2O
.