摘要:A.B.C.D.E五种芳香族化合物都是某些植物挥发油中的主要成分.有的是药物.有的是香料.它们的结构简式如下所示: 请回答下列问题: (1)这五种化合物中.互为同分异构体的是 反应①采取了适当措施.使分子中烯键不起反应.以上反应中的W是A-E中的某一化合物.则W是 . X是D的同分异构体.X的结构简式是 . 反应②属于 反应.
网址:http://m.1010jiajiao.com/timu3_id_51619[举报]
有A、B、C、D、E五种短周期元素,A元素的一种同位素原子核内不含中子,其单质为气体;B原子最外层电子数是次外层电子数的3倍,C 2+与B元素的离子具有相同的电子层结构;D与E原子具有相同的电子层数,且次外层电子数均为8;在同周期主族元素中原子半径E最大,D最小.回答下列问题:
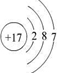
(1)C 2+离子与D原子的结构示意图分别为: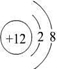
 、
、
 .
.
(2)B和E形成的两种化合物的电子式是:
 、
、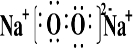
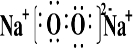
其中之一可与A 和B形成的化合物反应得到游离态B,写出该反应的化学方程式:
(3)由这五种元素中的几种形成的化合物中碱性最强的是
查看习题详情和答案>>
(1)C 2+离子与D原子的结构示意图分别为:




(2)B和E形成的两种化合物的电子式是:


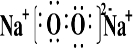
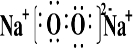
其中之一可与A 和B形成的化合物反应得到游离态B,写出该反应的化学方程式:
2Na2O2+2H2O=4NaOH+O2↑
2Na2O2+2H2O=4NaOH+O2↑
.(3)由这五种元素中的几种形成的化合物中碱性最强的是
NaOH
NaOH
(化学式),含氧酸酸性最强的是HClO4
HClO4
(化学式).(1)有A、B、C、D、E五种微粒:当A微粒失去3个电子后,电子层结构与氖原子相同;B微粒得到1个电子后,电子层结构与氩原子相同;C微粒带两个单位正电荷,核电荷数为12;D微粒有18个电子,当失去2个电子时显电中性;E微粒不带电,原子核中只有一个质子.请回答下列问题.
写出微粒的符号:A
(2)6.02×1024个Na+约含
查看习题详情和答案>>
写出微粒的符号:A
Al
Al
、BCl
Cl
、CMg2+
Mg2+
、DS2-
S2-
.(2)6.02×1024个Na+约含
10
10
mol Na+,其质量为230
230
g;4.5molCH4约含有2.709×1024(或4.5NA),
2.709×1024(或4.5NA),
个CH4,其质量为72
72
g.短周期A,B,C,D,E五种元素原子序数依次增大,A、B同主族,B、C、D三种元素原子形成的金属阳离子电子层结构相同,E元素原子最外层电子数等于A、B、C、D元素原子最外层电子数之和.A、B能形成原子个数比为1:1的离子化合物W,W易与水发生氧化还原反应,回答下列问题:
(1)W的电子式
(2)若以C、D两元素的单质作为电极①以A、E组成的化合物为电解质构成原电池,则负极为
(3)已知C单质与E单质可发生燃烧反应,以H2SO4作为电解质溶液设计成燃料电池,则负极反应式是
查看习题详情和答案>>
(1)W的电子式
Na+[:H]-
Na+[:H]-
,W与水反应的化学方程式NaH+H2O=NaOH+H2↑
NaH+H2O=NaOH+H2↑
.(2)若以C、D两元素的单质作为电极①以A、E组成的化合物为电解质构成原电池,则负极为
镁
镁
(填元素名称),正极反应式是2H++2e-=H2↑
2H++2e-=H2↑
. ②以B元素最高价氧化物的水化物为电解质构成原电池,则负极为铝
铝
(填元素名称),负极反应式是2Al+8OH--6e-=2AlO2-+4H2O
2Al+8OH--6e-=2AlO2-+4H2O
.(3)已知C单质与E单质可发生燃烧反应,以H2SO4作为电解质溶液设计成燃料电池,则负极反应式是
Mg-2e-═Mg2+
Mg-2e-═Mg2+
,正极反应式Cl2+2e-═2Cl-
Cl2+2e-═2Cl-
. 元素周期表短周期的一部分如表所示.下列有关A、B、C、D、E五种元素的叙述中,正确的是( )
元素周期表短周期的一部分如表所示.下列有关A、B、C、D、E五种元素的叙述中,正确的是( ) A、B、C、D、E五种物质都含1~18号元素中的某 一 元素,它们按图所示关系相互转化,已知A为单质.
A、B、C、D、E五种物质都含1~18号元素中的某 一 元素,它们按图所示关系相互转化,已知A为单质.