摘要:3.某学生的实验报告中有如下数据: ① 用托盘天平称取工业用碳酸钠样品10.62 g ② 用量筒量取40.8 mL盐酸, ③ 用pH试纸测得盐酸的pH为1.53, ④ 工业用碳酸钠晶体的样品中.结晶水含量为56.64%. 以上数据合理的是 ( ) A. ①③ B. ②④ C. ①④ D. ②③
网址:http://m.1010jiajiao.com/timu3_id_5093[举报]
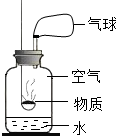 某校化学兴趣小组同学做镁带在空气中燃烧的实验时,发现白色生成物中混有少量淡黄色固体.针对这一现象,他们开展了如下实验探究.请仔细阅读并完成下列探究报告.
某校化学兴趣小组同学做镁带在空气中燃烧的实验时,发现白色生成物中混有少量淡黄色固体.针对这一现象,他们开展了如下实验探究.请仔细阅读并完成下列探究报告.探究目的:探究镁在空气中燃烧产生的淡黄色固体是镁与空气中什么物质反应产生的?
分析猜想:分析空气中各种成分,寻找猜想依据.
干燥空气中各组分气体的体积分数大约是:氮气
78
78
%,氧气21
21
%,稀有气体0.94%,二氧化碳0.03%,其他气体和杂质0.03%已学知识:氧气与镁反应生成的氧化镁是白色固体.
查阅资料:稀有气体化学性质稳定,一般不与其它物质反应.
猜想1:可能是镁与氮气反应生成淡黄色固体.
猜想2:可能是镁与二氧化碳反应生成淡黄色固体.
猜想3:可能是镁与
水蒸气
水蒸气
生成淡黄色固体.实验一:镁带与氮气的反应
(一)获取氮气
(1)把空气除尘净化,除去二氧化碳和水蒸气,液化后再蒸发,先蒸发出来的气体就是氮气.这种方法属于
物理
物理
(选填“物理”或“化学”)方法.但在实验室里空气不易被液化.(2)如图是获取氮气的方法及装置.用燃烧法除去空气(已除去二氧化碳、水蒸气和杂质)中的氧气从而得到较纯净的氮气,燃烧匙内选用的物质最好是
C
C
.A.木炭 B.蜡烛C.红磷 D.铁丝
(二)燃烧镁带,观察现象
将镁带打磨光亮,点燃,伸入盛氮气的集气瓶中,瓶内壁附着一层淡黄色的固体.
(三)实验结论:镁与氮气在点燃的条件下发生化合反应生成淡黄色的氮化镁(Mg3N2).
该反应的化学方程式是
3Mg+N2
Mg3N2
| ||
3Mg+N2
Mg3N2
.
| ||
实验二:将燃着的镁带伸入盛二氧化碳的集气瓶中,镁带剧烈燃烧,瓶内出现白色固体和黑色固体.生成的黑色固体物质的化学式是
C
C
.实验结论:镁在空气中燃烧产生的淡黄色固体是镁与空气中的
氮气
氮气
反应产生的.反思与评价:通过上述的实验及所学知识,你对燃烧的条件有什么新的认识?
物质的燃烧不一定有氧气参与
物质的燃烧不一定有氧气参与
.拓展与迁移:
不能
不能
(填“能”或“不能”)用镁条代替红磷完成测定空气中氧气含量的实验,理由是镁条不但能够和氧气反应,而且能够和氮气反应,所以若用镁条来代替红磷完成测定空气中氧气含量的实验,则会由于消耗了氮气而得出错误的结论
镁条不但能够和氧气反应,而且能够和氮气反应,所以若用镁条来代替红磷完成测定空气中氧气含量的实验,则会由于消耗了氮气而得出错误的结论
.某校化学兴趣小组同学做镁带在空气中燃烧的实验时,发现白色生成物中混有少量淡黄色固体.针对这一现象,他们开展了如下实验探究.请仔细阅读并完成下列探究报告.
探究目的:探究镁在空气中燃烧产生的淡黄色固体是镁与空气中什么物质反应产生的?
分析猜想:分析空气中各种成分,寻找猜想依据.
干燥空气中各组分气体的体积分数大约是:氮气______%,氧气______%,稀有气体0.94%,二氧化碳0.03%,其他气体和杂质0.03%
已学知识:氧气与镁反应生成的氧化镁是白色固体.
查阅资料:稀有气体化学性质稳定,一般不与其它物质反应.
猜想1:可能是镁与氮气反应生成淡黄色固体.
猜想2:可能是镁与二氧化碳反应生成淡黄色固体.
猜想3:可能是镁与______生成淡黄色固体.
实验一:镁带与氮气的反应
(一)获取氮气
(1)把空气除尘净化,除去二氧化碳和水蒸气,液化后再蒸发,先蒸发出来的气体就是氮气.这种方法属于______(选填“物理”或“化学”)方法.但在实验室里空气不易被液化.
(2)如图是获取氮气的方法及装置.用燃烧法除去空气(已除去二氧化碳、水蒸气和杂质)中的氧气从而得到较纯净的氮气,燃烧匙内选用的物质最好是______.
A.木炭 B.蜡烛C.红磷 D.铁丝
(二)燃烧镁带,观察现象
将镁带打磨光亮,点燃,伸入盛氮气的集气瓶中,瓶内壁附着一层淡黄色的固体.
(三)实验结论:镁与氮气在点燃的条件下发生化合反应生成淡黄色的氮化镁(Mg3N2).
该反应的化学方程式是______.
实验二:将燃着的镁带伸入盛二氧化碳的集气瓶中,镁带剧烈燃烧,瓶内出现白色固体和黑色固体.生成的黑色固体物质的化学式是______.
实验结论:镁在空气中燃烧产生的淡黄色固体是镁与空气中的______反应产生的.
反思与评价:通过上述的实验及所学知识,你对燃烧的条件有什么新的认识?______.
拓展与迁移:______(填“能”或“不能”)用镁条代替红磷完成测定空气中氧气含量的实验,理由是______.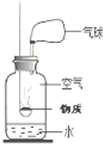
查看习题详情和答案>>
探究目的:探究镁在空气中燃烧产生的淡黄色固体是镁与空气中什么物质反应产生的?
分析猜想:分析空气中各种成分,寻找猜想依据.
干燥空气中各组分气体的体积分数大约是:氮气______%,氧气______%,稀有气体0.94%,二氧化碳0.03%,其他气体和杂质0.03%
已学知识:氧气与镁反应生成的氧化镁是白色固体.
查阅资料:稀有气体化学性质稳定,一般不与其它物质反应.
猜想1:可能是镁与氮气反应生成淡黄色固体.
猜想2:可能是镁与二氧化碳反应生成淡黄色固体.
猜想3:可能是镁与______生成淡黄色固体.
实验一:镁带与氮气的反应
(一)获取氮气
(1)把空气除尘净化,除去二氧化碳和水蒸气,液化后再蒸发,先蒸发出来的气体就是氮气.这种方法属于______(选填“物理”或“化学”)方法.但在实验室里空气不易被液化.
(2)如图是获取氮气的方法及装置.用燃烧法除去空气(已除去二氧化碳、水蒸气和杂质)中的氧气从而得到较纯净的氮气,燃烧匙内选用的物质最好是______.
A.木炭 B.蜡烛C.红磷 D.铁丝
(二)燃烧镁带,观察现象
将镁带打磨光亮,点燃,伸入盛氮气的集气瓶中,瓶内壁附着一层淡黄色的固体.
(三)实验结论:镁与氮气在点燃的条件下发生化合反应生成淡黄色的氮化镁(Mg3N2).
该反应的化学方程式是______.
实验二:将燃着的镁带伸入盛二氧化碳的集气瓶中,镁带剧烈燃烧,瓶内出现白色固体和黑色固体.生成的黑色固体物质的化学式是______.
实验结论:镁在空气中燃烧产生的淡黄色固体是镁与空气中的______反应产生的.
反思与评价:通过上述的实验及所学知识,你对燃烧的条件有什么新的认识?______.
拓展与迁移:______(填“能”或“不能”)用镁条代替红磷完成测定空气中氧气含量的实验,理由是______.

某校化学兴趣小组同学做镁带在空气中燃烧的实验时,发现白色生成物中混有少量淡黄色固体.针对这一现象,他们开展了如下实验探究.请仔细阅读并完成下列探究报告.
探究目的:探究镁在空气中燃烧产生的淡黄色固体是镁与空气中什么物质反应产生的?
分析猜想:分析空气中各种成分,寻找猜想依据.
干燥空气中各组分气体的体积分数大约是:氮气 %,氧气 %,稀有气体0.94%,二氧化碳0.03%,其他气体和杂质0.03%
已学知识:氧气与镁反应生成的氧化镁是白色固体.
查阅资料:稀有气体化学性质稳定,一般不与其它物质反应.
猜想1:可能是镁与氮气反应生成淡黄色固体.
猜想2:可能是镁与二氧化碳反应生成淡黄色固体.
猜想3:可能是镁与 生成淡黄色固体.
实验一:镁带与氮气的反应
(一)获取氮气
(1)把空气除尘净化,除去二氧化碳和水蒸气,液化后再蒸发,先蒸发出来的气体就是氮气.这种方法属于 (选填“物理”或“化学”)方法.但在实验室里空气不易被液化.
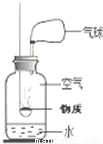
(2)如图是获取氮气的方法及装置.用燃烧法除去空气(已除去二氧化碳、水蒸气和杂质)中的氧气从而得到较纯净的氮气,燃烧匙内选用的物质最好是 .
A.木炭 B.蜡烛C.红磷 D.铁丝
(二)燃烧镁带,观察现象
将镁带打磨光亮,点燃,伸入盛氮气的集气瓶中,瓶内壁附着一层淡黄色的固体.
(三)实验结论:镁与氮气在点燃的条件下发生化合反应生成淡黄色的氮化镁(Mg3N2).
该反应的化学方程式是 .
实验二:将燃着的镁带伸入盛二氧化碳的集气瓶中,镁带剧烈燃烧,瓶内出现白色固体和黑色固体.生成的黑色固体物质的化学式是 .
实验结论:镁在空气中燃烧产生的淡黄色固体是镁与空气中的 反应产生的.
反思与评价:通过上述的实验及所学知识,你对燃烧的条件有什么新的认识? .
拓展与迁移: (填“能”或“不能”)用镁条代替红磷完成测定空气中氧气含量的实验,理由是 .
 查看习题详情和答案>>
查看习题详情和答案>>
探究目的:探究镁在空气中燃烧产生的淡黄色固体是镁与空气中什么物质反应产生的?
分析猜想:分析空气中各种成分,寻找猜想依据.
干燥空气中各组分气体的体积分数大约是:氮气 %,氧气 %,稀有气体0.94%,二氧化碳0.03%,其他气体和杂质0.03%
已学知识:氧气与镁反应生成的氧化镁是白色固体.
查阅资料:稀有气体化学性质稳定,一般不与其它物质反应.
猜想1:可能是镁与氮气反应生成淡黄色固体.
猜想2:可能是镁与二氧化碳反应生成淡黄色固体.
猜想3:可能是镁与 生成淡黄色固体.
实验一:镁带与氮气的反应
(一)获取氮气
(1)把空气除尘净化,除去二氧化碳和水蒸气,液化后再蒸发,先蒸发出来的气体就是氮气.这种方法属于 (选填“物理”或“化学”)方法.但在实验室里空气不易被液化.
(2)如图是获取氮气的方法及装置.用燃烧法除去空气(已除去二氧化碳、水蒸气和杂质)中的氧气从而得到较纯净的氮气,燃烧匙内选用的物质最好是 .
A.木炭 B.蜡烛C.红磷 D.铁丝
(二)燃烧镁带,观察现象
将镁带打磨光亮,点燃,伸入盛氮气的集气瓶中,瓶内壁附着一层淡黄色的固体.
(三)实验结论:镁与氮气在点燃的条件下发生化合反应生成淡黄色的氮化镁(Mg3N2).
该反应的化学方程式是 .
实验二:将燃着的镁带伸入盛二氧化碳的集气瓶中,镁带剧烈燃烧,瓶内出现白色固体和黑色固体.生成的黑色固体物质的化学式是 .
实验结论:镁在空气中燃烧产生的淡黄色固体是镁与空气中的 反应产生的.
反思与评价:通过上述的实验及所学知识,你对燃烧的条件有什么新的认识? .
拓展与迁移: (填“能”或“不能”)用镁条代替红磷完成测定空气中氧气含量的实验,理由是 .
 查看习题详情和答案>>
查看习题详情和答案>>
一化学兴趣小组对某生铁样品中铁的质量分数进行探究.请按要求完成下列探究报告.
[实验目的]测定某生铁样品中单质铁的质量分数.
[资料支撑]生铁中除铁外,还含有碳、硅、锰、磷和硫等元素.碳在生铁中以两种形态存在,一种是游离碳(石墨),另一种是化合碳(如Fe3C等);硅、锰、磷、硫存在形式较为复杂;这些物质通常都不与稀硫酸发生化学反应.
[实验方案]生铁样品与过量的稀硫酸反应,测定反应前后可称量物质的质量差.
[实验过程](1)取一只烧杯,称得其质量为70.4g,加入一定量生铁样品碎屑,称得烧杯和样品的总质量为102.4g;
(1)向盛有生铁样品的烧杯中加入稀硫酸,边加边搅拌,直到烧杯中不再产生气泡,再加入少量稀硫酸以确保过量,测得共用去稀硫酸247.3g;
(3)静置,称量.称得烧杯和剩余物质的总质量为348.7g.
[数据处理]计算该生铁样品中单质铁的质量分数:
[交流讨论]实验称量时称量物应放在托盘天平的
查看习题详情和答案>>
[实验目的]测定某生铁样品中单质铁的质量分数.
[资料支撑]生铁中除铁外,还含有碳、硅、锰、磷和硫等元素.碳在生铁中以两种形态存在,一种是游离碳(石墨),另一种是化合碳(如Fe3C等);硅、锰、磷、硫存在形式较为复杂;这些物质通常都不与稀硫酸发生化学反应.
[实验方案]生铁样品与过量的稀硫酸反应,测定反应前后可称量物质的质量差.
[实验过程](1)取一只烧杯,称得其质量为70.4g,加入一定量生铁样品碎屑,称得烧杯和样品的总质量为102.4g;
(1)向盛有生铁样品的烧杯中加入稀硫酸,边加边搅拌,直到烧杯中不再产生气泡,再加入少量稀硫酸以确保过量,测得共用去稀硫酸247.3g;
(3)静置,称量.称得烧杯和剩余物质的总质量为348.7g.
[数据处理]计算该生铁样品中单质铁的质量分数:
87.5%
87.5%
.[交流讨论]实验称量时称量物应放在托盘天平的
左
左
盘(选填“左”或“右”)一化学兴趣小组对某生铁样品中铁的质量分数进行探究.请按要求完成下列探究报告.
[实验目的]测定某生铁样品中单质铁的质量分数.
[资料支撑]生铁中除铁外,还含有碳、硅、锰、磷和硫等元素.碳在生铁中以两种形态存在,一种是游离碳(石墨),另一种是化合碳(如Fe3C等);硅、锰、磷、硫存在形式较为复杂;这些物质通常都不与稀硫酸发生化学反应.
[实验方案]生铁样品与过量的稀硫酸反应,测定反应前后可称量物质的质量差.
[实验过程](1)取一只烧杯,称得其质量为70.4g,加入一定量生铁样品碎屑,称得烧杯和样品的总质量为102.4g;
(2)向盛有生铁样品的烧杯中加入稀硫酸,边加边搅拌,直到烧杯中不再产生气泡,再加入少量稀硫酸以确保过量,测得共用去稀硫酸247.3g;
(3)静置,称量.称得烧杯和剩余物质的总质量为348.7g.
[数据处理]计算该生铁样品中单质铁的质量分数: .
[交流讨论]实验称量时称量物应放在托盘天平的 盘(选填“左”或“右”)