题目内容
某校化学兴趣小组同学做镁带在空气中燃烧的实验时,发现白色生成物中混有少量淡黄色固体.针对这一现象,他们开展了如下实验探究.请仔细阅读并完成下列探究报告.探究目的:探究镁在空气中燃烧产生的淡黄色固体是镁与空气中什么物质反应产生的?
分析猜想:分析空气中各种成分,寻找猜想依据.
干燥空气中各组分气体的体积分数大约是:氮气 %,氧气 %,稀有气体0.94%,二氧化碳0.03%,其他气体和杂质0.03%
已学知识:氧气与镁反应生成的氧化镁是白色固体.
查阅资料:稀有气体化学性质稳定,一般不与其它物质反应.
猜想1:可能是镁与氮气反应生成淡黄色固体.
猜想2:可能是镁与二氧化碳反应生成淡黄色固体.
猜想3:可能是镁与 生成淡黄色固体.
实验一:镁带与氮气的反应
(一)获取氮气
(1)把空气除尘净化,除去二氧化碳和水蒸气,液化后再蒸发,先蒸发出来的气体就是氮气.这种方法属于 (选填“物理”或“化学”)方法.但在实验室里空气不易被液化.
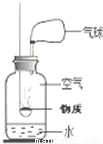
(2)如图是获取氮气的方法及装置.用燃烧法除去空气(已除去二氧化碳、水蒸气和杂质)中的氧气从而得到较纯净的氮气,燃烧匙内选用的物质最好是 .
A.木炭 B.蜡烛C.红磷 D.铁丝
(二)燃烧镁带,观察现象
将镁带打磨光亮,点燃,伸入盛氮气的集气瓶中,瓶内壁附着一层淡黄色的固体.
(三)实验结论:镁与氮气在点燃的条件下发生化合反应生成淡黄色的氮化镁(Mg3N2).
该反应的化学方程式是 .
实验二:将燃着的镁带伸入盛二氧化碳的集气瓶中,镁带剧烈燃烧,瓶内出现白色固体和黑色固体.生成的黑色固体物质的化学式是 .
实验结论:镁在空气中燃烧产生的淡黄色固体是镁与空气中的 反应产生的.
反思与评价:通过上述的实验及所学知识,你对燃烧的条件有什么新的认识? .
拓展与迁移: (填“能”或“不能”)用镁条代替红磷完成测定空气中氧气含量的实验,理由是 .
【答案】分析:分析猜想:根据空气中各气体的体积分数进行解答;
猜想3:根据空气中的成分来作出猜想;
实验一:(一)(1)根据题意,把空气液化,然后蒸发,先蒸发出来的气体就是氮气,根据是否有新物质生成,确定利用的是物理方法还是化学方法.
(2)将空气中氧气除去得到较纯净的氮气,所选除氧剂要具备以下特征:①本身能够在空气中燃烧;②本身的状态为非气体;③生成的物质为非气态.可以据此结合题给的选项进行解答;
(三)根据题给的信息可以写出该镁和氮气反应的化学方程式;
实验二:CO2与镁发生了置换反应,根据质量守恒定律,可以确定生成的黑色固体的成分.
实验结论:综合上述实验可以知道,反应中产生的黄色固体为镁条和氮气反应生成的;
反思与评价:根据上述实验可以知道,物质的燃烧不一定有氧气参与,可以据此解答该题;
拓展与迁移:镁条不但能够和氧气反应,而且能够和氮气反应,可以据此解答该题.
解答:解:分析猜想:根据空气中各气体的体积分数可以知道,氮气占空气总体积的78%,氧气占空气总体积的21%;
猜想3:根据空气中的成分可以知道,在空气中含有水蒸气,所以该淡黄色固体可能是镁和水蒸气反应生成的;
实验一:(一)(1)把空气液化,然后蒸发,先蒸发出来的气体就是氮气,分离过程中没有新物质生成,属于物理方法;
(2)A、木炭在空气中能够燃烧生成二氧化碳气体,虽除去氧气,而增加了新的气体二氧化碳,尽管水能吸收二氧化硫,由于二氧化碳的溶解度较小,所以不能被全部吸收,所以不能得到较纯净的氮气,故A错误;
B、蜡烛燃烧产生了二氧化碳和水,所以不能得到纯净的氮气,故B错误;
C、红磷燃烧生成了白色固体,所以能够将氧气除去而得到较纯净的氮气,故C正确;
D、铁丝只能在纯氧中燃烧而不能在空气中燃烧,所以不能除去氧气,故D错误;
故选C.
(三)镁与氮气在点燃的条件下发生化合反应生成淡黄色的氮化镁(Mg3N2),该反应的化学方程式为:3Mg+N2 Mg3N2;
Mg3N2;
实验二:将燃着的镁带伸入盛CO2的集气瓶中,镁带剧烈燃烧,瓶内出现白色固体和黑色固体.CO2与镁发生了置换反应,生成物为氧化镁和碳,黑色固体物质是碳..
实验结论:综合上述实验可以知道,反应中产生的黄色固体为镁条和氮气反应生成的;
反思与评价:根据上述实验可以知道,物质的燃烧不一定有氧气参与;
拓展与迁移:镁条不但能够和氧气反应,而且能够和氮气反应,所以若用镁条来代替红磷完成测定空气中氧气含量的实验,则会由于消耗了氮气而得出错误的结论.
故答案为:分析猜想:78;21;
猜想3:水蒸气;
实验一:(一)(1)物理;
(2)C.
(三)3Mg+N2 Mg3N2;
Mg3N2;
实验二:C.
实验结论:氮气;
反思与评价:物质的燃烧不一定有氧气参与;
拓展与迁移:不能;镁条不但能够和氧气反应,而且能够和氮气反应,所以若用镁条来代替红磷完成测定空气中氧气含量的实验,则会由于消耗了氮气而得出错误的结论.
点评:本题难度较大,考查同学们新信息获取、处理及灵活运用所学化学知识进行分析问题、解决问题的能力.
猜想3:根据空气中的成分来作出猜想;
实验一:(一)(1)根据题意,把空气液化,然后蒸发,先蒸发出来的气体就是氮气,根据是否有新物质生成,确定利用的是物理方法还是化学方法.
(2)将空气中氧气除去得到较纯净的氮气,所选除氧剂要具备以下特征:①本身能够在空气中燃烧;②本身的状态为非气体;③生成的物质为非气态.可以据此结合题给的选项进行解答;
(三)根据题给的信息可以写出该镁和氮气反应的化学方程式;
实验二:CO2与镁发生了置换反应,根据质量守恒定律,可以确定生成的黑色固体的成分.
实验结论:综合上述实验可以知道,反应中产生的黄色固体为镁条和氮气反应生成的;
反思与评价:根据上述实验可以知道,物质的燃烧不一定有氧气参与,可以据此解答该题;
拓展与迁移:镁条不但能够和氧气反应,而且能够和氮气反应,可以据此解答该题.
解答:解:分析猜想:根据空气中各气体的体积分数可以知道,氮气占空气总体积的78%,氧气占空气总体积的21%;
猜想3:根据空气中的成分可以知道,在空气中含有水蒸气,所以该淡黄色固体可能是镁和水蒸气反应生成的;
实验一:(一)(1)把空气液化,然后蒸发,先蒸发出来的气体就是氮气,分离过程中没有新物质生成,属于物理方法;
(2)A、木炭在空气中能够燃烧生成二氧化碳气体,虽除去氧气,而增加了新的气体二氧化碳,尽管水能吸收二氧化硫,由于二氧化碳的溶解度较小,所以不能被全部吸收,所以不能得到较纯净的氮气,故A错误;
B、蜡烛燃烧产生了二氧化碳和水,所以不能得到纯净的氮气,故B错误;
C、红磷燃烧生成了白色固体,所以能够将氧气除去而得到较纯净的氮气,故C正确;
D、铁丝只能在纯氧中燃烧而不能在空气中燃烧,所以不能除去氧气,故D错误;
故选C.
(三)镁与氮气在点燃的条件下发生化合反应生成淡黄色的氮化镁(Mg3N2),该反应的化学方程式为:3Mg+N2
 Mg3N2;
Mg3N2;实验二:将燃着的镁带伸入盛CO2的集气瓶中,镁带剧烈燃烧,瓶内出现白色固体和黑色固体.CO2与镁发生了置换反应,生成物为氧化镁和碳,黑色固体物质是碳..
实验结论:综合上述实验可以知道,反应中产生的黄色固体为镁条和氮气反应生成的;
反思与评价:根据上述实验可以知道,物质的燃烧不一定有氧气参与;
拓展与迁移:镁条不但能够和氧气反应,而且能够和氮气反应,所以若用镁条来代替红磷完成测定空气中氧气含量的实验,则会由于消耗了氮气而得出错误的结论.
故答案为:分析猜想:78;21;
猜想3:水蒸气;
实验一:(一)(1)物理;
(2)C.
(三)3Mg+N2
 Mg3N2;
Mg3N2;实验二:C.
实验结论:氮气;
反思与评价:物质的燃烧不一定有氧气参与;
拓展与迁移:不能;镁条不但能够和氧气反应,而且能够和氮气反应,所以若用镁条来代替红磷完成测定空气中氧气含量的实验,则会由于消耗了氮气而得出错误的结论.
点评:本题难度较大,考查同学们新信息获取、处理及灵活运用所学化学知识进行分析问题、解决问题的能力.

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目
 (2012?荔湾区一模)某校化学兴趣小组同学发现,长期使用的热水壶底部有一层水垢,水垢的主要成分是碳酸钙和氢氧化镁.他们为了测定水垢中碳酸钙的含量,将足量质量分数为10%的盐酸加入到10g水垢中,产生CO2气体的情况如图所示.
(2012?荔湾区一模)某校化学兴趣小组同学发现,长期使用的热水壶底部有一层水垢,水垢的主要成分是碳酸钙和氢氧化镁.他们为了测定水垢中碳酸钙的含量,将足量质量分数为10%的盐酸加入到10g水垢中,产生CO2气体的情况如图所示.  某校化学兴趣小组同学在实验测定一块大理石中碳酸钙的质量分数.他们称取的大理石质量为12.5g,将其放入足量的稀盐酸中,产生气体的情况如图所示.计算该大理石中碳酸钙的质量分数?(大理石中除碳酸钙之外的其它杂质不与盐酸发生反应)
某校化学兴趣小组同学在实验测定一块大理石中碳酸钙的质量分数.他们称取的大理石质量为12.5g,将其放入足量的稀盐酸中,产生气体的情况如图所示.计算该大理石中碳酸钙的质量分数?(大理石中除碳酸钙之外的其它杂质不与盐酸发生反应) 某校化学兴趣小组同学发现,长期使用的热水壶底部有一层水垢,水垢的主要成分是碳酸钙和氢氧化镁.他们为了测定水垢中碳酸钙的含量,将足量质量分数为10%的盐酸加入到12.5g水垢后,产生CO2气体的情况如图所示.
某校化学兴趣小组同学发现,长期使用的热水壶底部有一层水垢,水垢的主要成分是碳酸钙和氢氧化镁.他们为了测定水垢中碳酸钙的含量,将足量质量分数为10%的盐酸加入到12.5g水垢后,产生CO2气体的情况如图所示.