摘要:5. 已知可逆反应: 请回答下列问题: (1)在某温度下.反应物的起始浓度分别为:c(M)= 1 mol,L-1, c(N)=2.4 mol·L-1; 达到平衡后.M的转化率为60%.此时N的转化率为 , (2)若反应温度升高.M的转化率 (填“增大 “减小 或“不变 ,) (3)若反应温度不变.反应物的起始浓度分别为:c(M)= 1 mol,L-1, c(N)=2.4 mol·L-1;达到平衡后.c(P)=2 mol·L-1,a= ; (4)若反应温度不变.反应物的起始浓度为:c(M)= 1 mol,L-1.达到平衡后.M的转化率为 .
网址:http://m.1010jiajiao.com/timu3_id_48061[举报]
已知可逆反应X(g)+Y(g)?Z(g)(未配平).温度为T0时,在容积固定的容器中发生反应各物质的浓度随时间变化的关系如图a所示.其他条件相同,温度分别为T1、T2时发生反应,Z的浓度随时间变化的关系如图b所示.下列叙述正确的是( )
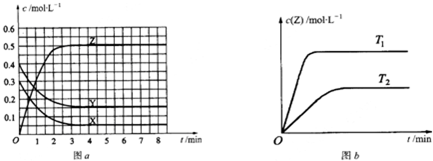

| A、发生反应时,各物质的反应速率大小关系为:v(X)=v(Y)=2v(Z) | B、图a中反应达到平衡时,Y的转化率为37.5% | C、增大压强,平衡向正反应方向移动 | D、该反应正反应的反应热△H>0 |
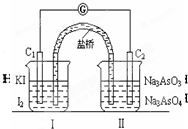 已知可逆反应AsO43-+2I-+2H+?AsO33-+I2+H2O,设计如图装置,进行下述操作:
已知可逆反应AsO43-+2I-+2H+?AsO33-+I2+H2O,设计如图装置,进行下述操作:①向(Ⅱ)烧杯中逐滴加入浓盐酸,发现微安表(G)指针偏转;
②若改往(Ⅱ)烧杯中滴加40%NaOH溶液,发现微安表指针与 ①的偏转方向相反.下列有关说法不正确的是( )
查看习题详情和答案>>
已知可逆反应 2SO2 (g)+O2(g)?2SO3(g);△H<0.现有甲、乙两个容器相同的恒容容器.在 500℃和有催化剂存在下,向甲中加入 2mol SO2 和1mol O2,向乙中加入2mol SO3,并同时开始发生反应.当两容器中反应分别达到平衡后,维持条件不变,则( )
查看习题详情和答案>>
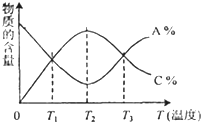 已知可逆反应aA+bB?cC中,物质的含量A%和C%随时间进行、温度的变化曲线如图所示,下列说法正确的是( )
已知可逆反应aA+bB?cC中,物质的含量A%和C%随时间进行、温度的变化曲线如图所示,下列说法正确的是( )| A、该反应在T1温度时已达到过化学平衡 | B、该反应在T3温度时才达到过化学平衡 | C、增大压强平衡一定会向正反应方向移动 | D、该可逆反应的正反应是放热反应 |
 2NH3(g)△H=-92kJ?mol-1下列关于此反应的说法中错误的是( )
2NH3(g)△H=-92kJ?mol-1下列关于此反应的说法中错误的是( )