题目内容
已知可逆反应 2SO2 (g)+O2(g)?2SO3(g);△H<0.现有甲、乙两个容器相同的恒容容器.在 500℃和有催化剂存在下,向甲中加入 2mol SO2 和1mol O2,向乙中加入2mol SO3,并同时开始发生反应.当两容器中反应分别达到平衡后,维持条件不变,则( )
分析:根据在相同的温度和体积下,对于前后气体体积变化的可逆反应,按化学计量转化到一边,对应成分的物质的量相同,
则两平衡等效且等同,衡混合物中各组成成分的含量、浓度、物质的量不变来分析.
A、根据甲容器终反应的SO2和乙容器中反应的SO3的不一定相等来分析;
B、2mol SO2 和1mol O2完全反应生成SO3放出的热量等于2molSO3完全反应生成2mol SO2 和1mol O2所吸收的热量,但甲容器终反应的SO2和乙容器中反应的SO3的不一定相等;
C、当两容器中反应分别达到平衡后,两平衡等效且等同,衡混合物中各组成成分的物质的量对应相等,则甲、乙两容器中混合气体平均摩尔质量一定相等;
D、两容器中反应的速率无法比较大小;
则两平衡等效且等同,衡混合物中各组成成分的含量、浓度、物质的量不变来分析.
A、根据甲容器终反应的SO2和乙容器中反应的SO3的不一定相等来分析;
B、2mol SO2 和1mol O2完全反应生成SO3放出的热量等于2molSO3完全反应生成2mol SO2 和1mol O2所吸收的热量,但甲容器终反应的SO2和乙容器中反应的SO3的不一定相等;
C、当两容器中反应分别达到平衡后,两平衡等效且等同,衡混合物中各组成成分的物质的量对应相等,则甲、乙两容器中混合气体平均摩尔质量一定相等;
D、两容器中反应的速率无法比较大小;
解答:解:A、据题意,当两容器中反应分别达到平衡后,两平衡等效且等同,衡混合物中各组成成分的物质的量对应相等,甲容器终反应的SO2和乙容器中反应的SO3的不一定相等,所以甲中SO2的转化率不一定等于乙中SO3的分解率,故A错误;
B、2mol SO2 和1mol O2完全反应生成SO3放出的热量等于2molSO3完全反应生成2mol SO2 和1mol O2所吸收的热量,但甲容器终反应的SO2和乙容器中反应的SO3的不一定相等,所以甲中反应放出的热量与乙中反应吸收的热量数值上不一定相等,故B错误;
C、当两容器中反应分别达到平衡后,两平衡等效且等同,混合物中各组成成分的物质的量对应相等,则甲、乙两容器中混合气体平均摩尔质量一定相等,即混合气体平均相对分子质量一定相等,故C正确;
D、两容器中反应的速率无法比较大小,所以无法判断到达平衡的时间,故D错误;
故选:D.
B、2mol SO2 和1mol O2完全反应生成SO3放出的热量等于2molSO3完全反应生成2mol SO2 和1mol O2所吸收的热量,但甲容器终反应的SO2和乙容器中反应的SO3的不一定相等,所以甲中反应放出的热量与乙中反应吸收的热量数值上不一定相等,故B错误;
C、当两容器中反应分别达到平衡后,两平衡等效且等同,混合物中各组成成分的物质的量对应相等,则甲、乙两容器中混合气体平均摩尔质量一定相等,即混合气体平均相对分子质量一定相等,故C正确;
D、两容器中反应的速率无法比较大小,所以无法判断到达平衡的时间,故D错误;
故选:D.
点评:本题结合等效平衡考查了反应中物质的转化率、反应中热效应等知识,难度中等,注意分析.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 4C(g)
△H>0达到平衡时,c(A)=2mol/L,c(B)=7mol/L,c(c)
4C(g)
△H>0达到平衡时,c(A)=2mol/L,c(B)=7mol/L,c(c)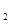 (g)
(g) 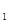 与K
与K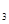 的平衡常数K=19。在该温度下的体积
的平衡常数K=19。在该温度下的体积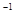 c0(O
c0(O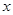 kJ·mol
kJ·mol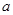 +b>
+b>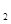 (g)的平衡常数为K1;H
(g)的平衡常数为K1;H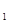 与K
与K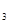 的平衡常数K=19。在该温度下的体积
的平衡常数K=19。在该温度下的体积 容包括:化学平衡、电离平衡、水解平衡和
容包括:化学平衡、电离平衡、水解平衡和 4C(g) △H>0达到平衡时,c(A)=2mol/L,c(B)=7mol/L,c(c)
4C(g) △H>0达到平衡时,c(A)=2mol/L,c(B)=7mol/L,c(c)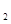 (g)
(g) 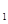 与K
与K 的平衡常数K=19。在该温度下的体积
的平衡常数K=19。在该温度下的体积 c0(O
c0(O
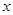 kJ·mol
kJ·mol +b>
+b>