摘要:6.答案:(1)验证Na与CuSO4溶液反应是否有Cu生成 2可溶于盐酸而Cu不溶 (3)镊子 烧杯 CuSO4溶液 盐酸或稀硫酸 CuO Na与水反应放出的热使生成的Cu(OH)2部分分解 解析:(1)该学生怀疑Na也与CuSO4发生了置换反应而生成了Cu.因而他实验探究的目的是验证Na与CuSO4溶液反应是否有Cu生成.(2)当Na不与CuSO4发生置换反应时.沉淀只含有Cu(OH)2,当Na与CuSO4发生置换反应时.沉淀中既有Cu(OH)2.又有Cu.根据Cu(OH)2可溶于盐酸而Cu不溶.只要是加入过量的盐酸观察沉淀是否全部溶解即可.(3)这个实验需要首先完成Na和CuSO4溶液的反应.然后再进行沉淀与盐酸的反应.完成Na与CuSO4溶液的反应.需要的试剂是Na和CuSO4溶液.还需要的用品是镊子.烧杯.完成沉淀与盐酸的反应.需要的试剂是稀盐酸或稀硫酸.不再需要别的用品.Na与水反应放出大量热量.而Cu(OH)2受热易分解.因此.实验中意外发现的黑色沉淀应该是CuO.
网址:http://m.1010jiajiao.com/timu3_id_45023[举报]
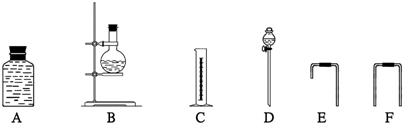
关于下列各实验装置的叙述中,不正确的是(???? )
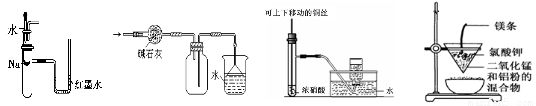
①???????????????????? ②?????????????? ③???????????????????? ④
A.装置①可用于验证Na与H2O反应是否放热
B.装置②可用于干燥、收集NH3,并吸收多余的NH3
C.装置③可用于制备并收集少量NO2
D.装置④可制得金属锰
查看习题详情和答案>>
关于下列各实验装置的叙述中,不正确的是
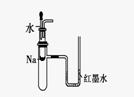
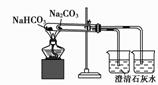
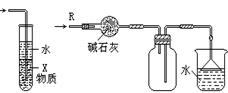
① ② ③ ④
A.装置①可用于验证Na与H2O反应是否放热
B.装置②可用于比较Na2CO3与NaHCO3的稳定性
C.装置③中X若为CCl4,可用于吸收NH3或HCl,并防止倒吸
D.装置④可用于干燥、收集NH3,并吸收多余的NH3
查看习题详情和答案>>关于下列各实验装置的叙述中,不正确的是
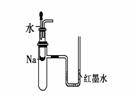
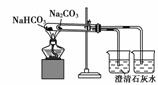
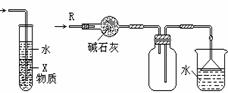
① ② ③ ④
A.装置①可用于验证Na与H2O反应是否放热
B.装置②可用于比较Na2CO3与NaHCO3的稳定性
C.装置③中X若为CCl4,可用于吸收NH3或HCl,并防止倒吸
D.装置④可用于干燥、收集NH3,并吸收多余的NH3
查看习题详情和答案>>
能源是人类社会发展的基础,地球上最基本的能源是太阳能,生物质能来源于植物及其加工产品所贮存的能量,化石燃料蕴藏的能量也来自远古时期生物体所吸收利用的太阳能.
(1)在当代人们的生活中,你所知道的利用太阳能辐射加热物体的方式有
(2)在生物质能的利用过程中,可以制得重要的有机物乙醇.某校化学课外兴趣小组的学生为了验证乙醇的分子结构,设计如下实验程序:乙醇的组成元素的确定、分子式的确定、分子结构的确定.
(Ⅰ)他们决定用分析乙醇燃烧的产物来确定乙醇中含有C、H两种元素,简要说明他们的实验操作方法和现象:
①证明含有氢元素的实验操作方法和现象是
②证明含有碳元素的实验操作方法和现象是
(Ⅱ)用分析燃烧产物来证实乙醇中还含有氧元素时,需要取得一些实验数据,这些数据应该是
实验中他们可能会用到下列装置,请你将必需的相关装置的序号按从左到右排出合理的顺序(→表示气体的流向):
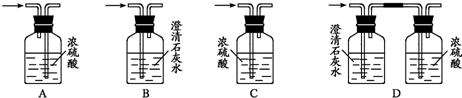
(Ⅲ)为确定乙醇的分子式,除(Ⅱ)中需要取得的数据外,你认为还是否需要测定乙醇的相对分子质量呢?
(Ⅳ)为确定乙醇的分子结构,他们先测定一定量无水乙醇和金属钠反应生成氢气的体积,选用了如下图所示的仪器装置(有的仪器配有双孔橡皮塞).则
①这些仪器装置的合理的连接顺序是
②由实验证明乙醇的分子结构是CH3CH2OH而不是CH3OCH3的理由是
(3)开发新能源以缓解石油等的短缺引起的能源危机是一个重要课题.据报道,某地近年建设了一个年生产工业酒精500万吨的工厂,目的是为了将工业酒精与汽油混合作为汽车燃料而减少汽油的消耗量.已知生产酒精的方法有如下三种(用化学方程式表示):
方法一:CH2=CH2+H2O
CH3CH2OH
方法二:CH3-CH2Br+H2O
CH3CH2OH+HBr
方法三:(C6H10O5)n(淀粉)+n H2O
n C6H12O6(葡萄糖)
C6H12O6(葡萄糖)
2C2H5OH+2CO2↑
综合地看,你认为这三种方法中,较好的是
A.方法一 B.方法二 C.方法三
你认为该工厂生产工业酒精用的是
查看习题详情和答案>>
(1)在当代人们的生活中,你所知道的利用太阳能辐射加热物体的方式有
地膜、大棚、温室、太阳能热水器等
地膜、大棚、温室、太阳能热水器等
(任举三例).(2)在生物质能的利用过程中,可以制得重要的有机物乙醇.某校化学课外兴趣小组的学生为了验证乙醇的分子结构,设计如下实验程序:乙醇的组成元素的确定、分子式的确定、分子结构的确定.
(Ⅰ)他们决定用分析乙醇燃烧的产物来确定乙醇中含有C、H两种元素,简要说明他们的实验操作方法和现象:
①证明含有氢元素的实验操作方法和现象是
用一干燥的小烧杯倒置在乙醇燃烧火焰上方,烧杯内壁有水珠生成
用一干燥的小烧杯倒置在乙醇燃烧火焰上方,烧杯内壁有水珠生成
.②证明含有碳元素的实验操作方法和现象是
将内壁用澄清石灰水润湿的小烧杯倒置在火焰上方,石灰水变浑浊
将内壁用澄清石灰水润湿的小烧杯倒置在火焰上方,石灰水变浑浊
.(Ⅱ)用分析燃烧产物来证实乙醇中还含有氧元素时,需要取得一些实验数据,这些数据应该是
乙醇、二氧化碳及水三种物质的质量
乙醇、二氧化碳及水三种物质的质量
.实验中他们可能会用到下列装置,请你将必需的相关装置的序号按从左到右排出合理的顺序(→表示气体的流向):
CD或CB
CD或CB
.
(Ⅲ)为确定乙醇的分子式,除(Ⅱ)中需要取得的数据外,你认为还是否需要测定乙醇的相对分子质量呢?
不需要
不需要
.(Ⅳ)为确定乙醇的分子结构,他们先测定一定量无水乙醇和金属钠反应生成氢气的体积,选用了如下图所示的仪器装置(有的仪器配有双孔橡皮塞).则

①这些仪器装置的合理的连接顺序是
D
D
接B
B
接E
E
接A
A
接F
F
接C
C
(填代表各部分仪器装置的大写字母).②由实验证明乙醇的分子结构是CH3CH2OH而不是CH3OCH3的理由是
根据Na与乙醇反应生成的H2的量判断出只有一个H与其他H原子处于不同的特殊位置.从而进一步确定其结构为C2H5OH而非CH3-O-CH3
根据Na与乙醇反应生成的H2的量判断出只有一个H与其他H原子处于不同的特殊位置.从而进一步确定其结构为C2H5OH而非CH3-O-CH3
.(3)开发新能源以缓解石油等的短缺引起的能源危机是一个重要课题.据报道,某地近年建设了一个年生产工业酒精500万吨的工厂,目的是为了将工业酒精与汽油混合作为汽车燃料而减少汽油的消耗量.已知生产酒精的方法有如下三种(用化学方程式表示):
方法一:CH2=CH2+H2O
| ||
| △ |
方法二:CH3-CH2Br+H2O
| ||
| △ |
方法三:(C6H10O5)n(淀粉)+n H2O
| 淀粉酶 |
C6H12O6(葡萄糖)
| 酒化酶 |
综合地看,你认为这三种方法中,较好的是
A
A
(填字母),理由是反应原理符合绿色化学的原则,反应物的原子全部转化为期望的最终产物
反应原理符合绿色化学的原则,反应物的原子全部转化为期望的最终产物
.A.方法一 B.方法二 C.方法三
你认为该工厂生产工业酒精用的是
方法三
方法三
(填“方法一”、“方法二”或“方法三”)而不是另外的两种方法的原因是乙烯、溴乙烷都是来自于以石油为原料制得的物质,石油是不可再生的,利用它们制成酒精还不如直接利用石油
乙烯、溴乙烷都是来自于以石油为原料制得的物质,石油是不可再生的,利用它们制成酒精还不如直接利用石油
_. 有A、B、C、D、E五种短周期元素,它们的原子序数由A到E依次增大,已知A和B原子有相同的电子层数,且A的L层电子数是K层电子数的两倍,C在空气中燃烧时呈现黄色火焰,C的单质在高温下与B的单质充分反应,可以得到与E单质颜色相同的淡黄色固态化合物.D为原子核内有12个中子的二价金属,当2.4克D与盐酸反应时,在标准状况下放出气体2.24L.
有A、B、C、D、E五种短周期元素,它们的原子序数由A到E依次增大,已知A和B原子有相同的电子层数,且A的L层电子数是K层电子数的两倍,C在空气中燃烧时呈现黄色火焰,C的单质在高温下与B的单质充分反应,可以得到与E单质颜色相同的淡黄色固态化合物.D为原子核内有12个中子的二价金属,当2.4克D与盐酸反应时,在标准状况下放出气体2.24L.试根据以上叙述回答:
(1)写出元素名称:A
碳
碳
E硫
硫
,写出D的原子符号2412Mg
2412Mg
(标出质子数和质量数)(2)画出C的原子结构示意图


(3)写出AB2与C2B2反应的化学方程式
2CO2+2Na2O2=2Na2CO3+O2
2CO2+2Na2O2=2Na2CO3+O2
.(4)比较B和E的气态氢化物的稳定性(用化学式回答):
H2O>H2S
H2O>H2S
.(5)判断C元素和D元素的金属性强弱,简要地说明你的一个判断依据:
金属性 Na>Mg,钠跟冷水能反应,镁和冷水不反应 或其他合理答案
金属性 Na>Mg,钠跟冷水能反应,镁和冷水不反应 或其他合理答案
.