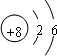题目内容
 有A、B、C、D、E五种短周期元素,它们的原子序数由A到E依次增大,已知A和B原子有相同的电子层数,且A的L层电子数是K层电子数的两倍,C在空气中燃烧时呈现黄色火焰,C的单质在高温下与B的单质充分反应,可以得到与E单质颜色相同的淡黄色固态化合物.D为原子核内有12个中子的二价金属,当2.4克D与盐酸反应时,在标准状况下放出气体2.24L.
有A、B、C、D、E五种短周期元素,它们的原子序数由A到E依次增大,已知A和B原子有相同的电子层数,且A的L层电子数是K层电子数的两倍,C在空气中燃烧时呈现黄色火焰,C的单质在高温下与B的单质充分反应,可以得到与E单质颜色相同的淡黄色固态化合物.D为原子核内有12个中子的二价金属,当2.4克D与盐酸反应时,在标准状况下放出气体2.24L.试根据以上叙述回答:
(1)写出元素名称:A
碳
碳
E硫
硫
,写出D的原子符号2412Mg
2412Mg
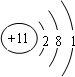
(标出质子数和质量数)(2)画出C的原子结构示意图
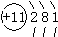
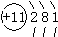
(3)写出AB2与C2B2反应的化学方程式
2CO2+2Na2O2=2Na2CO3+O2
2CO2+2Na2O2=2Na2CO3+O2
.(4)比较B和E的气态氢化物的稳定性(用化学式回答):
H2O>H2S
H2O>H2S
.(5)判断C元素和D元素的金属性强弱,简要地说明你的一个判断依据:
金属性 Na>Mg,钠跟冷水能反应,镁和冷水不反应 或其他合理答案
金属性 Na>Mg,钠跟冷水能反应,镁和冷水不反应 或其他合理答案
.分析:A的L层电子数是K层电子数的两倍,故A为C.C在空气中燃烧时呈现黄色火焰,故C为钠.钠的化合物淡黄色固态化合物应为过氧化钠,B为氧.E单质为S.2.4克D与盐酸反应时,在标准状况下放出气体2.24L.氢气的物质的量为0.1mol,D为二价金属则D的摩尔质量为24g/mol,D的质子数:24-12=12,故D为Mg.
解答:解:(1)A的L层电子数是K层电子数的两倍,故A为C.C在空气中燃烧时呈现黄色火焰,故C为钠.钠的化合物淡黄色固态化合物应为过氧化钠,B为氧.E单质为S.2.4克D与盐酸反应时,在标准状况下放出气体2.24L.氢气的物质的量为0.1mol,D为二价金属则D的摩尔质量为24g/mol,D的质子数:24-12=12,故D为Mg.
(2)C的原子结构示意图为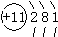
(3)AB2为CO2,C2B2为Na2O2二者反应的方程式为:2CO2+2Na2O2=2Na2CO3+O2
(4)根据元素的非金属性越强,对应气态氢化物的稳定性也就越强,因为 氧>硫,故H2O>H2S.
(5)金属性 Na>Mg,钠跟冷水能反应,镁和冷水不反应.
故答案为:(1)碳 硫 2412Mg
(2)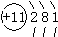 (3)2CO2+2Na2O2=2Na2CO3+O2
(3)2CO2+2Na2O2=2Na2CO3+O2
(4)H2O>H2S
(5)金属性 Na>Mg,钠跟冷水能反应,镁和冷水不反应 或其他合理答案
(2)C的原子结构示意图为
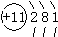
(3)AB2为CO2,C2B2为Na2O2二者反应的方程式为:2CO2+2Na2O2=2Na2CO3+O2
(4)根据元素的非金属性越强,对应气态氢化物的稳定性也就越强,因为 氧>硫,故H2O>H2S.
(5)金属性 Na>Mg,钠跟冷水能反应,镁和冷水不反应.
故答案为:(1)碳 硫 2412Mg
(2)
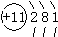 (3)2CO2+2Na2O2=2Na2CO3+O2
(3)2CO2+2Na2O2=2Na2CO3+O2(4)H2O>H2S
(5)金属性 Na>Mg,钠跟冷水能反应,镁和冷水不反应 或其他合理答案
点评:本题考查原子结构,元素及其化合物性质,氧化性还原性比较,难度适中.

练习册系列答案
相关题目