摘要:8].在一定条件下.把amol X.bmol Y混合.发生反应:X2Z(g)达到平衡时Z的体积分数是40﹪.则a︰b的范围是 A 1/5<a/b<2 B 1/4<a/b<3/2 C 1/3<a/b<1 D 1/6<a/b<4/3
网址:http://m.1010jiajiao.com/timu3_id_435248[举报]
已知X2O8n-有强氧化性,X2O8n-在一定条件下可以把Mn2+氧化成MnO4-,若反应后X2O8n-变成XO42-,又知反应中氧化剂与还原剂的离子数之比为5:2,则X2O8 n-中X元素的化合价是( )
| A、+7 | B、+6 | C、+5 | D、+4 |
(2009?潮州月考)R2O
在一定条件下可以把Mn2+氧化成MnO
,若反应后R2O
转变为RO
.又知反应中氧化剂与还原剂的物质的量之比为5:2,则n值为( )
n- 6 |
- 4 |
n- 6 |
n- 3 |
查看习题详情和答案>>
纳米TiO2在涂料、光催化、化妆品等领域有着极其广泛的应用.制备纳米TiO2的方法之一是TiCl4水解生成TiO2?xH2O,经过滤、水洗除去其中的Cl-,再烘干、焙烧除去水分得到粉体TiO2.用氧化还原滴定法测定TiO2的质量分数操作如下:首先在一定条件下,把TiO2溶解并转化为Ti3+,再用NH4Fe(SO4)2标准溶液滴定Ti3+至全部转化成Ti4+.
请回答下列问题:
(1)TiCl4水解生成TiO2?xH2O的化学方程式为
(2)检验TiO2?xH2O中Cl-是否被除净的方法是
(3)配制NH4Fe(SO4)2标准溶液时,加入一定量H2SO4的目的是
(4)该滴定操作所用到的指示剂是
(5)滴定分析时,称取TiO2(摩尔质量为M g?mol-1)试样w g,消耗c mol?L-1NH4Fe(SO4)2标准溶液V mL,则TiO2质量分数为
或
%
或
%.
查看习题详情和答案>>
请回答下列问题:

(1)TiCl4水解生成TiO2?xH2O的化学方程式为
TiCl4+(x+2)H2O=TiO2?xH2O↓+4HCl
TiCl4+(x+2)H2O=TiO2?xH2O↓+4HCl
.(2)检验TiO2?xH2O中Cl-是否被除净的方法是
取少量最后一次水洗液,滴加AgNO3溶液,不产生白色沉淀,说明Cl-已除净
取少量最后一次水洗液,滴加AgNO3溶液,不产生白色沉淀,说明Cl-已除净
.(3)配制NH4Fe(SO4)2标准溶液时,加入一定量H2SO4的目的是
抑制NH4Fe(SO4)2水解
抑制NH4Fe(SO4)2水解
;配制溶液使用的仪器除天平、药匙、玻璃棒、烧杯、量筒外,还需要如图中的ac
ac
(填字母代号).(4)该滴定操作所用到的指示剂是
KSCN溶液
KSCN溶液
,滴定终点的现象是溶液变为红色,且半分钟不褪色
溶液变为红色,且半分钟不褪色
(5)滴定分析时,称取TiO2(摩尔质量为M g?mol-1)试样w g,消耗c mol?L-1NH4Fe(SO4)2标准溶液V mL,则TiO2质量分数为
| cVM |
| 1000W |
| cVM |
| 10W |
| cVM |
| 1000W |
| cVM |
| 10W |
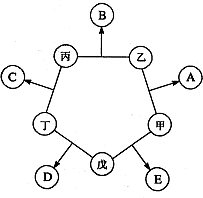 甲、乙、丙、丁、戊五种单质在一定条件下反应生成A、B、C、D、E五种化合物,其转化关系如图所示:又知:①甲、乙、丙、丁均为前三周期元素的单质,常温下均为气态,丙、丁是空气的主要成分,戊是日常生活中一种常见的金属.
甲、乙、丙、丁、戊五种单质在一定条件下反应生成A、B、C、D、E五种化合物,其转化关系如图所示:又知:①甲、乙、丙、丁均为前三周期元素的单质,常温下均为气态,丙、丁是空气的主要成分,戊是日常生活中一种常见的金属.②乙在甲中燃烧发出苍白色火焰,戊在甲中燃烧生成棕黄色烟,E的水溶液呈黄色.
③常温下B、C均为无色气体,D为磁性黑色固体.
(1)D的化学式
(2)把戊加入到E的水溶液中,写出该反应的离子方程式
(3)工业上可由B与丁反应制取C,写出该反应的化学方程式
(4)将氯气和E同时加(通)入强碱性溶液中,可制得一种高效杀菌、净水剂(其中含由+6价戊元素形成的带2个单位负电荷的含氧酸根离子),请写出该反应的离子方程式