摘要:11.(根据2011年富阳中学高考预测卷第17题改编)某化学课外兴趣小组为探究铜跟浓硫酸的反应情况.用下图所示装置先进行了有关实验: (1)B是用来收集实验中产生的气体的装置.但未将导管画全.请在图上把导管补充完整. (2)实验中他们取6.4g 铜片和12mL 18mol·L-1浓硫酸放在圆底烧瓶中共热.直到反应完毕.最后发现烧瓶中还有铜片剩余.该小组学生根据所学的化学知识认为还有一定量的硫酸剩余. ①写出铜跟浓硫酸反应的化学方程式: , ②为什么有一定量的余酸但未能使铜片完全溶解.你认为原因是 , ③下列药品中能够用来证明反应结束后的烧瓶中确有余酸的是: . A.铁粉 B.氯化钡溶液 C.银粉 D.碳酸氢钠溶液 (3)为定量测定余酸的物质的量浓度.甲学生进行了如下设计学生设计的方案是:在反应后的溶液中加蒸馏水稀释至1000mL.取20mL与锥形瓶中.滴入2~3滴甲基橙指示剂.用标准氢氧化钠溶液进行滴定(已知氢氧化铜开始沉淀的pH约为5).通过测出消耗氢氧化钠溶液的体积来求余酸的物质的量浓度.假定反应前后烧瓶中溶液的体积不变.你认为他设计的实验方案能否求得余酸的物质的量浓度 .其理由是 .ww.k@s@5@ 高#考#资#源#网 (4)现已确认.SO2和NOx的排放是造成酸沉降的两大罪魁祸首.汽车排放的尾气中含有未燃烧充分的CH.以及N2.CO2.NO.CO等.有人设计利用反应2NO + 2CO N2 + 2CO2 将有害的污染物转化为可参与大气循环的N2和CO2. 在某温度下用气体传感器测得不同时间的NO和CO浓度如表: 时间/h 0 1 2 3 4 5 c(NO)/mol·L-1 1.00×10-3 4.5×10-4 2.5×10-4 1.5×10-4 1.00×10-4 1.00×10-4 c(CO)/mol·L-1 3.6×10-3 3.05×10-3 2.85×10-3 2.75×10-3 2.70×10-3 2.70×10-3 在上述条件下反应能够自发进行.则反应的 0.前2h内的平均反应速率v(N2)= .在该温度下.反应的平衡常数K= .据此你认为将该反应从理论转化为现实的最重要的研究方向是
网址:http://m.1010jiajiao.com/timu3_id_433051[举报]
某化学课外兴趣小组为探究铜跟浓硫酸的反应情况,用如图1所示装置进行有关实验.
已知:①SO2难溶于饱和亚硫酸氢钠溶液.②SO2能与酸性高锰酸钾溶液发生氧化还原反应.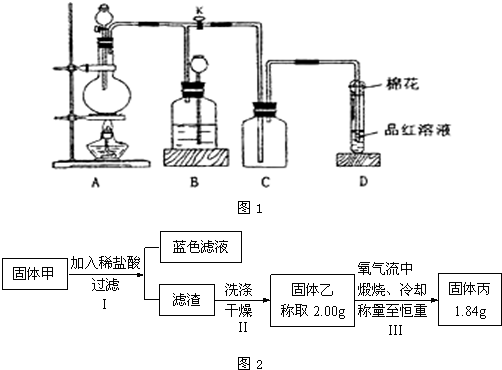
请回答:
(1)装置A中发生的化学反应方程式为
a.酸性 b.脱水性 c.强氧化性 d.吸水性
(2)装置D中试管口放置的棉花中浸入
(3)装置B的作用是贮存多余的气体.当D处有明显的现象后,关闭旋塞K并移去酒精灯,但由于余热的作用,A处仍有气体产生,此时B中的现象是
a.水 b.饱和NaHSO3溶液 c.酸性KMnO4溶液 d.NaOH溶液
(4)实验中,取一定质量的铜片和一定体积18.4mol?L-1的浓硫酸放在圆底烧瓶中共热,直到反应完毕,发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余.
①有一定量的余酸但未能使铜片完全溶解,你认为原因是
②下列药品中能用来证明反应结束后的烧瓶中确有余酸的是(填字母)
a.银粉 b.铁粉 c.BaCl2溶液 d.NaHCO3溶液
(5)实验中发现试管内除了产生白色固体外,在铜表面还产生黑色固体甲,其中可能含有氧化铜、硫化铜、硫化亚铜,以及被掩蔽的氧化亚铜.
查阅资料:
i.氧化亚铜在酸性环境下会发生自身氧化还原反应生成Cu2+和铜单质,在氧气流中煅烧,可以转化为氧化铜.
ii.硫化铜和硫化亚铜常温下都不溶于稀盐酸,在氧气流中煅烧,硫化铜和硫化亚铜都转化为氧化铜和二氧化硫.
为了研究甲的成分,该小组同学在收集到足够量的固体甲后,进行了如图2所示实验:
①Ⅲ中在煅烧过程中一定发生的反应的化学方程式为
②下列对于固体甲的成分的判断中,正确的是(填字母选项)
a.固体甲中,CuO和Cu2O至少有一种
b.固体甲中,CuS和Cu2S不能同时存在
c.固体甲中若没有Cu2O,则一定有Cu2S
d.固体甲中若存在Cu2O,也可能有Cu2S.
查看习题详情和答案>>
已知:①SO2难溶于饱和亚硫酸氢钠溶液.②SO2能与酸性高锰酸钾溶液发生氧化还原反应.

请回答:
(1)装置A中发生的化学反应方程式为
Cu+2 H2SO4(浓)
CuSO4+SO2↑+2 H2O
| ||
Cu+2 H2SO4(浓)
CuSO4+SO2↑+2 H2O
.此反应表明浓硫酸具有(填字母)
| ||
ac
ac
.a.酸性 b.脱水性 c.强氧化性 d.吸水性
(2)装置D中试管口放置的棉花中浸入
NaOH
NaOH
溶液,其作用是吸收SO2气体,防止污染空气
吸收SO2气体,防止污染空气
.(3)装置B的作用是贮存多余的气体.当D处有明显的现象后,关闭旋塞K并移去酒精灯,但由于余热的作用,A处仍有气体产生,此时B中的现象是
集气瓶内液面下降,长颈漏斗内液面上升
集气瓶内液面下降,长颈漏斗内液面上升
.B中应放置的液体是(填字母)b
b
.a.水 b.饱和NaHSO3溶液 c.酸性KMnO4溶液 d.NaOH溶液
(4)实验中,取一定质量的铜片和一定体积18.4mol?L-1的浓硫酸放在圆底烧瓶中共热,直到反应完毕,发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余.
①有一定量的余酸但未能使铜片完全溶解,你认为原因是
浓硫酸由浓变稀,稀硫酸不再与铜反应
浓硫酸由浓变稀,稀硫酸不再与铜反应
.②下列药品中能用来证明反应结束后的烧瓶中确有余酸的是(填字母)
b、d
b、d
.a.银粉 b.铁粉 c.BaCl2溶液 d.NaHCO3溶液
(5)实验中发现试管内除了产生白色固体外,在铜表面还产生黑色固体甲,其中可能含有氧化铜、硫化铜、硫化亚铜,以及被掩蔽的氧化亚铜.
查阅资料:
i.氧化亚铜在酸性环境下会发生自身氧化还原反应生成Cu2+和铜单质,在氧气流中煅烧,可以转化为氧化铜.
ii.硫化铜和硫化亚铜常温下都不溶于稀盐酸,在氧气流中煅烧,硫化铜和硫化亚铜都转化为氧化铜和二氧化硫.
为了研究甲的成分,该小组同学在收集到足够量的固体甲后,进行了如图2所示实验:
①Ⅲ中在煅烧过程中一定发生的反应的化学方程式为
2CuS+3O2
2CuO+2SO2
| ||
2CuS+3O2
2CuO+2SO2
.
| ||
②下列对于固体甲的成分的判断中,正确的是(填字母选项)
a c d
a c d
.a.固体甲中,CuO和Cu2O至少有一种
b.固体甲中,CuS和Cu2S不能同时存在
c.固体甲中若没有Cu2O,则一定有Cu2S
d.固体甲中若存在Cu2O,也可能有Cu2S.
某化学课外兴趣小组为探究铜跟浓硫酸的反应情况,用如图所示装置先进行了有关实验:
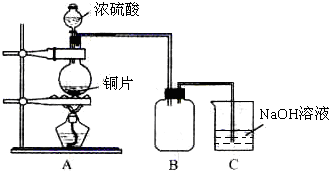
(1)B是用来收集实验中产生的气体的装置,但未将导管画全,请在图上把导管补充完整.
(2)实验中他们取6.4g 铜片和12mL 18mol?L-1浓硫酸放在圆底烧瓶中共热,直到反应完毕,最后发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余.
①写出铜跟浓硫酸反应的化学方程式: ;
②有一定量的余酸但未能使铜片完全溶解,你认为其中原因是 ;
(3)为定量测定余酸的物质的量浓度,该小组学生进行了如下设计:
先测定铜与浓硫酸反应产生的SO2的量,再计算余酸的物质的量浓度.他们认为测定二氧化硫的量的方法有多种,你认为下列实验方案中可行的是 (填写编号).
A.将装置A产生的气体缓缓通过预先称量过的盛有碱石灰的干燥管,结束反应后再次称量
B.将装置A产生的气体缓缓通入足量用稀硫酸酸化的高锰酸钾溶液,再加入足量氯化钡溶液,过滤、洗涤、干燥、称量沉淀
C.用排水法测定装置A产生气体的体积(已折算成标准状况)
D.将装置A产生的气体缓缓通入足量氢氧化钡溶液,反应完全后,过滤、洗涤、干燥、称量沉淀
E.将装置A产生的气体缓缓通入足量硝酸酸化的硝酸钡溶液,反应完全后,过滤、洗涤、干燥、称量沉淀
请你对不可行的方案中选出一例进行分析: [要求标明不可行的方案序号、说出不可行的理由及造成的误差(偏高或偏低)].
(4)请你再设计一种其他可行的实验方案,来测定余酸的物质的量浓度,简要写出操作步骤及需要测定的数据(不必计算) .
查看习题详情和答案>>

(1)B是用来收集实验中产生的气体的装置,但未将导管画全,请在图上把导管补充完整.
(2)实验中他们取6.4g 铜片和12mL 18mol?L-1浓硫酸放在圆底烧瓶中共热,直到反应完毕,最后发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余.
①写出铜跟浓硫酸反应的化学方程式:
②有一定量的余酸但未能使铜片完全溶解,你认为其中原因是
(3)为定量测定余酸的物质的量浓度,该小组学生进行了如下设计:
先测定铜与浓硫酸反应产生的SO2的量,再计算余酸的物质的量浓度.他们认为测定二氧化硫的量的方法有多种,你认为下列实验方案中可行的是
A.将装置A产生的气体缓缓通过预先称量过的盛有碱石灰的干燥管,结束反应后再次称量
B.将装置A产生的气体缓缓通入足量用稀硫酸酸化的高锰酸钾溶液,再加入足量氯化钡溶液,过滤、洗涤、干燥、称量沉淀
C.用排水法测定装置A产生气体的体积(已折算成标准状况)
D.将装置A产生的气体缓缓通入足量氢氧化钡溶液,反应完全后,过滤、洗涤、干燥、称量沉淀
E.将装置A产生的气体缓缓通入足量硝酸酸化的硝酸钡溶液,反应完全后,过滤、洗涤、干燥、称量沉淀
请你对不可行的方案中选出一例进行分析:
(4)请你再设计一种其他可行的实验方案,来测定余酸的物质的量浓度,简要写出操作步骤及需要测定的数据(不必计算)
 某化学课外兴趣小组为探究铜跟浓硫酸的反应情况,用图所示装置进行有关实验.请回答:
某化学课外兴趣小组为探究铜跟浓硫酸的反应情况,用图所示装置进行有关实验.请回答:(1)装置A中发生的化学反应方程式为
2H2SO4(浓)+Cu
CuSO4+2H2O+SO2↑;
| ||
2H2SO4(浓)+Cu
CuSO4+2H2O+SO2↑;
.
| ||
(2)装置D中试管口放置的棉花中应浸一种液体,这种液体是
氢氧化钠溶液或碳酸钠溶液等碱性溶液
氢氧化钠溶液或碳酸钠溶液等碱性溶液
,其作用是吸收多余的二氧化硫,防止污染空气
吸收多余的二氧化硫,防止污染空气
.(3)装置B的作用是贮存多余的气体.当D处有明显的现象后,关闭旋塞K并移去酒精灯,但由于余热的作用,A处仍有气体产生,此时B中现象是
瓶中液面下降,长颈漏斗中液面上升
瓶中液面下降,长颈漏斗中液面上升
.B中应放置的液体是(填字母)d
d
.a.水 b.酸性KMnO4 溶液 c.浓溴水 d.饱和NaHSO3溶液
(4)实验中,取一定质量的铜片和一定体积18mol?L-1的浓硫酸放在圆底烧瓶中共热,直到反应完毕,发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余.
①有一定量的余酸但未能使铜片完全溶解,你认为原因是
随反应进行,硫酸浓度变稀,Cu不与稀H2SO4反应;
随反应进行,硫酸浓度变稀,Cu不与稀H2SO4反应;
.②下列药品中能用来证明反应结束后的烧瓶中确有余酸的是
ad
ad
(填字母).a.铁粉 b.BaCl2溶液 c.银粉 d.NaHCO3溶液.
 某化学课外兴趣小组为探究苯与溴发生反应的反应类型并制取纯净的溴苯,进行如下实验.请根据要求回答相关问题.
某化学课外兴趣小组为探究苯与溴发生反应的反应类型并制取纯净的溴苯,进行如下实验.请根据要求回答相关问题.Ⅰ:制取溴苯(装置如图所示)
(1)向烧瓶中滴入溴的苯溶液片刻后,在烧瓶中可观察到的现象是
烧瓶中溶液沸腾,产生红棕色气体
烧瓶中溶液沸腾,产生红棕色气体
(2)锥形瓶中有淡黄色浑浊生成,能否证明苯与溴发生了取代反应(填“能”或“不能”)
不能
不能
,原因是逸出的溴蒸汽也能与硝酸银反应生成淡黄色沉淀
逸出的溴蒸汽也能与硝酸银反应生成淡黄色沉淀
.(3)若不能确定,请从下列装置中选取适宜装置加以改进,请在下面实验流程图的方框中填入序号.
(Ⅰ):
②
②
;(Ⅱ):④
④

①装有NaOH溶液的洗气瓶
②装有CCl4的洗气瓶
③装有KI溶液的洗气瓶
④装有湿润淀粉KI试纸的集气瓶
(4)该实验还可用
石蕊试液或者碳酸氢钠溶液
石蕊试液或者碳酸氢钠溶液
代替AgNO3溶液检验取代反应的产物之一溴化氢.Ⅱ:提纯溴苯
(5)反应后所得混合液,经以下几步操作可得到纯净的溴苯.简要写出各操作步骤和目的(不一定填满).

操作1
水洗后分液
水洗后分液
;目的:除去溴化铁
除去溴化铁
.操作2
氢氧化钠溶液洗涤后分液
氢氧化钠溶液洗涤后分液
;目的:除去未反应的溴
除去未反应的溴
.操作3
蒸馏
蒸馏
;目的:除去苯等有机杂质
除去苯等有机杂质
.操作4
无
无
;目的:无
无
.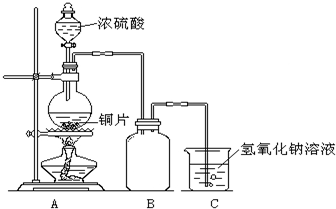 某化学课外兴趣小组为探究铜与浓硫酸的反应,用右图所示的装置进行实验:
某化学课外兴趣小组为探究铜与浓硫酸的反应,用右图所示的装置进行实验:请回答下列问题:
(1)B是用来收集实验中产生气体的装置,但未将导管画全,请将装置图补充完整.
(2)实验中他们取6.4g铜片和12mL18mol?L-1浓硫酸放在圆底烧瓶中共热,直到反应停止,最后发现烧瓶中还有铜片剩余,该小组中的同学认为还有一定量的硫酸剩余.
①写出铜与浓硫酸反应的化学方程式:
Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O
| ||
Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O
,
| ||
实验中若有m g铜参加了反应,则有
| m |
| 64 |
| m |
| 64 |
还原
还原
(填“氧化”或“还原”),转移电子的物质的量为| m |
| 32 |
| m |
| 32 |
②下列试剂中,能证明反应停止后烧瓶中有硫酸剩余的是
D
D
(填写字母编号).A.硫酸钠溶液 B.氯化钡溶液 C.银粉 D.碳酸钠溶液
③为什么有一定量的硫酸剩余但未能使铜片完全溶解?你认为的原因是
稀硫酸不与铜反应
稀硫酸不与铜反应
(3)为了测定剩余硫酸的物质的量浓度,该兴趣小组设计了三个实验方案:
方案一:将装置A产生的气体缓缓通过已称量过的装有碱石灰的干燥管,反应停止后再次称量,两次质量差即是吸收的二氧化硫.
方案二:将装置A产生的气体缓缓通入足量的用硫酸酸化的高锰酸钾溶液,再加入足量的氯化钡溶液,过滤、洗涤、干燥,称得沉淀的质量即是二氧化硫转化为硫酸钡沉淀的质量.
方案三:当铜和浓硫酸的反应结束后,在装置A中加入足量的锌粉,用排水法测得产生氢气的体积为V L(已换算为标准状况).
实际上,以上方案一、二均不可取,请你说出原因?
方案一
产生的气体中含有水蒸气,干燥管中的质量差不仅仅是SO2的质量(或烧瓶中的二氧化硫不能完全排出)
产生的气体中含有水蒸气,干燥管中的质量差不仅仅是SO2的质量(或烧瓶中的二氧化硫不能完全排出)
;方案二
沉淀的质量一部分是高锰酸钾溶液中起酸化作用的硫酸与氯化钡反应而产生的
沉淀的质量一部分是高锰酸钾溶液中起酸化作用的硫酸与氯化钡反应而产生的
.方案三:写出剩余硫酸的物质的量浓度的计算式(假设反应后溶液的体积仍为12mL)
| V |
| 22.4×0.012 |
| V |
| 22.4×0.012 |