摘要:25℃时.5 mLO.1 mol·L -1 H2S04和15mL0.1 mol·L -1 NaOH 溶液相混合并稀释至500mL.所得溶液的pH为 A.12.3 B.11 C.3 D.1.7
网址:http://m.1010jiajiao.com/timu3_id_432253[举报]
25℃时,5 mL0.1 mol·L-1 H2SO4和15mL0.1 mol·L-1 NaOH溶液相混合并稀释至500mL,所得溶液的pH为
[ ]
A.12.3
B.11
C.3
D.1.7
查看习题详情和答案>>
B.11
C.3
D.1.7
(1)25℃时x mol?L-1的CH3COOH溶液与0.01mol?L-1的NaOH溶液等体积混合,溶液显中性,则[CH3COO-]
(2)高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压,高铁电池的总反应为3Zn+2K2FeO4+8H2O
3Zn(OH)2+2Fe(OH)3+4KOH
①写出该电池充电时阴阳两极的电极反应式
阴极:
阳极:
②下列叙述正确的是
A.Zn电极在放电时作负极,发生氧化反应
B.该电池放电时,K+向负极移动
C.放电时正极有1molK2FeO4被还原,则转移3mol电子,
③用该电池电解200mL 1mol?L-1 的AgNO3溶液(用惰性电极),当阴极质量增加2.16g时,被电解溶液的pH为
(3)几种常见离子在溶液中开始沉淀时的pH如下表:
当向含相同浓度Cu2+、Mg2+、Fe2+离子的溶液中滴加NaOH溶液时,
查看习题详情和答案>>
=
=
[Na+](填“>”“=”“<”),用含x的代数式表示CH3COOH的电离平衡常数Ka=| 10-9 |
| x-10-2 |
| 10-9 |
| x-10-2 |
(2)高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压,高铁电池的总反应为3Zn+2K2FeO4+8H2O
| 放电 |
| 充电 |
①写出该电池充电时阴阳两极的电极反应式
阴极:
Zn(OH)2+2e-=Zn+2OH-
Zn(OH)2+2e-=Zn+2OH-
阳极:
Fe(OH)3-3e-+5OH-=FeO42-+4H2O
Fe(OH)3-3e-+5OH-=FeO42-+4H2O
②下列叙述正确的是
AC
AC
(填字母).A.Zn电极在放电时作负极,发生氧化反应
B.该电池放电时,K+向负极移动
C.放电时正极有1molK2FeO4被还原,则转移3mol电子,
③用该电池电解200mL 1mol?L-1 的AgNO3溶液(用惰性电极),当阴极质量增加2.16g时,被电解溶液的pH为
1
1
(溶液体积变化忽略不计).(3)几种常见离子在溶液中开始沉淀时的pH如下表:
| 离子 | Fe2+ | Cu2+ | Mg2+ |
| pH | 7.6 | 5.2 | 10.4 |
Cu2+
Cu2+
(填离子符号)先沉淀,KSP[(Fe(OH)2]<
<
KSP[(Mg(OH)2](填“>”、“=”或“<”).25℃时,用两个质量相同的铜棒作电极,电解500mL 0.1mol?L-1 H2SO4溶液,电解过程中,电解液的pH变化如表所示(假定溶液温度保持不变).电解2h后,取出电极,对电极进行干燥,并称量,测得两电极的质量差为9.6g.已知,25℃时0.1mol?L-1 CuSO4溶液的pH为4.17.
(1)实验刚开始阶段电解池阴极所发生反应的电极反应式为
(2)电解进行到1.5h后,电解质溶液的pH不再发生变化的原因是
(3)电解进行的2h中,转移电子的总物质的量
(4)若欲使所得电解质溶液复原到500mL 0.1mol?L-1 H2SO4溶液,应对溶液进行怎样处理?
查看习题详情和答案>>
| 时间/h | 0.5 | 1 | 1.5 | 2 |
| pH | 1.3 | 2.4 | 3.0 | 3.0 |
2H++2e-═H2↑
2H++2e-═H2↑
.(2)电解进行到1.5h后,电解质溶液的pH不再发生变化的原因是
电解持续进行,H+电解完后,电解过程发生转变,阳极反应式为Cu-2e-═Cu2+,阴极反应式为Cu2++2e-═Cu,电解质溶液的组成、浓度不再发生变化,溶液的pH也不再发生变化
电解持续进行,H+电解完后,电解过程发生转变,阳极反应式为Cu-2e-═Cu2+,阴极反应式为Cu2++2e-═Cu,电解质溶液的组成、浓度不再发生变化,溶液的pH也不再发生变化
;用离子反应方程式表示0.1mol?L-1 CuSO4溶液的pH为4.17的原因Cu2++2H2?Cu(OH)2+2H+
Cu2++2H2?Cu(OH)2+2H+
.(3)电解进行的2h中,转移电子的总物质的量
>
>
0.15mol(填“<”、“=”或“>”).(4)若欲使所得电解质溶液复原到500mL 0.1mol?L-1 H2SO4溶液,应对溶液进行怎样处理?
向溶液中通入约0.05mol H2S
向溶液中通入约0.05mol H2S
.运用反应原理研究氮、硫、氯、碘及其化合物的反应有重要意义.
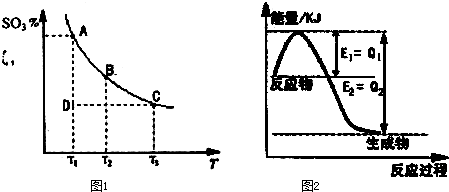
(1 )在反应:2SO2(g)+O2(g)?2SO3(g)的混合体系中,SO3的百分含量和温度的关系如图1(曲线上任何一点都表示平衡状态):
①2SO2(g)+O2(g)?2SO3(g)的△H 0 (填“>”或“<”);若在恒温、恒压时,向该平衡体系中通入氦气,平衡将 移动(填“向左”、“向右”或“不”);
②当温度为T1,反应进行到状态D时,V正 V逆(填“>”、“<”或“=).
(2 )①图2是一定条件下,N2和H2发生可逆反应生成1mol NH3的能量变化图,该反应的热化学反应方程式 .
(△H用含Q1、Q2的代数式表示) ②25°C时,将a mol?L-1的氨水与b mol?L-1的盐酸等体积混合,所得溶液的PH=7,则c ( NH+4) c (Cl-),a b,(填“>”、“<”或“=”);
(3)海水中含有大量以化合态形式存在的氯、碘元素.
已知:25℃时,Ksp[AgCl]=1.6×10-10 mol2?L-2、Ksp[AgI]=1.5×10-16mol2?L-2).在 25℃时,向 10mL0.002mol?l-1 的 NaCl 溶液中滴入 10mL0.002mol.l-1AgNO3溶液,有白色沉淀生成,向所得浊液中继续滴入O.1mol l-1的NaI溶液,白色沉淀逐渐转化为黄色沉淀,其原因是 ,该反应的离子方程式 .
查看习题详情和答案>>
(1 )在反应:2SO2(g)+O2(g)?2SO3(g)的混合体系中,SO3的百分含量和温度的关系如图1(曲线上任何一点都表示平衡状态):
①2SO2(g)+O2(g)?2SO3(g)的△H
②当温度为T1,反应进行到状态D时,V正
(2 )①图2是一定条件下,N2和H2发生可逆反应生成1mol NH3的能量变化图,该反应的热化学反应方程式
(△H用含Q1、Q2的代数式表示) ②25°C时,将a mol?L-1的氨水与b mol?L-1的盐酸等体积混合,所得溶液的PH=7,则c ( NH+4)

(3)海水中含有大量以化合态形式存在的氯、碘元素.
已知:25℃时,Ksp[AgCl]=1.6×10-10 mol2?L-2、Ksp[AgI]=1.5×10-16mol2?L-2).在 25℃时,向 10mL0.002mol?l-1 的 NaCl 溶液中滴入 10mL0.002mol.l-1AgNO3溶液,有白色沉淀生成,向所得浊液中继续滴入O.1mol l-1的NaI溶液,白色沉淀逐渐转化为黄色沉淀,其原因是
 近现代战争中,制造坦克战车最常用的装甲材料是经过轧制和热处理后的合金钢,热处理后整个装甲结构的化学和机械特性和最大限度的保持一致.钢中合金元素的百分比含量为:铬0.5~1.25 镍0.5~1.5 钼0.3~0.6 锰0.8~1.6 碳0.3
近现代战争中,制造坦克战车最常用的装甲材料是经过轧制和热处理后的合金钢,热处理后整个装甲结构的化学和机械特性和最大限度的保持一致.钢中合金元素的百分比含量为:铬0.5~1.25 镍0.5~1.5 钼0.3~0.6 锰0.8~1.6 碳0.3(1)铬元素的基态原子的价电子层排布式是
(2)C元素与其同主族下一周期元素组成的晶体中,C原子的杂化方式为
(3)Mn和Fe的部分电离能数据如下表:
| 元素 | Mn | Fe | |
| 电离能 /kJ?mol-1 |
I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
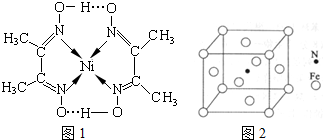
(4)镍(Ni)可形成多种配合物,且各种配合物有广泛的用途.某镍配合物结构如图1所示,分子内含有的作用力有
A.氢键 B.离子键 C.共价键 D.金属键 E.配位键
组成该配合物分子且同属第二周期元素的电负性由大到小的顺序是
(5)金属镍粉在CO气流中轻微加热,生成无色挥发性液态Ni(CO)4,呈四面体构型.423K时,Ni(CO)4分解为Ni和CO,从而制得高纯度的Ni粉.试推测:四羰基镍的晶体类型是
(6)铁能与氮形成一种磁性材料,其晶胞结构如图2所示,则该磁性材料的化学式为