摘要: 常温下.向含白色沉淀M的浊液中加入氯化钠固体.M的溶解度 将 (填“增大".“减小"或“不变 ).将 (填“增大".“减小"或“不变 ).
网址:http://m.1010jiajiao.com/timu3_id_431843[举报]
甲、乙、丙均为中学化学常见的气体单质,A、B、C为常见的化合物,已知:
(1)A和B都极易溶于水,用两根玻璃棒分别蘸取A和B的浓溶液后,相互靠近会看到白烟
(2)各物质之间存在如下图所示的转化关系
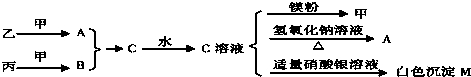
请回答下列问题:
(1)写出物质A与B的化学式:______、______.
(2)C溶液中离子浓度的大小关系是______.
(3)“C溶液+镁粉→甲”的化学方程式为______.
(4)丙气体通入200mL氢氧化钠溶液中恰好完全反应,此时电子转移总数为0.1NA,则氢氧化钠溶液的pH为______.
(5)常温下,向含白色沉淀M的浊液中加入氯化钠固体,M的溶解度将______(填“增大”、“减小”或“不变”),Ksp(M)将______(填“增大”、“减小”或“不变”).
查看习题详情和答案>>
甲、乙、丙均为中学化学常见的气体单质,A、B、C为常见的化合物,已知:
(1)A和B都极易溶于水,用两根玻璃棒分别蘸取A和B的浓溶液后,相互靠近会看到白烟
(2)各物质之间存在如下图所示的转化关系
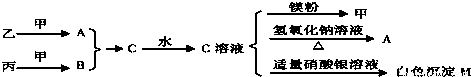
请回答下列问题:
(1)写出物质A与B的化学式:______、______.
(2)C溶液中离子浓度的大小关系是______.
(3)“C溶液+镁粉→甲”的化学方程式为______.
(4)丙气体通入200mL氢氧化钠溶液中恰好完全反应,此时电子转移总数为0.1NA,则氢氧化钠溶液的pH为______.
(5)常温下,向含白色沉淀M的浊液中加入氯化钠固体,M的溶解度将______(填“增大”、“减小”或“不变”),Ksp(M)将______(填“增大”、“减小”或“不变”).
查看习题详情和答案>>
(1)A和B都极易溶于水,用两根玻璃棒分别蘸取A和B的浓溶液后,相互靠近会看到白烟
(2)各物质之间存在如下图所示的转化关系

请回答下列问题:
(1)写出物质A与B的化学式:______、______.
(2)C溶液中离子浓度的大小关系是______.
(3)“C溶液+镁粉→甲”的化学方程式为______.
(4)丙气体通入200mL氢氧化钠溶液中恰好完全反应,此时电子转移总数为0.1NA,则氢氧化钠溶液的pH为______.
(5)常温下,向含白色沉淀M的浊液中加入氯化钠固体,M的溶解度将______(填“增大”、“减小”或“不变”),Ksp(M)将______(填“增大”、“减小”或“不变”).
查看习题详情和答案>>
甲、乙、丙均为中学化学常见的气体单质,A、B、C为常见的化合物,已知:
(1)A和B都极易溶于水,用两根玻璃棒分别蘸取A和B的浓溶液后,相互靠近会看到白烟
(2)各物质之间存在如下图所示的转化关系
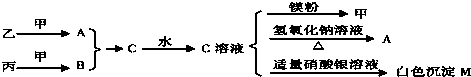
请回答下列问题:
(1)写出物质A与B的化学式:
(2)C溶液中离子浓度的大小关系是
(3)“C溶液+镁粉→甲”的化学方程式为
(4)丙气体通入200mL氢氧化钠溶液中恰好完全反应,此时电子转移总数为0.1NA,则氢氧化钠溶液的pH为
(5)常温下,向含白色沉淀M的浊液中加入氯化钠固体,M的溶解度将
查看习题详情和答案>>
(1)A和B都极易溶于水,用两根玻璃棒分别蘸取A和B的浓溶液后,相互靠近会看到白烟
(2)各物质之间存在如下图所示的转化关系

请回答下列问题:
(1)写出物质A与B的化学式:
NH3
NH3
、HCl
HCl
.(2)C溶液中离子浓度的大小关系是
c(Cl-)>c(NH4+)>c(H+)>c(OH-)
c(Cl-)>c(NH4+)>c(H+)>c(OH-)
.(3)“C溶液+镁粉→甲”的化学方程式为
Mg+2NH4Cl=MgCl2+2NH3↑+H2↑
Mg+2NH4Cl=MgCl2+2NH3↑+H2↑
.(4)丙气体通入200mL氢氧化钠溶液中恰好完全反应,此时电子转移总数为0.1NA,则氢氧化钠溶液的pH为
14
14
.(5)常温下,向含白色沉淀M的浊液中加入氯化钠固体,M的溶解度将
减小
减小
(填“增大”、“减小”或“不变”),Ksp(M)将不变
不变
(填“增大”、“减小”或“不变”).甲、乙、丙均为中学化学常见的气体单质,A、B、C为常见的化合物,已知:
①A和B都极易溶于水,用两根玻璃棒分别蘸取A和B的浓溶液后,相互靠近会看到白烟.
②各物质之间存在如图所示的转化关系
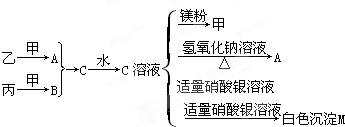
请回答下列问题:
(1)C溶液显
(2)乙和甲反应生成A的化学方程式为
(3)丙气体通入1L氢氧化钠溶液中恰好完全反应,此时电子转移为2mol,则氢氧化钠溶液的物质的量浓度为
(4)常温下,向含白色沉淀M的浊中加入氯化钠固体,M的溶解度将
查看习题详情和答案>>
①A和B都极易溶于水,用两根玻璃棒分别蘸取A和B的浓溶液后,相互靠近会看到白烟.
②各物质之间存在如图所示的转化关系

请回答下列问题:
(1)C溶液显
酸
酸
性(填“酸”、“碱”或“中”),理由是NH4++H2O NH3?H2O+H+
NH3?H2O+H+
 NH3?H2O+H+
NH3?H2O+H+NH4++H2O NH3?H2O+H+
NH3?H2O+H+
(离子方程式表示). NH3?H2O+H+
NH3?H2O+H+(2)乙和甲反应生成A的化学方程式为
N2+3H2
2NH3
| ||
| 高温高压 |
N2+3H2
2NH3
.C和氢氧化钠溶液生成A的离子方程式为
| ||
| 高温高压 |
NH4++OH-
NH3↑+H2O
| ||
NH4++OH-
NH3↑+H2O
.
| ||
(3)丙气体通入1L氢氧化钠溶液中恰好完全反应,此时电子转移为2mol,则氢氧化钠溶液的物质的量浓度为
4mol/L
4mol/L
.(4)常温下,向含白色沉淀M的浊中加入氯化钠固体,M的溶解度将
减小
减小
(填“增大”、“减小”或“不变”),Ksp(M)将不变
不变
(填“增大”、“减少”或“不变”).(9分)运用化学反应原理研究氮、硫、氯、碘等单质及其化合物的反应有重要意义。
(1)氮是地球上含量丰富的元素,氮及其化合物在工农业生产、生活中有着重要作用。
①下图是一定的温度和压强下是N2和H2反应生成1molNH3过程中能量变化示意图,请写出工业合成氨的热化学反应方程式: 。(△H的数值用含字母a、b的代数式表示)
②氨气溶于水得到氨水。在25°C下,将m mol·L-1的氨水与n mol·L-1的盐酸等体积混合,反应后的溶液呈中性,则c(NH+4) c(Cl-)(填“>”、“<”或“=”);用含m和n的代数式表示出混合液中氨水的电离平衡常数表达式 。
(2)海水中含有大量的元素,常量元素如氯、微量元素如碘在海水中均以化合态存在。
25°C下,向0.1mol·L-1的NaCl溶液中逐滴加入适量的0.1mol·L-1硝酸银溶液,有白色沉淀生成。从沉淀溶解平衡的角度解释产生沉淀的原因是 ,向反应后的浊液中,继续加入适量0.1mol·L-1的NaI溶液,振荡、静置,看到的现象是 ,产生该现象的原因是(用离子方程式表示) 。
(已知25°C时![]() )
)
查看习题详情和答案>>