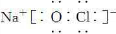题目内容
甲、乙、丙均为中学化学常见的气体单质,A、B、C为常见的化合物,已知:
(1)A和B都极易溶于水,用两根玻璃棒分别蘸取A和B的浓溶液后,相互靠近会看到白烟
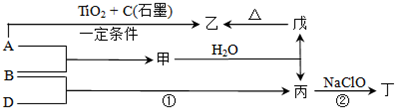
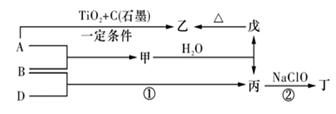
(2)各物质之间存在如下图所示的转化关系
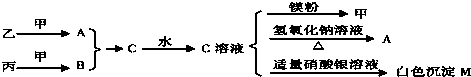
请回答下列问题:
(1)写出物质A与B的化学式:
(2)C溶液中离子浓度的大小关系是
(3)“C溶液+镁粉→甲”的化学方程式为
(4)丙气体通入200mL氢氧化钠溶液中恰好完全反应,此时电子转移总数为0.1NA,则氢氧化钠溶液的pH为
(5)常温下,向含白色沉淀M的浊液中加入氯化钠固体,M的溶解度将
(1)A和B都极易溶于水,用两根玻璃棒分别蘸取A和B的浓溶液后,相互靠近会看到白烟
(2)各物质之间存在如下图所示的转化关系

请回答下列问题:
(1)写出物质A与B的化学式:
NH3
NH3
、HCl
HCl
.(2)C溶液中离子浓度的大小关系是
c(Cl-)>c(NH4+)>c(H+)>c(OH-)
c(Cl-)>c(NH4+)>c(H+)>c(OH-)
.(3)“C溶液+镁粉→甲”的化学方程式为
Mg+2NH4Cl=MgCl2+2NH3↑+H2↑
Mg+2NH4Cl=MgCl2+2NH3↑+H2↑
.(4)丙气体通入200mL氢氧化钠溶液中恰好完全反应,此时电子转移总数为0.1NA,则氢氧化钠溶液的pH为
14
14
.(5)常温下,向含白色沉淀M的浊液中加入氯化钠固体,M的溶解度将
减小
减小
(填“增大”、“减小”或“不变”),Ksp(M)将不变
不变
(填“增大”、“减小”或“不变”).分析:先通过题眼判断C物质,然后通过C判断甲、A、M,通过A判断B、乙、丙,再通过题中信息分析习题.
解答:解:(1)用两根玻璃棒分别蘸取A和B的浓溶液后,相互靠近会看到白烟,得A、B是NH3和HCl,C就是NH4Cl.
NH4Cl是强酸弱碱盐,溶液呈酸性,与镁粉反应,NH4++H2O
NH3.H2O+H+,2H++Mg=Mg2++H2,甲是气体单质,所以甲是氢气.
NH4Cl溶液与氢氧化钠溶液加热反应方程式为NH4Cl+NaOH
NH3↑+NaCl+H2O,A是常见化合物,且极易溶于水,
A由甲与乙气体单质反应得到,所以A是氨气,甲是氢气,所以乙是氮气,
所以A是NH3,B是HCl.丙是氯气.
故答案为:NH3;HCl;
(2)C溶液是NH4Cl溶液,NH4Cl是强酸弱碱盐,溶液呈酸性,NH4++H2O
NH3.H2O+H+导致溶液中c(Cl-)>c(NH4+),c(H+)>c(OH-),
故答案为:c(Cl-)>c(NH4+)>c(H+)>c(OH-);
(3)NH4Cl是强酸弱碱盐,溶液呈酸性,NH4++H2O
NH3.H2O+H+,与镁粉反应有气体生成,同时生成氯化镁,故答案为:Mg+2NH4Cl=MgCl2+2NH3↑+H2↑;
(4)设氢氧化钠的物质的量浓度为xmol/L,
氯气与氢氧化钠溶液的反应方程式为:
Cl2+2NaOH=NaCl+NaClO+H2O 转移电子数
2 NA
0.2x 0.1NA
则x=1,即氢氧化钠的浓度为1mol/L,根据水的离子积常数得,氢离子的浓度为10-14mol/L,
所以,pH=14,故答案为:14;
(5)、NH4Cl+AgNO3=AgCl↓+NH4NO3白色沉淀是AgCl,即M是AgCl,AgCl
Ag++Cl-,这是一个可逆反应,加入氯化钠固体,氯离子的浓度增加,
平衡向逆反应方向移动,氯化银的溶解度降低,难溶物的Ksp只与温度有关,与离子的浓度无关.
故答案为:减小;不变.
NH4Cl是强酸弱碱盐,溶液呈酸性,与镁粉反应,NH4++H2O
| 水解 |
NH4Cl溶液与氢氧化钠溶液加热反应方程式为NH4Cl+NaOH
| ||
A由甲与乙气体单质反应得到,所以A是氨气,甲是氢气,所以乙是氮气,
所以A是NH3,B是HCl.丙是氯气.
故答案为:NH3;HCl;
(2)C溶液是NH4Cl溶液,NH4Cl是强酸弱碱盐,溶液呈酸性,NH4++H2O
| 水解 |
故答案为:c(Cl-)>c(NH4+)>c(H+)>c(OH-);
(3)NH4Cl是强酸弱碱盐,溶液呈酸性,NH4++H2O
| 水解 |
(4)设氢氧化钠的物质的量浓度为xmol/L,
氯气与氢氧化钠溶液的反应方程式为:
Cl2+2NaOH=NaCl+NaClO+H2O 转移电子数
2 NA
0.2x 0.1NA
则x=1,即氢氧化钠的浓度为1mol/L,根据水的离子积常数得,氢离子的浓度为10-14mol/L,
所以,pH=14,故答案为:14;
(5)、NH4Cl+AgNO3=AgCl↓+NH4NO3白色沉淀是AgCl,即M是AgCl,AgCl
| 电离 |
平衡向逆反应方向移动,氯化银的溶解度降低,难溶物的Ksp只与温度有关,与离子的浓度无关.
故答案为:减小;不变.
点评:找出题眼是解本题的关键,然后根据相关信息分析.对于元素化合物推断题,要注意一些特殊现象,然后根据特殊现象判断物质.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目