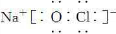题目内容
甲、乙、丙均为中学化学常见的气体单质,A、B、C为常见的化合物,已知:
①A和B都极易溶于水,用两根玻璃棒分别蘸取A和B的浓溶液后,相互靠近会看到白烟.
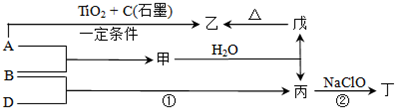
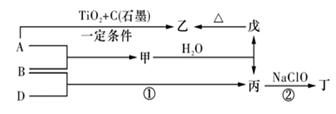
②各物质之间存在如图所示的转化关系
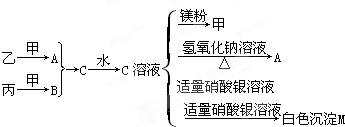
请回答下列问题:
(1)C溶液显
(2)乙和甲反应生成A的化学方程式为
(3)丙气体通入1L氢氧化钠溶液中恰好完全反应,此时电子转移为2mol,则氢氧化钠溶液的物质的量浓度为
(4)常温下,向含白色沉淀M的浊中加入氯化钠固体,M的溶解度将
①A和B都极易溶于水,用两根玻璃棒分别蘸取A和B的浓溶液后,相互靠近会看到白烟.
②各物质之间存在如图所示的转化关系

请回答下列问题:
(1)C溶液显
酸
酸
性(填“酸”、“碱”或“中”),理由是NH4++H2O NH3?H2O+H+
NH3?H2O+H+
 NH3?H2O+H+
NH3?H2O+H+NH4++H2O NH3?H2O+H+
NH3?H2O+H+
(离子方程式表示). NH3?H2O+H+
NH3?H2O+H+(2)乙和甲反应生成A的化学方程式为
N2+3H2
2NH3
| ||
| 高温高压 |
N2+3H2
2NH3
.C和氢氧化钠溶液生成A的离子方程式为
| ||
| 高温高压 |
NH4++OH-
NH3↑+H2O
| ||
NH4++OH-
NH3↑+H2O
.
| ||
(3)丙气体通入1L氢氧化钠溶液中恰好完全反应,此时电子转移为2mol,则氢氧化钠溶液的物质的量浓度为
4mol/L
4mol/L
.(4)常温下,向含白色沉淀M的浊中加入氯化钠固体,M的溶解度将
减小
减小
(填“增大”、“减小”或“不变”),Ksp(M)将不变
不变
(填“增大”、“减少”或“不变”).分析:由A和B都极易溶于水,用两根玻璃棒分别蘸取A和B的浓溶液后,相互靠近会看到白,则A、B分别为氨气和HCl,所以C为NH4Cl,C与NaOH反应生成A,所以A为NH3,则B为HCl,结合转化关系可知,乙为N2,甲为H2,丙为Cl2,白色沉淀M为AgCl,然后结合物质的性质来解答.
解答:解:由A和B都极易溶于水,用两根玻璃棒分别蘸取A和B的浓溶液后,相互靠近会看到白,则A、B分别为氨气和HCl,所以C为NH4Cl,C与NaOH反应生成A,所以A为NH3,则B为HCl,结合转化关系可知,乙为N2,甲为H2,丙为Cl2,白色沉淀M为AgCl,
(1)氯化铵溶液水解显酸性,水解离子反应为NH4++H2O NH3?H2O+H+,故答案为:酸;NH4++H2O
NH3?H2O+H+,故答案为:酸;NH4++H2O NH3?H2O+H+;
NH3?H2O+H+;
(2)乙和甲反应生成A的化学方程式为N2+3H2
2NH3,C和氢氧化钠溶液生成A的离子方程式为NH4++OH-
NH3↑+H2O,
故答案为:N2+3H2
2NH3;NH4++OH-
NH3↑+H2O;
(3)由Cl2+2NaOH=NaCl+NaClO+H2O可知,该反应中转移1mol电子,则电子转移为2mol,消耗4molNaOH,其浓度为
=4mol/L,故答案为:4mol/L;
(4)由AgCl(s) Ag+(aq)+Cl-(aq)可知,加入氯化钠固体,溶解平衡逆向移动,M的溶解度将减小,而温度不变,则Ksp(M)不变,
Ag+(aq)+Cl-(aq)可知,加入氯化钠固体,溶解平衡逆向移动,M的溶解度将减小,而温度不变,则Ksp(M)不变,
故答案为:减小;不变.
(1)氯化铵溶液水解显酸性,水解离子反应为NH4++H2O
 NH3?H2O+H+,故答案为:酸;NH4++H2O
NH3?H2O+H+,故答案为:酸;NH4++H2O NH3?H2O+H+;
NH3?H2O+H+; (2)乙和甲反应生成A的化学方程式为N2+3H2
| ||
| 高温高压 |
| ||
故答案为:N2+3H2
| ||
| 高温高压 |
| ||
(3)由Cl2+2NaOH=NaCl+NaClO+H2O可知,该反应中转移1mol电子,则电子转移为2mol,消耗4molNaOH,其浓度为
| 4mol |
| 1L |
(4)由AgCl(s)
 Ag+(aq)+Cl-(aq)可知,加入氯化钠固体,溶解平衡逆向移动,M的溶解度将减小,而温度不变,则Ksp(M)不变,
Ag+(aq)+Cl-(aq)可知,加入氯化钠固体,溶解平衡逆向移动,M的溶解度将减小,而温度不变,则Ksp(M)不变,故答案为:减小;不变.
点评:本题考查无机物的推断,注意白烟为解答本题的突破口,熟悉铵盐的生成及氨气的制法即可解答,注重基本知识的考查,题目难度中等.

练习册系列答案
 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案
相关题目