网址:http://m.1010jiajiao.com/timu3_id_431541[举报]
CO(g)+H2O(g)
 H2(g)+CO2(g)的平衡常数随温度的变化如下表
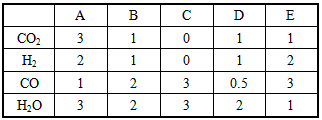
H2(g)+CO2(g)的平衡常数随温度的变化如下表
(1)上述正向反应的△H____0(填“>”或“<”)。
(2)若在800℃时进行上述反应,各物质以不同的物质的量(单位:mol)组合分别投入恒容反应器,则向正反应方向移动的有_______(填字母编号)。
(4)常温常压下,空气中的CO2溶于水,达到平衡时,溶液的pH=5. 60,c(H2CO3)=1.5×10-5 mol/L。若忽略水的电离及H2CO3的第二级电离,则H2CO3
 HCO3-+H+的平衡常数K1=___________。
HCO3-+H+的平衡常数K1=___________。(已知:10-5.60= 2.5×10-6)
“富煤、贫油、少气”是我国能源发展面临的现状。随着能源的日益紧张,发展“煤化工”对我国能源结构的调整具有重要意义。下图是煤化工产业链之一。

“洁净煤技术”研究在世界上相当普遍,科研人员通过向地下煤层气化炉中交替鼓入空气和水蒸气的方法,连续产出热值很高的煤炭合成气,其主要成分是CO和H2。CO和H2可作为能源和化工原料,应用十分广泛。
(1)已知:C(s)+O2(g)=CO2(g) ΔH1=-393.5 kJ·mol–1 ①
C(s)+H2O(g)=CO(g)+H2(g) ΔH2=+131.3 kJ·mol–1 ②
则反应CO(g)+H2(g) +O2(g)= H2O(g)+CO2(g),ΔH= _________kJ·mol–1。在标准状况下,33.6 L的煤炭合成气(设全部为CO和H2)与氧气完全反应生成CO2和H2O,反应中转移______mole-。
(2)在一恒容的密闭容器中,由CO和H2合成甲醇:CO(g)+2H2(g) CH3OH(g)
CH3OH(g)
①下列情形能说明上述反应已达到平衡状态的是_______
a.体系压强保持不变
b.密闭容器中CO、H2、CH3OH(g)3种气体共存
c.CH3OH与H2物质的量之比为1:2
d.每消耗1 mol CO的同时生成2molH2
②CO的平衡转化率(α)与温度、压强的关系如图所示。

A、B两点的平衡常数_____(填“前者”、“后者”或“一样”)大; 达到A、C两点的平衡状态所需的时间tA tC(填“大于”、“小于”或“等于”)。
在不改变反应物用量的情况下,为提高CO的转化率可采取的措施是_____________(答出两点即可)。
(3)工作温度650℃的熔融盐燃料电池,是用煤炭气(CO、H2)作负极燃气,空气与CO2的混合气体为正极燃气,用一定比例的Li2CO3和Na2CO3低熔点混合物做电解质,以金属镍(燃料极)为催化剂制成的。负极的电极反应式为:CO + H2-4e- + 2CO32-= 3CO2+H2O;则该电池的正极反应式为____________。
查看习题详情和答案>>
“富煤、贫油、少气”是我国能源发展面临的现状。随着能源的日益紧张,发展“煤化工”对我国能源结构的调整具有重要意义。下图是煤化工产业链之一。
“洁净煤技术”研究在世界上相当普遍,科研人员通过向地下煤层气化炉中交替鼓入空气和水蒸气的方法,连续产出热值很高的煤炭合成气,其主要成分是CO和H2。CO和H2可作为能源和化工原料,应用十分广泛。
(1)已知:C(s)+O2(g)=CO2(g) ΔH1=-393.5 kJ·mol–1 ①
C(s)+H2O(g)=CO(g)+H2(g) ΔH2=+131.3 kJ·mol–1 ②
则反应CO(g)+H2(g) +O2(g)= H2O(g)+CO2(g),ΔH= _________kJ·mol–1。在标准状况下,33.6 L的煤炭合成气(设全部为CO和H2)与氧气完全反应生成CO2和H2O,反应中转移______mole-。
(2)在一恒容的密闭容器中,由CO和H2合成甲醇:CO(g)+2H2(g) CH3OH(g)
CH3OH(g)
①下列情形能说明上述反应已达到平衡状态的是_______
a.体系压强保持不变
b.密闭容器中CO、H2、CH3OH(g)3种气体共存
c.CH3OH与H2物质的量之比为1:2
d.每消耗1 mol CO的同时生成2molH2
②CO的平衡转化率(α)与温度、压强的关系如图所示。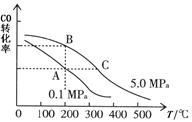
A、B两点的平衡常数_____(填“前者”、“后者”或“一样”)大;达到A、C两点的平衡状态所需的时间tA tC(填“大于”、“小于”或“等于”)。
在不改变反应物用量的情况下,为提高CO的转化率可采取的措施是_____________(答出两点即可)。
(3)工作温度650℃的熔融盐燃料电池,是用煤炭气(CO、H2)作负极燃气,空气与CO2的混合气体为正极燃气,用一定比例的Li2CO3和Na2CO3低熔点混合物做电解质,以金属镍(燃料极)为催化剂制成的。负极的电极反应式为:CO + H2-4e- + 2CO32-= 3CO2+H2O;则该电池的正极反应式为____________。

“洁净煤技术”研究在世界上相当普遍,科研人员通过向地下煤层气化炉中交替鼓入空气和水蒸气的方法,连续产出热值很高的煤炭合成气,其主要成分是CO和H2。CO和H2可作为能源和化工原料,应用十分广泛。
(1)已知:C(s)+O2(g)=CO2(g) ΔH1=-393.5 kJ·mol–1 ①
C(s)+H2O(g)=CO(g)+H2(g) ΔH2=+131.3 kJ·mol–1 ②
则反应CO(g)+H2(g) +O2(g)= H2O(g)+CO2(g),ΔH= _________kJ·mol–1。在标准状况下,33.6 L的煤炭合成气(设全部为CO和H2)与氧气完全反应生成CO2和H2O,反应中转移______mole-。
(2)在一恒容的密闭容器中,由CO和H2合成甲醇:CO(g)+2H2(g)
 CH3OH(g)
CH3OH(g)①下列情形能说明上述反应已达到平衡状态的是_______
a.体系压强保持不变
b.密闭容器中CO、H2、CH3OH(g)3种气体共存
c.CH3OH与H2物质的量之比为1:2
d.每消耗1 mol CO的同时生成2molH2
②CO的平衡转化率(α)与温度、压强的关系如图所示。

A、B两点的平衡常数_____(填“前者”、“后者”或“一样”)大;达到A、C两点的平衡状态所需的时间tA tC(填“大于”、“小于”或“等于”)。
在不改变反应物用量的情况下,为提高CO的转化率可采取的措施是_____________(答出两点即可)。
(3)工作温度650℃的熔融盐燃料电池,是用煤炭气(CO、H2)作负极燃气,空气与CO2的混合气体为正极燃气,用一定比例的Li2CO3和Na2CO3低熔点混合物做电解质,以金属镍(燃料极)为催化剂制成的。负极的电极反应式为:CO + H2-4e- + 2CO32-= 3CO2+H2O;则该电池的正极反应式为____________。
I.煤化工中常需研究不同溫度下平衡常数、投料比等问题。
已知:CO (g) +H2O(g) H2 (g) +CO2
(g)平衡常数K随温度的变化如下表:
H2 (g) +CO2
(g)平衡常数K随温度的变化如下表:

回答下列问题
(1)该反应的平衡常数表达式K=______,ΔH=______0(填“<”、“>”、“=”)
(2)已知在一定温度下,CCs) +CO2 (g) 2C0
Cg)平衡常数K1;
2C0
Cg)平衡常数K1;
C (s)
+H2O (g) CO
Cg) +H2 (g)平衡常数K2
CO
Cg) +H2 (g)平衡常数K2
则K、K1 、K2,之间的关系是______:
(3)8000C时,向一个10L的恒容反应器中充入0.40molCO和1.60mol水蒸气,经一段时 间后反应达到平衡,此时CO的转化率为:若保持其他条件不变,向平衡体系中 再通入0.10molCO和0.40molCO2,此时v正 ______v逆 (填“>”、“=”或“<”)。
II.某小组利用H2C2O4溶液和酸性KMnO4溶液反应来探究“条件对化学反应速率的影响”。
(4) 向酸性KmnO4溶液中加入一定量的H2C2O4溶液,当溶液中的KmnO4耗尽后,紫色溶 液将褪去。为确保能观察到紫色褪去,H2C2O4与KmnO4初始的物质的量需要满足的关 系为n(H2C2O4): n(KMnO4) ______。
(5) 为探究反应物浓度对化学反应速率的影响,该小组设计了如下实验方案

表中x= ______ ml ,理由是______。
(6) 已知50°C时,浓度c(H2C2O4)随反应时间t的变化曲线如图示,若保持其他条件不变,请在答题卡坐标图 中画出25°C时c(H2C2O4)随t的变化曲线示意图。

查看习题详情和答案>>