网址:http://m.1010jiajiao.com/timu3_id_430431[举报]
已知2X2(g)+Y2(g) 2Z(g) ΔH=-akJ·mol-1(a>0),在一个容积固定的容器中加入2mol X2和1mol Y2在500℃时充分反应达平衡后Z的浓度为W mol·L-1,放出热量b kJ。
⑴此反应平衡常数表达式为______________;若将温度降低到300℃,则反应平衡常数将_____(填增大、减少或不变)。
⑵若原来容器中只加入2mol Z,500℃充分反应达平衡后,吸收热量c kJ,则Z浓度_______Wmol·L—1(填“>”、“<”或“=”),a、b、c之间满足关系___________(用代数式表示)。
⑶能说明反应已达平衡状态的是___________________。
| A.浓度c(Z)=2c(Y2) | B.容器内压强保持不变 | C.v逆(X2)=2v正(Y2) | D.容器内的密度保持不变 |
(6分)已知2X2(g)+Y2(g) 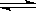 2Z(g) ΔH=-akJ·mol-1(a>0),在一个容积固定的容器中加入2mol X2和1mol Y2在500℃时充分反应达平衡后Z的浓度为W mol·L-1,放出热量b kJ。
2Z(g) ΔH=-akJ·mol-1(a>0),在一个容积固定的容器中加入2mol X2和1mol Y2在500℃时充分反应达平衡后Z的浓度为W mol·L-1,放出热量b kJ。
⑴此反应平衡常数表达式为____________ _;若将温度降低到300℃,则反应平衡常数将_____(填增大、减少或不变)。
⑵若原来容器中只加入2mol Z,500℃充分反应达平衡后,吸收热量c kJ,则Z浓度_______Wmol·L—1(填“>”、“<”或“=”),a、b、c之间满足关系______ _____(用代数式表示)。
⑶能说明反应已达平衡状态的是___________________。
| A.浓度c(Z)=2c(Y2) | B.容器内压强保持不变 |
| C.v逆(X2)=2v正(Y2) | D.容器内的密度保持不变 |
已知2X2(g)+Y2(g) = 2Z(g) ΔH=-akJ·mol-1(a>0),在一个容积固定的容器中加入2mol X2和1mol Y2,在500℃时充分反应达平衡后Z的浓度为W mol·L-1,放出热量b kJ。
⑴此反应平衡常数表达式为_________________;若将温度降低到300℃,则反应平衡常数将___________(填增大、减少或不变)。
⑵若原来容器中只加入2mol Z,500℃充分反应达平衡后,吸收热量c kJ,则Z浓度_______Wmol·L—1(填“>”、“<”或“=”),a、b、c之间满足关系___________(用代数式表示)。
⑶能说明反应已达平衡状态的是___________________。
| A.浓度c(Z)=2c(Y2) | B.容器内压强保持不变 |
| C.v逆(X2)=2v正(Y2) | D.容器内的密度保持不变 |
已知2X2(g)+Y2(g) = 2Z(g) ΔH=-akJ·mol-1(a>0),在一个容积固定的容器中加入2mol X2和1mol Y2,在500℃时充分反应达平衡后Z的浓度为W mol·L-1,放出热量b kJ。
⑴此反应平衡常数表达式为_________________;若将温度降低到300℃,则反应平衡常数将___________(填增大、减少或不变)。
⑵若原来容器中只加入2mol Z,500℃充分反应达平衡后,吸收热量c kJ,则Z浓度_______Wmol·L—1(填“>”、“<”或“=”),a、b、c之间满足关系___________(用代数式表示)。
⑶能说明反应已达平衡状态的是___________________。
A.浓度c(Z)=2c(Y2) B.容器内压强保持不变
C.v逆(X2)=2v正(Y2) D.容器内的密度保持不变
⑷若将上述容器改为恒压容器(反应器开始体积相同),相同温度下起始加入2mol X2和1mol Y2达到平衡后,Y2的转化率将_____(填“变大”、“变小”或“不变”)。
查看习题详情和答案>>
(6分)已知2X2(g)+Y2(g) 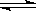 2Z(g) ΔH=-akJ·mol-1(a>0),在一个容积固定的容器中加入2mol X2和1mol Y2 在500℃时充分反应达平衡后Z的浓度为W mol·L-1,放出热量b kJ。
2Z(g) ΔH=-akJ·mol-1(a>0),在一个容积固定的容器中加入2mol X2和1mol Y2 在500℃时充分反应达平衡后Z的浓度为W mol·L-1,放出热量b kJ。
⑴ 此反应平衡常数表达式为____________ _;若将温度降低到300℃,则反应平衡常数将_____(填增大、减少或不变)。
⑵ 若原来容器中只加入2mol Z,500℃充分反应达平衡后,吸收热量c kJ,则Z浓度_______Wmol·L—1(填“>”、“<”或“=”),a、b、c之间满足关系______ _____(用代数式表示)。
⑶ 能说明反应已达平衡状态的是___________________。
A. 浓度c(Z)=2c(Y2) B. 容器内压强保持不变
C. v逆(X2)=2v正(Y2) D. 容器内的密度保持不变
⑷ 若将上述容器改为恒压容器(反应器开始体积相同),相同温度下起始加入2mol X2和1mol Y2达到平衡后,Y2的转化率将__ ___(填“变大”、“变小”或“不变”) 。
查看习题详情和答案>>