网址:http://m.1010jiajiao.com/timu3_id_429234[举报]
能正确表示下列反应的离子方程式是w.w.w.k.s.5.u.c.o.m
A.碳酸钙与盐酸反应 :CaCO3+2H+ ==Ca2+ +CO2↑+H2O
B.氯气与水反应:Cl2+H2O==2H+ +Cl- +ClO-
C.硫酸溶液与氢氧化钡溶液反应:Ba2++SO42-==BaSO4 ↓
D.金属铁放入稀硫酸中反应:2Fe + 6H+==2Fe3++ 3H2↑
查看习题详情和答案>>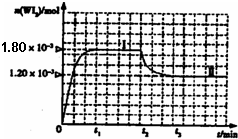 (2010?枣庄一模)卤素单质的性质活泼,卤素的化合物应用广泛,研究卤素单质及其化合物具有重要意义.
(2010?枣庄一模)卤素单质的性质活泼,卤素的化合物应用广泛,研究卤素单质及其化合物具有重要意义.(1)氯元素的原子结构示意图为


(2)二氧化氯(ClO2)是一种广泛用于水处理消毒剂,与Cl2相比,ClO2不但具有更显著的杀菌能力,而且不会产生对人体有害的有机氯化物.制备ClO2的方法有以下两种:
2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O…①
2NaClO2+H2O2+H2SO4=2C1O2↑+O2↑+Na2SO4+2H2O …②
你认为哪种方法最佳
(3)工业上用电解饱和食盐水的方法制取烧碱和氯气,请写出反应的离子方程式
| ||
| ||
(4)碘钨灯具有比白炽灯寿命长且环保节能的特点.一定温度下,灯泡内封存的少量碘与使用过程中沉积在管壁上的钨可以发生反应:W(s)+I2(g)
的密闭容器中,加热使其反应.如图是WI2(g)的物质的量随时间变化关系图象,其中曲线I(0~t2时间段)的反应温度为T1,曲线II(从t2开始)的反应温度为T2,且T2>T1.则:
①该反应的△H
②从反应开始到t1时间内的平均反应速率v(I2)=
| 0.036 |
| t1 |
| 0.036 |
| t1 |
③下列说法中不正确的是
A.该反应的平衡常数表达式是K=
| [WI2] |
| [W][I2] |
B.灯丝附近温度越高,灯丝附近区域WI2越易变为W而重新沉积到灯丝上
C.利用该反应原理可以提纯钨
(5)25℃时,向5mL含有KCl和KI浓度均为0.1mol/L的混合液中,滴加6mL0.1mol/L的AgNO3溶液,先生成的沉淀是
(6)Mg常用作提纯Ti的试剂,已知:
①Mg(s)+Cl2(g)=MgCl2(s)△H=-641kJ/mol
②Ti(s)+2Cl2(g)=TiCl4(l)△H=-770kJ/mol
请写出Mg与液态TiCl4反应提纯钛的热化学方程式
某研究性学习小组在网上收集到如下信息:Fe(NO3)3溶液可以蚀刻银,制作美丽的银饰。他们对蚀刻银的原因进行了如下探究:
[实验] 制备银镜,并与Fe(NO3)3溶液反应,发现银镜溶解。
(1)下列有关制备银镜过程的说法正确的是 。
a.边振荡盛有2%的AgNO3溶液的试管,边滴入2%的氨水。至最初的沉淀恰好溶解为止
b.将几滴银氨溶液滴入2 mL乙醛中
c.制备银镜时,用酒精灯的外焰给试管底部加热
d.银氨溶液具有较弱的氧化性
e.在银氨溶液配制过程中,溶液的pH增大
[提出假设]
假设1:Fe3+具有氧化性,能氧化Ag。W$w#w.k-s+5=u.c.o*m
假设2:Fe(NO3)3溶液显酸性,在此酸性条件下NO3— 能氧化Ag。
[设计实验方案,验证假设]
(2)甲同学从上述实验的生成物中检验出Fe3+,验证了假设1成立。请写出Fe3+氧化Ag的离子方程式: 。
(3)乙同学设计实验验证假设2,请帮他完成下表中内容(提示: NO![]() 在不同条件下的还原产物较复杂,有时难以观察到气体产生)。
在不同条件下的还原产物较复杂,有时难以观察到气体产生)。
| 实验步骤(不要求写具体操作过程) | 预期现象和结论 |
| ① ② …… | 若银镜消失,假设2成立。 若银镜不消失,假设2不成立。 |
[思考与交流]
(4)甲同学验证了假设1成立,若乙同学验证了假设2也成立。则丙同学由此得出结论:Fe(NO3)3溶液中的Fe3+和NO![]() 都氧化了Ag。
都氧化了Ag。
你是否同意丙同学的结论_ __ __,并简述理由: (用离子方程式表示)。
查看习题详情和答案>>X、Y、Z、W是元素周期表中原子序数依次增大的四种短周期元素,其相关信息如下表:
| 元素 | 相关信息 |
| X | X的最高价氧化物对应的水化物化学式为H2XO3 |
| Y | Y是地壳中含量最高的元素 |
| Z | Z的基态原子最外层电子排布式为3s23p1 |
| W | W的一种核素的质量数为28,中子数为14 |
| T | 常温常压下,T单质是淡黄色固体,常在火山口附近沉积 |
| P | P的价层电子排布为[Ar]3d104s2 |
(2)TY2中心原子的杂化方式为_______;XY2中一个分子周围有__________个紧邻分子;堆积方式与XY2晶胞类型相同的金属有_________(从“Cu、 Mg、K、Po”中选出正确的),其空间利用率为_______。
(3)Z的第一电离能比Mg的________(填“大”或“小”);写出Z单质与NaOH溶液反应的化学方程式 。
(4)写出W的最高价氧化物与NaOH溶液反应的离子方程式 ;W的最高价氧化物与XY2的熔点较高的是 ,原因是 。
(5)处理含XO、TO2烟道气污染的一种方法,是将其在催化剂作用下转化为单质T。已知:
① XO(g)+ 1/2O2(g)=XO2(g) ΔH="-283.0" kJ·mol-1 ② T(s)+O2(g)=TO2(g) ΔH="-296.0" kJ·mol-1
此反应的热化学方程式是______________________________。
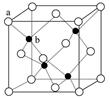
(6)P在周期表的 区;P和T形成的化合物PT在荧光体、光导体材料、涂料、颜料等行业中应用广泛。立方PT晶体结构如下图所示,其晶胞边长为540.0 pm,密度为_________ g·cm-3(列式并计算)。
 查看习题详情和答案>>
查看习题详情和答案>>