摘要: 可以判断NaHCO3 粉末中混有Na2CO3的实验方法是 A.加热时有无气体放出 B.滴加盐酸时有无气体放出 C.溶于水后滴加BaCl2有无沉淀 D.溶于水后滴加澄清的石灰水.有白色沉淀
网址:http://m.1010jiajiao.com/timu3_id_427483[举报]
(1)写出Fe2(SO4)3在水溶液中的电离方程式:
(2)写出下列离子方程式对应的一个化学方程式:2H++CO32-=H2O+CO2↑
(3)用“双线桥法”标明电子转移的方向和数目.
MnO2+4HCl
MnCl2+Cl2↑+2H2O
该反应中氧化剂与还原剂物质的量之比为
该反应的离子方程式为
(4)根据下列四个反应:
①Cl2+2KI=2KCl+I2 ②2FeCl2+Cl2=2FeCl3
③2FeCl3+2HI=2FeCl2+2HCl+I2 ④H2S+I2=S+2HI
可以判断FeCl3、Cl2、I2、S四种物质的氧化性由强到弱的正确顺序是
查看习题详情和答案>>
Fe2(SO4)3=2Fe2++3SO42-
Fe2(SO4)3=2Fe2++3SO42-
(2)写出下列离子方程式对应的一个化学方程式:2H++CO32-=H2O+CO2↑
HCl+NaHCO3-=H2O+NaCl+CO2↑
HCl+NaHCO3-=H2O+NaCl+CO2↑
(3)用“双线桥法”标明电子转移的方向和数目.
MnO2+4HCl
| ||
该反应中氧化剂与还原剂物质的量之比为
1:2
1:2
该反应的离子方程式为
MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O
| ||
MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O
| ||
(4)根据下列四个反应:
①Cl2+2KI=2KCl+I2 ②2FeCl2+Cl2=2FeCl3
③2FeCl3+2HI=2FeCl2+2HCl+I2 ④H2S+I2=S+2HI
可以判断FeCl3、Cl2、I2、S四种物质的氧化性由强到弱的正确顺序是
Cl2>FeCl3>I2>S
Cl2>FeCl3>I2>S
.Ⅰ电离平衡常数(用K表示)的大小可以判断电解质的相对强弱.25℃时,有关物质的电离平衡常数如下表所示:
(1)物质的量浓度均为0.1mol/L的下列四种溶液:①Na2CO3溶液 ②NaHCO3溶液 ③NaF溶液 ④NaClO溶液.依据数据判断pH由大到小的顺序是 .
(2)25℃时,在20mL0.1mol?L-1氢氟酸中加入VmL0.1mol?L-1NaOH溶液,测得混合溶液的pH变化曲线如图所示 ,下列说法正确的是 .
,下列说法正确的是 .
A.pH=3的HF溶液和pH=11的NaF溶液中,由水电离出的c(H+)相等
B.①点时pH=6,此时溶液中,c(F-)-c(Na+)=9.9×10-7mol/L
C.②点时,溶液中的c(F-)=c(Na+)
D.③点时V=20mL,此时溶液中c(F-)<c(Na+)=0.1mol?L-1
(3)已知25℃时,①HF(aq)+OH-(aq)=F-(aq)+H2O(l)△H=-akJ?mol-1,
②H+(aq)+OH-(aq)=H2O(l)△H=-bkJ?mol-1,
氢氟酸的电离方程式及热效应可表示为 .
(4)长期以来,一直认为氟的含氧酸不存在.1971年美国科学家用氟气通过细冰末时获得HFO,其结构式为H-O-F.HFO与等物质的量的H2O反应得到HF和化合物A,则每生成1molHF转移 mol电子.
Ⅱ氯化硫酰(SO2Cl2)主要用作氯化剂.它是一种无色液体,熔点-54.1℃,沸点69.1℃.氯化硫酰可用干燥的二氧化硫和氯气在活性炭催化剂存在下反应制取:
SO2(g)+Cl2(g) SO2Cl2(l)△H=-97.3kJ?mol-1
SO2Cl2(l)△H=-97.3kJ?mol-1
(1)试写出常温常压下化学平衡常数K的表达式:K= ;
(2)对上述反应,若要使化学平衡常数K增大,化学反应速率v正也增大,可采取的措施是 (选填编号).
a.降低温度 b.移走SO2Cl2
c.增加反应物浓度 d.无法满足上述条件
(3)下列描述中能说明上述反应已达平衡的是 (选填编号).
a.υ(Cl2)=υ(SO2) b.容器中气体压强不随时间而变化
c.c(Cl2):c(SO2)=1:1 d.容器中气体颜色不随时间两变化
(4)300℃时,体积为1L的密闭容器中充入16.20g SO2Cl2,达到平衡时容器中含SO2 7.616g.若在上述中的平衡体系中,再加入16.20g SO2Cl2,当再次达平衡时,容器中含SO2的质量范围是 .
查看习题详情和答案>>
| 化学式 | HF | H2CO3 | HClO |
| 电离平衡常数 (K) |
7.2×10-4 | K1=4.4×10-7 K2=4.7×10-11 |
3.0×10-8 |
(2)25℃时,在20mL0.1mol?L-1氢氟酸中加入VmL0.1mol?L-1NaOH溶液,测得混合溶液的pH变化曲线如图所示
 ,下列说法正确的是
,下列说法正确的是A.pH=3的HF溶液和pH=11的NaF溶液中,由水电离出的c(H+)相等
B.①点时pH=6,此时溶液中,c(F-)-c(Na+)=9.9×10-7mol/L
C.②点时,溶液中的c(F-)=c(Na+)
D.③点时V=20mL,此时溶液中c(F-)<c(Na+)=0.1mol?L-1
(3)已知25℃时,①HF(aq)+OH-(aq)=F-(aq)+H2O(l)△H=-akJ?mol-1,
②H+(aq)+OH-(aq)=H2O(l)△H=-bkJ?mol-1,
氢氟酸的电离方程式及热效应可表示为
(4)长期以来,一直认为氟的含氧酸不存在.1971年美国科学家用氟气通过细冰末时获得HFO,其结构式为H-O-F.HFO与等物质的量的H2O反应得到HF和化合物A,则每生成1molHF转移
Ⅱ氯化硫酰(SO2Cl2)主要用作氯化剂.它是一种无色液体,熔点-54.1℃,沸点69.1℃.氯化硫酰可用干燥的二氧化硫和氯气在活性炭催化剂存在下反应制取:
SO2(g)+Cl2(g)
 SO2Cl2(l)△H=-97.3kJ?mol-1
SO2Cl2(l)△H=-97.3kJ?mol-1(1)试写出常温常压下化学平衡常数K的表达式:K=
(2)对上述反应,若要使化学平衡常数K增大,化学反应速率v正也增大,可采取的措施是
a.降低温度 b.移走SO2Cl2
c.增加反应物浓度 d.无法满足上述条件
(3)下列描述中能说明上述反应已达平衡的是
a.υ(Cl2)=υ(SO2) b.容器中气体压强不随时间而变化
c.c(Cl2):c(SO2)=1:1 d.容器中气体颜色不随时间两变化
(4)300℃时,体积为1L的密闭容器中充入16.20g SO2Cl2,达到平衡时容器中含SO2 7.616g.若在上述中的平衡体系中,再加入16.20g SO2Cl2,当再次达平衡时,容器中含SO2的质量范围是
10℃时,在烧杯中加入0.1mol/L的NaHCO3溶液400mL,加热,测得该溶液的PH发生如下变化:
(1)甲同学认为,该溶液的pH升高的原因是HCO3-的水解程度增大,故碱性增强,该反应的离子方程式为: ;
(2)乙同学认为,溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度 (填“大于”或“小于”)NaHCO3;
(3)丙同学认为,要确定上述哪种说法合理,只要把加热后的溶液冷却到10℃后再测定溶液pH,若pH 8.3(填“>”、“<”或“=”),说明乙正确;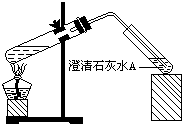
(4)丁同学设计如下实验方案对甲、乙同学的解释进行判断:实验装置如图,加热煮沸NaHCO3溶液,发现试管A中产生沉淀,说明 (填“甲”或“乙”)推断正确;
(5)将一定体积0.1mol/L的NaHCO3溶液置于烧杯中加热至微沸(溶液体积不变),测其pH为10.4;将烧杯冷却至室温,过一段时间(溶液体积不变)测得pH为9.5.据此资料可以判断 (填“甲”或“乙”)推测正确,原因是 .
查看习题详情和答案>>
| 温度(℃) | 10 | 20 | 30 | 40 | 70 |
| pH | 8.3 | 8.4 | 8.5 | 8.9 | 9.4 |
(2)乙同学认为,溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度
(3)丙同学认为,要确定上述哪种说法合理,只要把加热后的溶液冷却到10℃后再测定溶液pH,若pH

(4)丁同学设计如下实验方案对甲、乙同学的解释进行判断:实验装置如图,加热煮沸NaHCO3溶液,发现试管A中产生沉淀,说明
(5)将一定体积0.1mol/L的NaHCO3溶液置于烧杯中加热至微沸(溶液体积不变),测其pH为10.4;将烧杯冷却至室温,过一段时间(溶液体积不变)测得pH为9.5.据此资料可以判断
 (2012?深圳二模)NaCl和NaClO在酸性条件下可发生反应:ClO-+Cl-+2H+=Cl2↑+H2O,某学习小组拟研究消毒液(主要成分为NaCl和NaClO)的变质情况.
(2012?深圳二模)NaCl和NaClO在酸性条件下可发生反应:ClO-+Cl-+2H+=Cl2↑+H2O,某学习小组拟研究消毒液(主要成分为NaCl和NaClO)的变质情况.(1)此消毒液可吸收空气中的CO2生成NaHCO3而变质.写出化学反应方程式
NaClO+CO2+H2O=NaHCO3+HClO
NaClO+CO2+H2O=NaHCO3+HClO
.(2)取适量消毒液放在试管中,加入足量一定浓度的硫酸,有气体放出.通过以下装置检验气体的成分可以判断消毒液是否变质.
限选试剂:98%浓硫酸、1%品红溶液、1.0mol?L-1 KI-淀粉溶液、1.0mol?L-1NaOH、澄清石灰水、饱和NaCl溶液
请完成下列实验方案.
| 所加试剂 | 预期现象和结论 |
| 试管A中加足量① 1.0mol/LK淀 粉溶液 1.0mol/LK淀 ;粉溶液 试管B中加1%品红溶液; 试管C中加② 澄清石灰水 澄清石灰水 . |
若A中溶液变蓝色,B中溶液不退色,C中溶液变浑浊.则消毒液部分变质; ③ 若A中溶液变蓝色,B中溶液不退色 (无变化),C中溶液不变浑浊(无变化),则 消毒液未变质 若A中溶液变蓝色,B中溶液不退色 则消毒液未变质;(无变化),C中溶液不变浑浊(无变化),则 消毒液未变质 ④ 若A中溶液不变蓝色(无变化),B中溶 液不退色(无变化),C中溶液变浑浊则消 毒液完全变质 若A中溶液不变蓝色(无变化),B中溶 则消毒液完全变质.液不退色(无变化),C中溶液变浑浊则消 毒液完全变质 |
①量取25.00mL消毒液放入锥形瓶中,加入过量的a mol?L-1Na2SO3溶液b mL;
②滴定分析.将c mol?L-1的酸性KMnO4溶液装入
酸式
酸式
(填酸式或碱式)滴定管中;KMnO4和剩余的Na2SO3发生反应.当溶液由无色变成浅红色,且保持半分钟内红色不退时,停止滴定,记录数据.重复滴定实验2次,平均消耗酸性KMnO4溶液v mL;滴定过程中涉及的反应有:NaClO+Na2SO3=NaCl+Na2SO4;2KMnO4+5Na2SO3+3H2SO4=K2SO4+2MnSO4+5Na2SO4+3H2O.
③计算.消毒液中NaClO的浓度为
| (2ab-5vc) |
| 50 |
| (2ab-5vc) |
| 50 |
(2013?江苏三模)乙酰基二茂铁是常用的汽油的抗震剂,由二茂铁合成乙酰基二茂铁的原理如下:
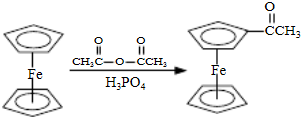
其实验步骤如下:
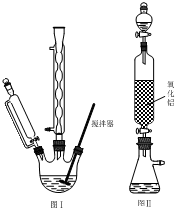 步骤1:如图Ⅰ所示,取1g二茂铁与3mL乙酸酐于装置中,开通搅拌器,慢慢滴加85%磷酸1mL,加热回流5min.
步骤1:如图Ⅰ所示,取1g二茂铁与3mL乙酸酐于装置中,开通搅拌器,慢慢滴加85%磷酸1mL,加热回流5min.
步骤2:待反应液冷却后,倒入烧杯中加入10g碎冰,搅拌至冰全部融化,缓慢滴加NaHCO3溶液中和至中性,置于冰水浴中15min.抽滤,烘干,得到乙酰基二茂铁粗产品.
步骤3:将乙酰基二茂铁粗产品溶解在苯中,从图Ⅱ装置的分液漏斗中滴下,再用乙醚淋洗.
步骤4:将其中一段时间的淋洗液收集,并进行操作X,得到纯净的针状晶体乙酰基二茂铁并回收乙醚.
(1)步骤2中的抽滤操作,除烧杯、玻璃棒外,还必须使用属于硅酸盐材质的仪器有
(2)步骤2中不需要测定溶液的pH就可以判断溶液接近中性,其现象是
(3)步骤3将粗产品中杂质分离实验的原理是
(4)步骤4中操作X的名称是
(5)为确定产品乙酰基二茂铁中是否含有杂质二乙酰基二茂铁(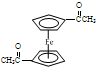 ),可以使用的仪器分析方法是
),可以使用的仪器分析方法是
查看习题详情和答案>>

其实验步骤如下:
 步骤1:如图Ⅰ所示,取1g二茂铁与3mL乙酸酐于装置中,开通搅拌器,慢慢滴加85%磷酸1mL,加热回流5min.
步骤1:如图Ⅰ所示,取1g二茂铁与3mL乙酸酐于装置中,开通搅拌器,慢慢滴加85%磷酸1mL,加热回流5min.步骤2:待反应液冷却后,倒入烧杯中加入10g碎冰,搅拌至冰全部融化,缓慢滴加NaHCO3溶液中和至中性,置于冰水浴中15min.抽滤,烘干,得到乙酰基二茂铁粗产品.
步骤3:将乙酰基二茂铁粗产品溶解在苯中,从图Ⅱ装置的分液漏斗中滴下,再用乙醚淋洗.
步骤4:将其中一段时间的淋洗液收集,并进行操作X,得到纯净的针状晶体乙酰基二茂铁并回收乙醚.
(1)步骤2中的抽滤操作,除烧杯、玻璃棒外,还必须使用属于硅酸盐材质的仪器有
布氏漏斗、抽滤瓶
布氏漏斗、抽滤瓶
.(2)步骤2中不需要测定溶液的pH就可以判断溶液接近中性,其现象是
滴加NaHCO3溶液不再产生气泡
滴加NaHCO3溶液不再产生气泡
.(3)步骤3将粗产品中杂质分离实验的原理是
不同物质在扩散剂中扩散的速率不同
不同物质在扩散剂中扩散的速率不同
.(4)步骤4中操作X的名称是
蒸馏
蒸馏
,该操作中不能使用明火的原因是乙醚易挥发且易燃
乙醚易挥发且易燃
.(5)为确定产品乙酰基二茂铁中是否含有杂质二乙酰基二茂铁(
 ),可以使用的仪器分析方法是
),可以使用的仪器分析方法是质谱法或核磁共振氢谱
质谱法或核磁共振氢谱
.