摘要:要重视重要题型的研究和讲解.最起码要让学生知道有这类题型.了解解此类题的基本方法.
网址:http://m.1010jiajiao.com/timu3_id_420302[举报]
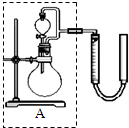 过氧化氢对环境友好,性质多样,有很重要的研究和应用价值.
过氧化氢对环境友好,性质多样,有很重要的研究和应用价值.实验室利用反应2H2O2
| ||
| 序号 | 条件 | 现象 | 结论 | |
| 温度/℃ | 催化剂 | |||
| 1 | 40 | FeCl3溶液 | ||
| 2 | 20 | FeCl3溶液 | ||
| 3 | 20 | MnO2 | ||
| 4 | 20 | 无 | ||
温度
温度
对H2O2分解速率的影响.实验2、3的目的是
比较FeCl3溶液和MnO2作为催化剂对H2O2分解反应速率影响的差异
比较FeCl3溶液和MnO2作为催化剂对H2O2分解反应速率影响的差异
实验中可以表明该反应速率差异的现象是
产生气泡的快慢
产生气泡的快慢
②实验室用MnO2做该反应的催化剂,使用如图所示装置的A部分制备O2,避免反应过于剧烈的操作是
旋转分液漏斗的活塞,控制滴加H2O2溶液的速率
旋转分液漏斗的活塞,控制滴加H2O2溶液的速率
.对溶液的研究和认识,在生产、生活和科研领域具有重要意义.
(1)现有一种含有弱酸HA和其钠盐NaA的溶液,请回答下列问题:
①组成该溶液的微观粒子有 .
②若向该溶液中加入少量盐酸时,发生反应的离子方程式是 ;
③若向该溶液中逐滴加入KOH溶液时,下列图象能表示Aˉ离子数目变化趋势的是 ;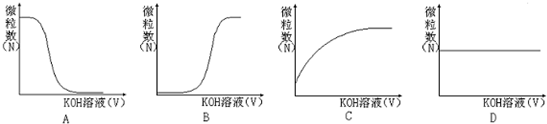
④现将1体积0.04mol?L-1HA溶液和1体积0.02mol?L-1NaOH溶液混合,得到2体积混合溶液.若该混合液显碱性,则其c(A-) 0.01mol?L-1(填“<”、“=”或“>”);若该混合液显酸性,溶液中所有离子的浓度由大到小的顺序是 .
(2)血液里含有的H2CO3和NaHCO3,与上述情况相似,对保持血液pH的稳定起到重要作用.
当c(H+)增大时,血液中消耗H+的离子方程式为 ;
当c(OH-)增大时,血液的pH也能保持基本稳定,试结合离子方程式简要说明 .
查看习题详情和答案>>
(1)现有一种含有弱酸HA和其钠盐NaA的溶液,请回答下列问题:
①组成该溶液的微观粒子有
②若向该溶液中加入少量盐酸时,发生反应的离子方程式是
③若向该溶液中逐滴加入KOH溶液时,下列图象能表示Aˉ离子数目变化趋势的是

④现将1体积0.04mol?L-1HA溶液和1体积0.02mol?L-1NaOH溶液混合,得到2体积混合溶液.若该混合液显碱性,则其c(A-)
(2)血液里含有的H2CO3和NaHCO3,与上述情况相似,对保持血液pH的稳定起到重要作用.
当c(H+)增大时,血液中消耗H+的离子方程式为
当c(OH-)增大时,血液的pH也能保持基本稳定,试结合离子方程式简要说明
海洋约占地球表面积的71%,海水化学资源的利用具有非常广阔的前景.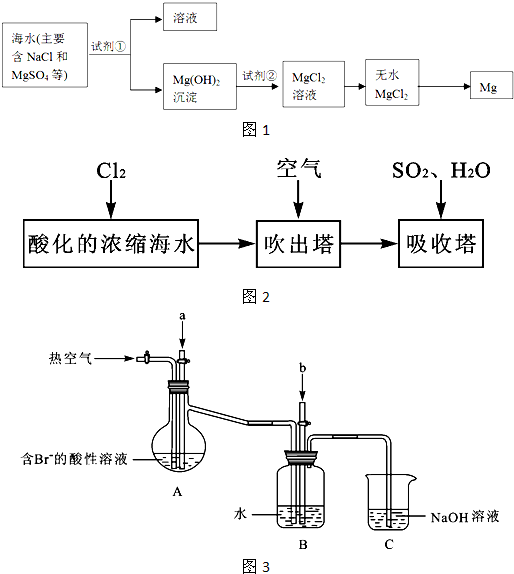
(1)海水晒盐可获得粗盐,在实验室中粗盐经过溶解、
(2)镁及其合金是一种用途很广的金属材料,目前世界上60%的镁是从海水中提取的,其主要步骤如图1所示:
①为了使MgSO4转化为Mg(OH)2,试剂①可以选用
②试剂②可以选用
③试从节约能源、提高金属镁的纯度分析,以下适宜的冶镁方法是
A.Mg(OH)2
MgO
Mg
B.Mg(OH)2
MgO
Mg
C.Mg(OH)2
MgCl2
Mg
D.Mg(OH)2
MgCl2
Mg
(3)溴及其化合物用途十分广泛,我国正在大力开展海水提溴的研究和开发工作.工业以浓缩海水为原料提取溴的部分过程如图2所示.
某课外小组在实验室模拟上述过程设计如图3所示装置进行实验(所有橡胶制品均已被保护,夹持装置已略去):
①A装置中通入a气体的目的是(用离子方程式表示)
②A装置中通入a气体一段时间后,停止通入,改通热空气.通入热空气的目的是
③反应过程中,B装置中有SO42-生成.检验SO42-的方法是
④C装置的作用是
查看习题详情和答案>>

(1)海水晒盐可获得粗盐,在实验室中粗盐经过溶解、
过滤
过滤
、蒸发
蒸发
可制得精盐.(2)镁及其合金是一种用途很广的金属材料,目前世界上60%的镁是从海水中提取的,其主要步骤如图1所示:
①为了使MgSO4转化为Mg(OH)2,试剂①可以选用
氢氧化钠(NaOH)
氢氧化钠(NaOH)
,要使MgSO4完全转化为沉淀,加入试剂①的量应过量
过量
;②试剂②可以选用
盐酸
盐酸
;③试从节约能源、提高金属镁的纯度分析,以下适宜的冶镁方法是
C
C
.A.Mg(OH)2
| △ |
| 电解 |
| 2800℃ |
B.Mg(OH)2
| △ |
| C |
| 还原 |
C.Mg(OH)2
| HCl |
| ||
| 714℃ |
D.Mg(OH)2
| HCl |
| 活泼金属 |
| 还原 |
(3)溴及其化合物用途十分广泛,我国正在大力开展海水提溴的研究和开发工作.工业以浓缩海水为原料提取溴的部分过程如图2所示.
某课外小组在实验室模拟上述过程设计如图3所示装置进行实验(所有橡胶制品均已被保护,夹持装置已略去):
①A装置中通入a气体的目的是(用离子方程式表示)
Cl2+2Br-=2Cl-+Br2
Cl2+2Br-=2Cl-+Br2
;②A装置中通入a气体一段时间后,停止通入,改通热空气.通入热空气的目的是
吹出Br2
吹出Br2
;③反应过程中,B装置中有SO42-生成.检验SO42-的方法是
取少量B装置中反应后的溶液于试管中,滴加氯化钡溶液,产生白色沉淀,证明有SO42-
取少量B装置中反应后的溶液于试管中,滴加氯化钡溶液,产生白色沉淀,证明有SO42-
;④C装置的作用是
吸收未反应的Cl2、Br2和SO2
吸收未反应的Cl2、Br2和SO2
. 能源是人类生存和发展的重要支柱.研究和有效地开发新能源在能源紧缺的今天具有重要的理论意义.
能源是人类生存和发展的重要支柱.研究和有效地开发新能源在能源紧缺的今天具有重要的理论意义.(1)已知下列热化学方程式:
①H2(g)+
| 1 |
| 2 |
②C(s)+
| 1 |
| 2 |
则水煤气能源的制取原理:C(s)+H2O(g)=H2(g)+CO(g)△H=
131.3
131.3
kJ/moL(2)研究活化能对于能源技术的革新有非常重大的实际意义.请认真观察下图,回答问题:
①图中反应的△H=
E2-E1
E2-E1
kJ/mol(用含有E1、E2代数式表示).②已知热化学方程式:H2(g)+
| 1 |
| 2 |
409.0
409.0
kJ/mol.③图中虚线(Ⅱ)与实线(Ⅰ)对于同一反应具有的意义:
使用了催化剂
使用了催化剂
.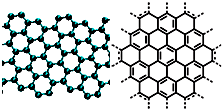 A.美国《科学》杂志评出的2009年十大科学突破之一是石墨烯的研究和应用方面的突破.石墨烯具有原子级的厚度、优异的电学性能、出色的化学稳定性和热力学稳定性.制备石墨烯方法有石墨剥离法、化学气相沉积法等.石墨烯的球棍模型及分子结构示意图如右:
A.美国《科学》杂志评出的2009年十大科学突破之一是石墨烯的研究和应用方面的突破.石墨烯具有原子级的厚度、优异的电学性能、出色的化学稳定性和热力学稳定性.制备石墨烯方法有石墨剥离法、化学气相沉积法等.石墨烯的球棍模型及分子结构示意图如右:(1)下列有关石墨烯说法正确的是
BD
BD
.A.石墨烯的结构与金刚石相似
B.石墨烯分子中所有原子可以处于同一平面
C.12g石墨烯含σ键数为NA
D.从石墨剥离得石墨烯需克服石墨层与层之间的分子间作用
(2)化学气相沉积法是获得大量石墨烯的有效方法之一,催化剂为金、铜、钴等金属或合金,含碳源可以是甲烷、乙炔、苯、乙醇或酞菁等中的一种或任意组合.
①钴原子在基态时,核外电子排布式为:
[Ar]3d74s2
[Ar]3d74s2
.
②乙醇沸点比氯乙烷高,主要原因是
乙醇分子间可形成氢键,而氯乙烷分子间无氢键
乙醇分子间可形成氢键,而氯乙烷分子间无氢键
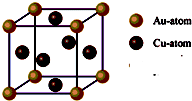
.③右图是金与铜形成的金属互化物合金,它的化学式可表示为:
Cu3Au或AuCu3
Cu3Au或AuCu3
.④含碳源中属于非极性分子的是
a、b、c
a、b、c
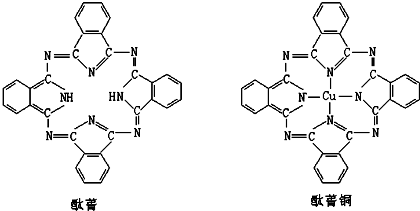
(a.甲烷 b.乙炔 c.苯 d.乙醇)⑤酞菁与酞菁铜染料分子结构如下图,酞菁分子中氮原子采用的杂化方式有:
sp3和sp2
sp3和sp2
;酞菁铜分子中心离子的配位数为:2
2
.
B.硫酸钾是重要的化工产品,生产方法很多,如曼海姆法、石膏两步转化法等.
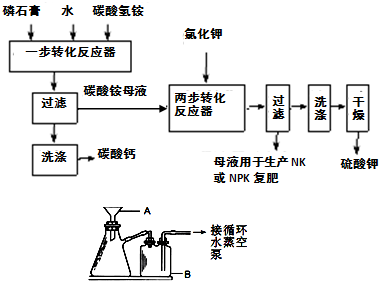
(1)本实验中,采用抽滤方法,图中A、B两仪器名称分别为:
布氏漏斗
布氏漏斗
、安全瓶
安全瓶
.(2)在一部转化反应器中发生的反应为:CaSO4?2H2O+2NH4HCO3=(NH4)2SO4+CaCO3+CO2↑+3H2O,该步反应温度必须低于35℃,其主要目的是
防止NH4HCO3分解
防止NH4HCO3分解
无此空
无此空
.(3)在两步转化反应器中发生反应的化学方程式为
(NH4)2SO4+2KCl=K2SO4+2NH4Cl
(NH4)2SO4+2KCl=K2SO4+2NH4Cl
无此空
无此空
.(4)两步转化反应器中用乙二醇代替水作溶剂,其目的是
降低K2SO4溶解度
降低K2SO4溶解度
有利于K2SO4析出,提高产率
有利于K2SO4析出,提高产率
.(5)磷石膏主要成分为二水硫酸钙(CaSO4?2H2O),还含有未分解的磷矿,未洗涤干净的磷酸、氟化钙、铁铝氧化物等,欲检验母液中含Fe3+,可用亚铁氰化钾溶液检验,该检验反应的离子方程式为:
Fe3++K++[Fe(CN)6]4-=KFe[Fe(CN)6]↓
Fe3++K++[Fe(CN)6]4-=KFe[Fe(CN)6]↓
.(6)该法优点除K2SO4产率高外,再列举一个优点
原料得到充分利用
原料得到充分利用
同时得到副产品化肥等
同时得到副产品化肥等
.