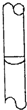
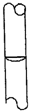
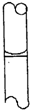
摘要: (本题包括2个小题.共16分) Ⅰ.. 一定物质的量浓度溶液的配制和酸碱中和滴定是中学化学中两个典型的定量实验.某研究性学习小组在实验室中配制1mol/L的稀硫酸标准溶液.然后用其滴定某未知浓度的NaOH溶液.下列有关说法中正确的是 A.实验中所用到的滴定管.容量瓶.在使用前均需要检漏, B.如果实验中需用60mL 的稀硫酸标准溶液.配制时应选用100mL容量瓶, C.容量瓶中含有少量蒸馏水.会导致所配标准溶液的浓度偏小, D.酸式滴定管用蒸馏水洗涤后.即装入标准浓度的稀硫酸.则测得的NaOH溶液的浓度将偏大, E.用甲基橙作指示剂.滴定终点时.溶液颜色从橙色变为红色, F.配制溶液和中和滴定的两个实验中.若在最后一次读数均俯视读数.则导致实验结果都偏大. Ⅱ . 现用如图所示的装置制取较多量的饱和氯水并测定饱和氯水的pH. 回答有关问题: (1)写出有关化学方程式. 装置甲: , 装置丁: . (2)证明氯水已饱和的现象是 . (3)制取结束时.装置丙的液体中含有的微粒是 , (4)有如下改进措施或建议.请作出评价: ①在装置乙和丙之间增加如图(a)所示的装置.你认为有无必要? . ②在装置丙的长导管下口处.接如图(b)所示的多孔球泡.这样做的好处是: . ③若撤去装置乙.直接将装置甲和丙相连.这样做对实验结果的影响是: .
网址:http://m.1010jiajiao.com/timu3_id_417162[举报]
将甲烷和氧气按一定物质的量之比混合点燃后,测得生成物总质量为18.4g,将全部生成物通过足量浓硫酸后,质量减少了9g.
(1)通过计算可得出原混合气体中甲烷的物质的量为
(2)通过对(1)计算结果的进一步分析,可推知原混合气体反应后的生成物应为
(3)求原混合气体中甲烷和氧气的物质的量之比(写出详细的计算过程).
查看习题详情和答案>>
(1)通过计算可得出原混合气体中甲烷的物质的量为
0.25
0.25
mol.(2)通过对(1)计算结果的进一步分析,可推知原混合气体反应后的生成物应为
CO2、CO
CO2、CO
和水组成的混合物(填化学式).(3)求原混合气体中甲烷和氧气的物质的量之比(写出详细的计算过程).
在花瓶中加入“鲜花保鲜剂”,能延长鲜花的寿命.下表是500mL“鲜花保鲜剂”中含有的成分,阅读后回答下列问题:
(1)下列“鲜花保鲜剂”的成分中,属于电解质且是常见的强氧化剂的是
A.硝酸银 B.高锰酸钾 C.硫酸钾 D.蔗糖
(2)“鲜花保鲜剂”中K+(阿司匹林中不含K+)的物质的量浓度为
(3)在配制一定物质的量浓度的溶液时,可分为以下几个步骤:①称量②计算 ③溶解④摇匀 ⑤转移 ⑥洗涤 ⑦定容 ⑧冷却.其正确的操作顺序为
(4)配制上述500mL“鲜花保鲜剂”所需的仪器有:托盘天平、烧杯、玻璃棒、药匙、
(5)在溶液配制过程中,下列操作造成K+的物质的量浓度偏高的是
A.定容时俯视刻度线
B.容量瓶在使用前未干燥,里面有少量蒸馏水
C.容量瓶在使用前刚刚配制完一定物质的量浓度的KCl溶液而未洗净
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理.
查看习题详情和答案>>
| 成分 | 质量(g) | 摩尔质量(g?mol-1) |
| 蔗糖 | 25.0 | 342 |
| 硫酸钾 | 0.435 | 174 |
| 阿司匹林 | 0.4 | 180 |
| 高锰酸钾 | 0.237 | 158 |
| 硝酸银 | 0.2 | 170 |
B
B
(填序号)A.硝酸银 B.高锰酸钾 C.硫酸钾 D.蔗糖
(2)“鲜花保鲜剂”中K+(阿司匹林中不含K+)的物质的量浓度为
0.013
0.013
mol?L-1.(3)在配制一定物质的量浓度的溶液时,可分为以下几个步骤:①称量②计算 ③溶解④摇匀 ⑤转移 ⑥洗涤 ⑦定容 ⑧冷却.其正确的操作顺序为
②①③⑧⑤⑥⑤⑦④
②①③⑧⑤⑥⑤⑦④
.(4)配制上述500mL“鲜花保鲜剂”所需的仪器有:托盘天平、烧杯、玻璃棒、药匙、
500mL容量瓶
500mL容量瓶
、胶头滴管
胶头滴管
.(在横线上填写所缺仪器的名称).(5)在溶液配制过程中,下列操作造成K+的物质的量浓度偏高的是
AC
AC
.A.定容时俯视刻度线
B.容量瓶在使用前未干燥,里面有少量蒸馏水
C.容量瓶在使用前刚刚配制完一定物质的量浓度的KCl溶液而未洗净
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理.
玻璃棒在实验中一般有如下三种用途:搅拌、引流和蘸取溶液,下列实验中用到搅拌的是( )
①配制一定物质的量浓度的溶液
②粗盐提纯
③银镜反应检验醛基
④从制取氧气的剩余固体中提取KCl
⑤测定溶液的pH
⑥浓盐酸与浓氨水相遇发烟.
①配制一定物质的量浓度的溶液
②粗盐提纯
③银镜反应检验醛基
④从制取氧气的剩余固体中提取KCl
⑤测定溶液的pH
⑥浓盐酸与浓氨水相遇发烟.
| A、①②④ | B、②③④ | C、②④⑥ | D、全部 |
 (I)下列操作会导致实验结果偏高的是
(I)下列操作会导致实验结果偏高的是D
D
.A.配制一定物质的量浓度的硫酸溶液时,定容摇匀后,发现液面低于刻度线.
B.在配制一定物质的量浓度溶液时,用10ml的量筒量取5.0ml液体溶质时俯视读数
C.用天平称量20.5g某物质,砝码和药品的位置放反,所得药品的质量
D.10%的硫酸和90%的硫酸等体积混合配制50%的硫酸溶液
E.配制一定物质的量浓度溶液时,定容时仰视读数,所得溶液的浓度
(Ⅱ)现有下列仪器或用品:
a.铁架台(含铁圈、铁夹);b.锥形瓶;c.滴定管;d.烧杯(若干);e.玻璃棒;f.胶头滴管;g.托盘天平(含砝码);h.滤纸;i.量筒;j.漏斗;k.温度计.
试填空:
(1)如图所示分别是温度计、量筒、滴定管的一部分,下述判断及读数(虚线刻度)不正确的是
AD
AD
.A.①是量筒,读数为2.5mL
B.②是量筒,读数为2.5mL
C.③是滴定管,读数为2.50mL
D.②是温度计,读数是2.5℃
(2)用给出的仪器和NaOH固体配制一定物质的量浓度的氢氧化钠溶液时,还缺少的仪器有
钥匙、容量瓶
钥匙、容量瓶
;(3)用给出的仪器进行粗盐的提纯实验,还缺少的仪器有
蒸发皿、酒精灯
蒸发皿、酒精灯
.