摘要:(二) 实验程序设计
网址:http://m.1010jiajiao.com/timu3_id_41455[举报]
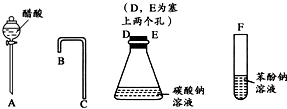
设计一个简单的一次性完成实验的装置,验证醋酸、二氧化碳水溶液(碳酸)和苯酚的酸性,其强弱的顺序是:CH3COOH>H2CO3>C6H5OH

(1)利用下列仪器可以组装实验装置,则仪器的连接顺序是:
(2)写出实验过程中发生反应的离子方程式.
查看习题详情和答案>>

(1)利用下列仪器可以组装实验装置,则仪器的连接顺序是:
ADEBCF
ADEBCF
.(2)写出实验过程中发生反应的离子方程式.
2CH3COOH+CO32-=2CH3COO-+H2O+CO2↑
2CH3COOH+CO32-=2CH3COO-+H2O+CO2↑
、H2O+CO2+C6H5O-→C6H5OH+HCO3-
H2O+CO2+C6H5O-→C6H5OH+HCO3-
. 实验室制取乙烯,常因温度过高而使乙醇和浓H2SO4反应生成少量的二氧化硫,有人设计下列实验以确定上述混合气体中有乙烯和二氧化硫.
实验室制取乙烯,常因温度过高而使乙醇和浓H2SO4反应生成少量的二氧化硫,有人设计下列实验以确定上述混合气体中有乙烯和二氧化硫.(1)实验室制取乙烯的化学方程式
CH3CH2OH
CH2=CH2↑+H2O
| 浓硫酸 |
| 170℃ |
CH3CH2OH
CH2=CH2↑+H2O
,反应类型为| 浓硫酸 |
| 170℃ |
消去反应
消去反应
.(2)Ⅰ、Ⅱ、Ⅲ、Ⅳ装置可盛放的试剂是Ⅰ
B
B
;ⅡC
C
;Ⅲ;B
B
ⅣA
A
.(将下列有关试剂的序号填入空格内)A.酸性KMnO4 B.品红溶液 C.NaOH溶液 D.浓H2SO4
(3)能说明二氧化硫气体存在的现象是
装置Ⅰ中的品红溶液褪色
装置Ⅰ中的品红溶液褪色
.(4)装置Ⅱ中开始反应时的离子方程式是
SO2+2OH-=SO32-+H2O
SO2+2OH-=SO32-+H2O
.(5)使用装置Ⅲ的目的是
检验SO2是否除尽
检验SO2是否除尽
.(6)确证含有乙烯的现象
Ⅲ中的品红不褪色,Ⅳ中的高锰酸钾溶液褪色
Ⅲ中的品红不褪色,Ⅳ中的高锰酸钾溶液褪色
.实验室用浓盐酸配制250mL0.1mol/L的盐酸溶液:☆
Ⅰ.(1)配制250mL0.1mol/L盐酸溶液需要浓盐酸(密度为1.2g/mL,质量分数为36.5%)的体积为
(2)配制时,其正确的操作顺序是(字母表示,每个字母只能用一次)
A.用30mL水洗涤烧杯2-3次,洗涤液均注入容量瓶,振荡
B.用量筒量取所需的浓盐酸,沿玻璃棒倒入烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入250mL的容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1-2cm处
(3)配制物质的量浓度的溶液,造成浓度偏高的操作是
A.溶解后的溶液未冷至室温就转入容量瓶中;
B.洗涤烧杯和玻棒的溶液未转入容量瓶中;
C.定容时眼睛俯视刻度线;
D.定容时眼睛仰视刻度线;
Ⅱ.(1)某学生设计的用该浓盐酸与二氧化锰反应制取并收集干燥纯净的氯气的装置如图:

①写出甲中发生反应的离子方程式:
②乙中盛的试剂是
丙中盛的试剂是
(2)如果将过量二氧化锰与20mL该浓盐酸混合加热,充分反应后理论上可生成标况下的氯气的体积为
①
(3)若将制得的少量氯气通入无色的饱和碘化钾溶液中,溶液变
(4)若将制得的氯气制成饱和氯水,则实验室保存饱和氯水的方法是
查看习题详情和答案>>
Ⅰ.(1)配制250mL0.1mol/L盐酸溶液需要浓盐酸(密度为1.2g/mL,质量分数为36.5%)的体积为
2.1mL
2.1mL
.(2)配制时,其正确的操作顺序是(字母表示,每个字母只能用一次)
BCAFED
BCAFED
.A.用30mL水洗涤烧杯2-3次,洗涤液均注入容量瓶,振荡
B.用量筒量取所需的浓盐酸,沿玻璃棒倒入烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入250mL的容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1-2cm处
(3)配制物质的量浓度的溶液,造成浓度偏高的操作是
AC
AC
.A.溶解后的溶液未冷至室温就转入容量瓶中;
B.洗涤烧杯和玻棒的溶液未转入容量瓶中;
C.定容时眼睛俯视刻度线;
D.定容时眼睛仰视刻度线;
Ⅱ.(1)某学生设计的用该浓盐酸与二氧化锰反应制取并收集干燥纯净的氯气的装置如图:

①写出甲中发生反应的离子方程式:
MnO2+4H++2Cl-=Mn2++Cl2↑+2H2O
MnO2+4H++2Cl-=Mn2++Cl2↑+2H2O
②乙中盛的试剂是
饱和NaCl溶液
饱和NaCl溶液
;作用是除去Cl2中混有的HCl气体
除去Cl2中混有的HCl气体
.丙中盛的试剂是
浓硫酸
浓硫酸
.(2)如果将过量二氧化锰与20mL该浓盐酸混合加热,充分反应后理论上可生成标况下的氯气的体积为
1344
1344
mL,而实际值明显少于理论值,其主要原因有:①
部分浓盐酸挥发了
部分浓盐酸挥发了
;②随着反应的进行浓盐酸变稀,稀盐酸不能被氧化成氯气
随着反应的进行浓盐酸变稀,稀盐酸不能被氧化成氯气
.(3)若将制得的少量氯气通入无色的饱和碘化钾溶液中,溶液变
棕黄色
棕黄色
色,其离子方程式是Cl2+2I-=2Cl-+I2
Cl2+2I-=2Cl-+I2
,向所得溶液中加入四氯化碳,振荡后静置,则溶液分为两层,下层是显紫红色
紫红色
色,这种操作叫做萃取
萃取
.(4)若将制得的氯气制成饱和氯水,则实验室保存饱和氯水的方法是
保存在细口棕色试剂瓶中,放置冷暗处
保存在细口棕色试剂瓶中,放置冷暗处
.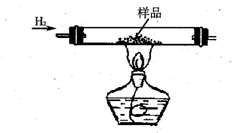 实验室有CuO和铜粉的混合物.要测定该样品(已称得其质量为m g)中氧化铜的质量分数.
实验室有CuO和铜粉的混合物.要测定该样品(已称得其质量为m g)中氧化铜的质量分数.(一)甲同学用“盐酸与锌反应生成的氢气还原氧化铜,再称取所得铜的总质量”的实验方法进行测定.部分实验装置如下:
请回答:
(1)对硬质玻璃管加热前如何检验空气是否已经排尽
(2)在制氢气装置与硬质玻璃管之间是否需要连接除杂装置?
理由是
(3)若m g样品经充分反应至固体质量不再减轻为止后,冷却、称量所得固体物质的质量为n g.则样品中氧化铜的质量分数为
(二)乙同学利用下列实验仪器及试剂,设计出两种方法测定样品中氧化铜的质量分数.
请你填写表格中的有关内容.
实验可能用到的主要仪器:①托盘天平、②玻璃棒、③漏斗、④泥三角、⑤烧杯、⑥坩埚、⑦酒精灯、⑧三角架
实验可能用到的试剂:a.稀硝酸b.稀硫酸c.蒸馏水d.浓硫酸
| 实验方法 | 有关化学方程式 | 实验用仪器(填序号) | 实验需直接测定的物理量(用文字说明) |
| (1) | H2SO4+CuO═CuSO4+H2O | ||
| (2) | 实验前坩埚与样品总质量(或坩埚质量)、实验后坩埚与CuO总质量 |
 设计一个简单的一次性完成实验的装置图,验证醋酸溶液、二氧化碳水溶液、苯酚溶液的酸性强弱顺序是CH3COOH>H2CO3>C6H5OH.
设计一个简单的一次性完成实验的装置图,验证醋酸溶液、二氧化碳水溶液、苯酚溶液的酸性强弱顺序是CH3COOH>H2CO3>C6H5OH.