摘要: 把一定量的SO2通入溶液中.溶液由棕色变为浅绿色. 但立即又变为棕黄色.此时若滴入溶液.则会产生白色沉淀.在上述一系列变化过程中.最终被还原的是 A.SO2 B. C. D.
网址:http://m.1010jiajiao.com/timu3_id_408915[举报]
把一定量的SO2通入Fe(NO3)3溶液中,溶液由棕色变为浅绿色,但立即又变为棕黄色,此时若滴入BaCl2溶液,则会产生白色沉淀.在上述一系列变化过程中,最终被还原的是
[ ]
A.SO2
B.Fe2+
C.NO3-
D.Fe3+
查看习题详情和答案>>
B.Fe2+
C.NO3-
D.Fe3+
(I)下列有关实验的叙述中,合理的是
A.把SO2通入紫色石蕊试液,可验证SO2的漂白性
B.一学生用pH试纸测得某氯水的pH为2
C.不宜用瓷坩埚灼烧氢氧化钠或碳酸钠
D.将10g ZnSO4?7H2O溶解在90g水中配制10%的ZnSO4溶液
E.向某溶液中滴加氯化钡溶液,产生不溶于稀硝酸的白色沉淀,则该溶液中一定含有SO2-4
F.配制一定物质的量浓度的溶液,定容时俯视容量瓶的刻度线,会使所配溶液浓度偏高
(II)(二氯化硫(SCl2)熔点-78℃,沸点59℃.密度1.638g/mL.遇水易分解二氯化硫与三氧化硫作用可生成重要化工试剂亚硫酰氯(SOCl2).以下是由氯气与硫反应合成二氯化硫的实验装置.

回答下列问题:
(1)装置B盛放的药品是
(2)实验开始前先在D中放入一定量的硫粉,加热使硫熔化,然后转动和摇动烧瓶使硫附着在烧瓶内壁表面形成一薄层,这样做的目的是
(3)实验时,D装置需加热至50-59℃,最好采用何种方式加热
(4)F装置中干燥管内所盛物质是
查看习题详情和答案>>
CF
CF
(填序号)A.把SO2通入紫色石蕊试液,可验证SO2的漂白性
B.一学生用pH试纸测得某氯水的pH为2
C.不宜用瓷坩埚灼烧氢氧化钠或碳酸钠
D.将10g ZnSO4?7H2O溶解在90g水中配制10%的ZnSO4溶液
E.向某溶液中滴加氯化钡溶液,产生不溶于稀硝酸的白色沉淀,则该溶液中一定含有SO2-4
F.配制一定物质的量浓度的溶液,定容时俯视容量瓶的刻度线,会使所配溶液浓度偏高
(II)(二氯化硫(SCl2)熔点-78℃,沸点59℃.密度1.638g/mL.遇水易分解二氯化硫与三氧化硫作用可生成重要化工试剂亚硫酰氯(SOCl2).以下是由氯气与硫反应合成二氯化硫的实验装置.

回答下列问题:
(1)装置B盛放的药品是
饱和食盐水
饱和食盐水
C中是浓硫酸
浓硫酸
(2)实验开始前先在D中放入一定量的硫粉,加热使硫熔化,然后转动和摇动烧瓶使硫附着在烧瓶内壁表面形成一薄层,这样做的目的是
增大反应接触面积
增大反应接触面积
(3)实验时,D装置需加热至50-59℃,最好采用何种方式加热
水浴加热
水浴加热
.为了防止E中液体挥发,可以采取的措施将锥形瓶放入冰水中冷却
将锥形瓶放入冰水中冷却
.(4)F装置中干燥管内所盛物质是
碱石灰(或固体氢氧化钠或生石灰)
碱石灰(或固体氢氧化钠或生石灰)
的作用是:防止空气中水蒸气进入并吸收残留余的氯气
防止空气中水蒸气进入并吸收残留余的氯气
.运用化学反应原理研究氮、碳、硫等单质及其化合物的反应有重要意义。
(1)氨在国民经济中占有重要地位。合成氨工业中,合成塔中每产生2mol NH3,放出92.2kJ热量。
①若起始时向容器内放入2mol N2和6mol H2,达平衡后放出的热量为Q,则Q(填 “>”、“<”或“=”) 184.4 kJ。
②已知

1mol N—H键断裂吸收的能量等于 kJ。
(2)硫酸的年产量可以用来衡量一个国家的化工生产能力。工业生产硫酸的流程中存在反应:2SO2(g)+O2(g) 2SO3(g)。反应体系中SO3的百分含量和温度的关系如下图所示(曲线上任何一点都表示平衡状态)。根据图示回答下列问题:
2SO3(g)。反应体系中SO3的百分含量和温度的关系如下图所示(曲线上任何一点都表示平衡状态)。根据图示回答下列问题:

①该反应的 0(填“>’或“<”)。
0(填“>’或“<”)。
②下列说法正确的是
a.若在恒温、恒压条件下向上述平衡体系中通入氦气,平衡不移动
b.在D点时,v正>v逆
c.B点、C点反应的平衡常数分别为K1、K2,则K1<K2
d.在A点时,消耗1mol SO2必定同时消耗1mol SO3
(3)过度排放CO2会造成温室效应。
①最近科学家提出“绿色自由”构想能把空气中的CO2转变为可再生燃料甲醇。甲醇可制作燃料电池,写出该电池负极反应式(电解液为KOH溶液) 。
②CO2也可用NaOH溶液吸收得到Na2CO3溶液,写出该反应的离子方程式 。
Na2CO3水溶液呈碱性,其原因是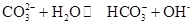 ,25℃时该反应的K=2×10-4mol·L-1,则当溶液中c(HCO- 3):c(CO2- 3)=2∶1时,溶液的pH= 。
,25℃时该反应的K=2×10-4mol·L-1,则当溶液中c(HCO- 3):c(CO2- 3)=2∶1时,溶液的pH= 。
(1)氨在国民经济中占有重要地位。合成氨工业中,合成塔中每产生2mol NH3,放出92.2kJ热量。
①若起始时向容器内放入2mol N2和6mol H2,达平衡后放出的热量为Q,则Q(填 “>”、“<”或“=”) 184.4 kJ。
②已知

1mol N—H键断裂吸收的能量等于 kJ。
(2)硫酸的年产量可以用来衡量一个国家的化工生产能力。工业生产硫酸的流程中存在反应:2SO2(g)+O2(g)
 2SO3(g)。反应体系中SO3的百分含量和温度的关系如下图所示(曲线上任何一点都表示平衡状态)。根据图示回答下列问题:
2SO3(g)。反应体系中SO3的百分含量和温度的关系如下图所示(曲线上任何一点都表示平衡状态)。根据图示回答下列问题:
①该反应的
 0(填“>’或“<”)。
0(填“>’或“<”)。②下列说法正确的是
a.若在恒温、恒压条件下向上述平衡体系中通入氦气,平衡不移动
b.在D点时,v正>v逆
c.B点、C点反应的平衡常数分别为K1、K2,则K1<K2
d.在A点时,消耗1mol SO2必定同时消耗1mol SO3
(3)过度排放CO2会造成温室效应。
①最近科学家提出“绿色自由”构想能把空气中的CO2转变为可再生燃料甲醇。甲醇可制作燃料电池,写出该电池负极反应式(电解液为KOH溶液) 。
②CO2也可用NaOH溶液吸收得到Na2CO3溶液,写出该反应的离子方程式 。
Na2CO3水溶液呈碱性,其原因是
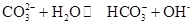 ,25℃时该反应的K=2×10-4mol·L-1,则当溶液中c(HCO- 3):c(CO2- 3)=2∶1时,溶液的pH= 。
,25℃时该反应的K=2×10-4mol·L-1,则当溶液中c(HCO- 3):c(CO2- 3)=2∶1时,溶液的pH= 。现有部分短周期元素的性质或原子结构如下表:
(1)用化学用语回答下列问题:
①A元素在周期表中的位置
②B元素原子结构示意图
 ;
;
③C单质分子的电子式
 ;用电子式表示A和B元素组成的化合物的形成过程
;用电子式表示A和B元素组成的化合物的形成过程
 ;
;
④D元素在自然界有两种核素,用原子符号表示其中子数为20的核素
(2)元素D与元素A相比,非金属性较强的是
a.常温下D的单质和A的单质状态不同
b.D的氢化物比A的氢化物稳定
c.一定条件下D和A的单质都能与钠反应
d.A的最高价含氧酸酸性弱于D的最高价含氧酸
e.D单质能与A的氢化物反应生成A单质
(3)探寻物质的性质差异性是学习的重要方法之一.A、B、C、D四种元素的最高价氧化物的水化物中化学性质明显不同于其他三种的是
(4)X是由A、B、C、D四种元素中的某种元素组成的单质,能经下列过程转化为W(其他条件略去).
X
Y
Z
W.
①若Y是有刺激性气味的无色气体,把Y通入BaCl2溶液中,然后滴加适量H2O2溶液,有白色沉淀生成,此白色沉淀的化学式为:
②若Z是红棕色气体,则Z→W的反应中氧化剂与还原剂物质的量之比为:
查看习题详情和答案>>
| 元素编号 | 元素性质或原子结构 |
| A | 有三个电子层,K、M层电子数之和等于L层电子数 |
| B | 短周期中金属性最强 |
| C | 常温下单质为双原子分子,氢化物的水溶液呈碱性 |
| D | 元素最高正价是+7价 |
①A元素在周期表中的位置
第三周期ⅥA族
第三周期ⅥA族
;②B元素原子结构示意图


③C单质分子的电子式




④D元素在自然界有两种核素,用原子符号表示其中子数为20的核素
1737Cl
1737Cl
.(2)元素D与元素A相比,非金属性较强的是
Cl
Cl
(用元素符号表示),下列表述中能证明这一事实的是bde
bde
(填选项序号).a.常温下D的单质和A的单质状态不同
b.D的氢化物比A的氢化物稳定
c.一定条件下D和A的单质都能与钠反应
d.A的最高价含氧酸酸性弱于D的最高价含氧酸
e.D单质能与A的氢化物反应生成A单质
(3)探寻物质的性质差异性是学习的重要方法之一.A、B、C、D四种元素的最高价氧化物的水化物中化学性质明显不同于其他三种的是
NaOH
NaOH
(写化学式).(4)X是由A、B、C、D四种元素中的某种元素组成的单质,能经下列过程转化为W(其他条件略去).
X
| O2 |
| O2 |
| H2O |
①若Y是有刺激性气味的无色气体,把Y通入BaCl2溶液中,然后滴加适量H2O2溶液,有白色沉淀生成,此白色沉淀的化学式为:
BaSO4
BaSO4
;生成该白色沉淀的化学方程式为BaCl2+SO2+H2O2=BaSO4↓+2HCl
BaCl2+SO2+H2O2=BaSO4↓+2HCl
;②若Z是红棕色气体,则Z→W的反应中氧化剂与还原剂物质的量之比为:
1:2
1:2
.