摘要:某研究小组用如图所示装置进行铜与浓硫酸反应的实验研究. (1)写出试管B中的实验现象 . (2)写出A中反应的化学方程式 (3)继续向A试管中加入H2O2.发现铜片 溶解.反应的离子方程式为: . 若仍不补充浓硫酸.只要求使铜片溶解.也可以加入(填写两种属于不同类别物质的化学式) . . (4)B试管口的棉花应沾有的试剂是 . (5)小组成员向反应后的溶液中加入足量的氧化铜.使剩余的硫酸全部转化为硫酸铜.过滤后.将滤液加热浓缩.冷却结晶制得硫酸铜晶体(CuSO4·xH2O).小组成员采用加热法测定该晶体里结晶水x的值. ①在他们的实验操作中.至少称量 次, ②下面是其中一次实验的数据: 坩埚质量 坩埚与晶体的总质量 加热后坩埚与固体总质量 11.7g 22.7g 18.9g 根据上表数据计算判断x的实侧值比理论值(x=5) .这次实验中产生误差的原因可能是 A.硫酸铜晶体中含有不挥发的杂质 B.实验前晶体表面有湿存水 C.加热时有晶体飞溅出去 D.加热失水后露置在空气中冷却
网址:http://m.1010jiajiao.com/timu3_id_408298[举报]
 某研究小组用如图所示装置进行铜与浓硫酸反应的实验研究.
某研究小组用如图所示装置进行铜与浓硫酸反应的实验研究.(1)写出试管B中的实验现象
品红溶液褪色
品红溶液褪色
.(2)写出A中反应的化学方程式
Cu+2H2SO4
CuSO4+SO2↑+2H2O
| ||
Cu+2H2SO4
CuSO4+SO2↑+2H2O
| ||
(3)继续向A试管中加入H2O2,发现铜片溶解,反应的离子方程式为:
Cu+H2O2+2H+=Cu2++2H2O
Cu+H2O2+2H+=Cu2++2H2O
.若仍不补充浓硫酸,只要求使铜片溶解,也可以加入(填写两种属于不同类别物质的化学式)
Fe2O3
Fe2O3
、NaNO3
NaNO3
.(4)B试管口的棉花应沾有的试剂是
NaOH(溶液)
NaOH(溶液)
.(5)小组成员向反应后的溶液中加入足量的氧化铜,使剩余的硫酸全部转化为硫酸铜,过滤后,将滤液加热浓缩,冷却结晶制得硫酸铜晶体(CuSO4?xH2O).小组成员采用加热法测定该晶体里结晶水x的值.
①在他们的实验操作中,至少称量
4
4
次;②下面是其中一次实验的数据:
| 坩埚质量 | 坩埚与晶体的总质量 | 加热后坩埚与固体总质量 |
| 11.7g | 22.7g | 18.9g |
偏小
偏小
(填“偏大”、“偏小”),这次实验中产生误差的原因可能是AD
AD
(填序号)A.硫酸铜晶体中含有不挥发的杂质 B.实验前晶体表面有湿存水
C.加热时有晶体飞溅出去 D.加热失水后露置在空气中冷却.
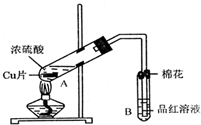 某研究小组用如图所示装置进行铜与浓硫酸反应的实验研究.
某研究小组用如图所示装置进行铜与浓硫酸反应的实验研究.
(1)写出试管B中的实验现象______.
(2)写出A中反应的化学方程式______
(3)继续向A试管中加入H2O2,发现铜片溶解,反应的离子方程式为:______.
若仍不补充浓硫酸,只要求使铜片溶解,也可以加入(填写两种属于不同类别物质的化学式)______、______.
(4)B试管口的棉花应沾有的试剂是______.
(5)小组成员向反应后的溶液中加入足量的氧化铜,使剩余的硫酸全部转化为硫酸铜,过滤后,将滤液加热浓缩,冷却结晶制得硫酸铜晶体(CuSO4?xH2O).小组成员采用加热法测定该晶体里结晶水x的值.
①在他们的实验操作中,至少称量______次;
②下面是其中一次实验的数据:
| 坩埚质量 | 坩埚与晶体的总质量 | 加热后坩埚与固体总质量 |
| 11.7g | 22.7g | 18.9g |
A.硫酸铜晶体中含有不挥发的杂质 B.实验前晶体表面有湿存水
C.加热时有晶体飞溅出去 D.加热失水后露置在空气中冷却. 查看习题详情和答案>>
某研究小组用如图所示装置进行铜与浓硫酸反应的实验研究.
(1)写出试管B中的实验现象______.
(2)写出A中反应的化学方程式______
(3)继续向A试管中加入H2O2,发现铜片溶解,反应的离子方程式为:______.
若仍不补充浓硫酸,只要求使铜片溶解,也可以加入(填写两种属于不同类别物质的化学式)______、______.
(4)B试管口的棉花应沾有的试剂是______.
(5)小组成员向反应后的溶液中加入足量的氧化铜,使剩余的硫酸全部转化为硫酸铜,过滤后,将滤液加热浓缩,冷却结晶制得硫酸铜晶体(CuSO4?xH2O).小组成员采用加热法测定该晶体里结晶水x的值.
①在他们的实验操作中,至少称量______次;
②下面是其中一次实验的数据:
根据上表数据计算判断x的实侧值比理论值(x=5)______(填“偏大”、“偏小”),这次实验中产生误差的原因可能是______(填序号)
A.硫酸铜晶体中含有不挥发的杂质 B.实验前晶体表面有湿存水
C.加热时有晶体飞溅出去 D.加热失水后露置在空气中冷却.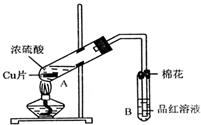
查看习题详情和答案>>
(1)写出试管B中的实验现象______.
(2)写出A中反应的化学方程式______
(3)继续向A试管中加入H2O2,发现铜片溶解,反应的离子方程式为:______.
若仍不补充浓硫酸,只要求使铜片溶解,也可以加入(填写两种属于不同类别物质的化学式)______、______.
(4)B试管口的棉花应沾有的试剂是______.
(5)小组成员向反应后的溶液中加入足量的氧化铜,使剩余的硫酸全部转化为硫酸铜,过滤后,将滤液加热浓缩,冷却结晶制得硫酸铜晶体(CuSO4?xH2O).小组成员采用加热法测定该晶体里结晶水x的值.
①在他们的实验操作中,至少称量______次;
②下面是其中一次实验的数据:
| 坩埚质量 | 坩埚与晶体的总质量 | 加热后坩埚与固体总质量 |
| 11.7g | 22.7g | 18.9g |
A.硫酸铜晶体中含有不挥发的杂质 B.实验前晶体表面有湿存水
C.加热时有晶体飞溅出去 D.加热失水后露置在空气中冷却.

某研究小组用如图所示装置进行铜与浓硫酸反应的实验研究。
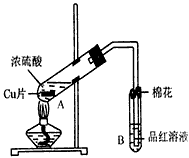
(1)写出试管B中的实验现象______________________。
(2)写出A中反应的化学方程式______________________。
(3)继续向A试管中加入H2O2,发现铜片溶解,反应的离子方程式为:______________________。若仍不补充浓硫酸,只要求使铜片溶解,也可以加入(填写两种属于不同类别物质的化学式)___________、
___________。
(4)B试管口的棉花应沾有的试剂是___________。
(5)小组成员向反应后的溶液中加入足量的氧化铜,使剩余的硫酸全部转化为硫酸铜,过滤后,将滤液加热浓缩,冷却结晶制得硫酸铜晶体(CuSO4·xH2O)。小组成员采用加热法测定该晶体里结晶水x的值。
①在他们的实验操作中,至少称量___________次;
②下面是其中一次实验的数据:
(2)写出A中反应的化学方程式______________________。
(3)继续向A试管中加入H2O2,发现铜片溶解,反应的离子方程式为:______________________。若仍不补充浓硫酸,只要求使铜片溶解,也可以加入(填写两种属于不同类别物质的化学式)___________、
___________。
(4)B试管口的棉花应沾有的试剂是___________。
(5)小组成员向反应后的溶液中加入足量的氧化铜,使剩余的硫酸全部转化为硫酸铜,过滤后,将滤液加热浓缩,冷却结晶制得硫酸铜晶体(CuSO4·xH2O)。小组成员采用加热法测定该晶体里结晶水x的值。
①在他们的实验操作中,至少称量___________次;
②下面是其中一次实验的数据:
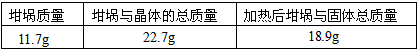
根据上表数据计算判断x的实侧值比理论值(x=5)________(填“偏大”、“偏小”),这次实验中产生误差的原因可能是___________(填序号)
A.硫酸铜晶体中含有不挥发的杂质
B.实验前晶体表面有湿存水
C.加热时有晶体飞溅出去
D.加热失水后露置在空气中冷却
查看习题详情和答案>>
A.硫酸铜晶体中含有不挥发的杂质
B.实验前晶体表面有湿存水
C.加热时有晶体飞溅出去
D.加热失水后露置在空气中冷却
某研究小组用如图所示装置进行铜与浓硫酸反应的实验研究。

(1)写出试管B中的实验现象____________________________________。
(2)写出A中反应的化学方程式:___________________________。
(3)充分反应后,若A试管中有铜片剩余,继续向A中加入H2O2,发现铜片溶解,反应的离子方程式为__________。
(4)充分反应后,若A试管中无铜片剩余,但出现白色混浊,该白色固体是________,初步确认该白色固体是什么物质的实验操作方法是__________________。
(5)B试管口的棉花应沾有的试剂是____________________________________。
(6)小组成员向(3)反应后的溶液中加入足量的氧化铜。使剩余的硫酸全部转化为硫酸铜,过滤后,将滤液加热浓缩,冷却后结晶制得硫酸铜晶体(CuSO4?xH2O)。小组成员采用加热法测定该晶体里结晶水x的值
①在他们的实验操作中,至少称量四次,最后两次称量的目的是
②下面是其中一次实验的数据:
| 坩埚质量 | 坩埚与晶体的总质量 | 加热后坩埚与固体总质量 |
| 11.0g | 37.8g | 27.0g |
根据上表数据计算判断x的实测值比理论值(x=5)____________(填“偏大”、“偏小”),这次实验中产生误差的原因可能是__________(填序号)
A.硫酸铜晶体中含有不挥发的杂质 B.实验前晶体表面有湿存水
C.加热时有晶体飞溅出去 D.加热失水后露置在空气中冷却
查看习题详情和答案>>