摘要:25.A.B两辆汽车在笔直的公路上同向行驶.当B车在A车前84m处时.B车速度为4m/s.且以2m/s2的加速度做匀加速运动,经过一段时间后.B车加速度突然变为零.A车一直以20m/s的速度做匀速运动.经过12s后两车相遇.问B车加速行驶的时间是多少?
网址:http://m.1010jiajiao.com/timu3_id_407172[举报]
A、B、C、D是四种常见的单质,A、B为金属,C、D常温下是气体,且D为黄绿色气体.甲、乙、丙为常见的化合物,甲是黑色且具有磁性的物质.它们之间的转化关系如下图所示:
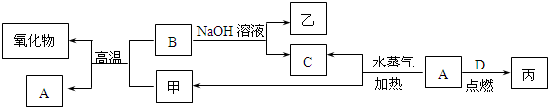
请回答下列问题:
(1)B与甲反应的化学方程式是
(2)常温下,将A或B的单质放入浓硫酸或浓硝酸中,是否溶解?
(3)将丙溶于水配成溶液,检验丙中阳离子的方法是
(4)写出A与水蒸气反应生成C和甲的化学方程式
(5)将A、B两种金属按一定的质量比组成混合物.
①取一定质量的该混合物,向其中加入足量的NaOH溶液,生成气体的体积在标准状况下为n L,B与NaOH溶液反应的离子方程式是
mol(用含字母的分数式表示).
②另取相同质量的该混合物,向其中加入足量的稀硫酸,固体全部溶解,生成气体的体积在标准状况下为m L,该反应中转移电子的物质的量为
mol,混合物中A的质量为
×56
×56g(用含字母的分数式表示).
③向②所得的溶液中加入过量的氢氧化钠溶液,充分搅拌,将产生的沉淀过滤出来,经洗涤、干燥、灼烧后得到一种固体,经称量发现该固体的质量和原混合物的质量恰好相等,则原混合物中铝的质量分数为
查看习题详情和答案>>

请回答下列问题:
(1)B与甲反应的化学方程式是
3Fe3O4+8Al
9Fe+4Al2O3
| ||
3Fe3O4+8Al
9Fe+4Al2O3
.
| ||
(2)常温下,将A或B的单质放入浓硫酸或浓硝酸中,是否溶解?
否
否
(填“是”或“否”).(3)将丙溶于水配成溶液,检验丙中阳离子的方法是
取少量丙的溶液于试管中,滴加KSCN溶液,若溶液变红,说明丙中存在Fe3+
取少量丙的溶液于试管中,滴加KSCN溶液,若溶液变红,说明丙中存在Fe3+
.(4)写出A与水蒸气反应生成C和甲的化学方程式
3Fe+4H2O(g)
Fe3O4+4H2
| ||
3Fe+4H2O(g)
Fe3O4+4H2
.
| ||
(5)将A、B两种金属按一定的质量比组成混合物.
①取一定质量的该混合物,向其中加入足量的NaOH溶液,生成气体的体积在标准状况下为n L,B与NaOH溶液反应的离子方程式是
2Al+2OH-+2H2O=2AlO2-+3H2↑
2Al+2OH-+2H2O=2AlO2-+3H2↑
,混合物中B的物质的量为| n |
| 33.6 |
| n |
| 33.6 |
②另取相同质量的该混合物,向其中加入足量的稀硫酸,固体全部溶解,生成气体的体积在标准状况下为m L,该反应中转移电子的物质的量为
| m |
| 11.2 |
| m |
| 11.2 |
| m-n |
| 22.4 |
| m-n |
| 22.4 |
③向②所得的溶液中加入过量的氢氧化钠溶液,充分搅拌,将产生的沉淀过滤出来,经洗涤、干燥、灼烧后得到一种固体,经称量发现该固体的质量和原混合物的质量恰好相等,则原混合物中铝的质量分数为
30%
30%
.(2012?石家庄二模)氨是重要的化工产品之一,研究合成氨反应具有重要意义.σ
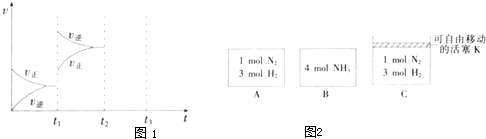
(1)已知断裂下列化学键需要吸收的能量分别为:N≡N 946.0kJ?mol-1、H-H 436kJ?mol-1、N-H 390.8kJ?mol-1,写出以N2(g)和H2(g)为原料合成NH3(g)的热化学方程式
(2)某小组研究了其他条件不变时,改变某一条件对上述反应的影响,实验结果如图1所示:
①t1时刻改变的条件为
②t2时刻,恒压充入氦气,t3时刻达到平衡.在图中画出t2时刻后的速率变化图象.
(3)相同温度下,A、B、C三个密闭容器,A、B恒容,C带有可自由移动的活塞K,各向其中充入如图2所示反应物,初始时控制活塞K,使三者体积相等,一段时间后均达到平衡.
①达到平衡时,A、C两个容器中NH3的浓度分别为c1、c2,则c1
②达到平衡时,若A、B两容器中反应物的转化率分别为α(A)、α(B),则 α(A)+α(B)
③达到平衡时,若容器C的体积是起始时的
,则平衡时容器C中H2的体积分数为
(4)直接供氨式碱性燃料电池(DAFC),以KOH溶液为电解质溶液,其电池反应为 4NH3+3O2═2N2+6H2O,则负极的电极反应式为
查看习题详情和答案>>

(1)已知断裂下列化学键需要吸收的能量分别为:N≡N 946.0kJ?mol-1、H-H 436kJ?mol-1、N-H 390.8kJ?mol-1,写出以N2(g)和H2(g)为原料合成NH3(g)的热化学方程式
N2(g)+3H2(g)?2NH3(g)△H=-90.8 kJ?mol-1
N2(g)+3H2(g)?2NH3(g)△H=-90.8 kJ?mol-1
(2)某小组研究了其他条件不变时,改变某一条件对上述反应的影响,实验结果如图1所示:
①t1时刻改变的条件为
升高温度
升高温度
.②t2时刻,恒压充入氦气,t3时刻达到平衡.在图中画出t2时刻后的速率变化图象.
(3)相同温度下,A、B、C三个密闭容器,A、B恒容,C带有可自由移动的活塞K,各向其中充入如图2所示反应物,初始时控制活塞K,使三者体积相等,一段时间后均达到平衡.
①达到平衡时,A、C两个容器中NH3的浓度分别为c1、c2,则c1
<
<
c2(填“>”、“<”或“=”).②达到平衡时,若A、B两容器中反应物的转化率分别为α(A)、α(B),则 α(A)+α(B)
<
<
1(填“>”、“<”或“=”).③达到平衡时,若容器C的体积是起始时的
| 3 | 4 |
50%
50%
(4)直接供氨式碱性燃料电池(DAFC),以KOH溶液为电解质溶液,其电池反应为 4NH3+3O2═2N2+6H2O,则负极的电极反应式为
2NH3-6e-+6OH-═N2+6H2O
2NH3-6e-+6OH-═N2+6H2O
.(Ⅰ)已知
有机物A~I有如下转化关系:

又知A、B、D、E、G、H都属于芳香烃,且对称性较高,1mol A、H被KMnO4(H+)氧化分别得2mol F、2mol I,A、E、G、H遇Br2的CCl4溶液都不褪色:A、G、H含碳量相同:H侧链及I的苯环上的一卤代物都只有一种.
(1)写结构简式:A
 E
E
 H
H

(2)写出D与过量Br2的CCl4溶液反应的化学方程式:

(3)上述①~⑨的反应中,属于取代反应的是
(Ⅱ)有机物在氧气中充分燃烧后,产物只有二氧化碳和水.甲、乙两组同学分别用A、B两种方法测定它的组成,如下图,得到两组数据.

已知:CO2+2NaOH=Na2CO3+H2O;浓硫酸具有吸水性
试回答下列问题:
(1)要得出正确结论,选用的方法应是
(2)用正确方法推测出该有机物是由
查看习题详情和答案>>

有机物A~I有如下转化关系:

又知A、B、D、E、G、H都属于芳香烃,且对称性较高,1mol A、H被KMnO4(H+)氧化分别得2mol F、2mol I,A、E、G、H遇Br2的CCl4溶液都不褪色:A、G、H含碳量相同:H侧链及I的苯环上的一卤代物都只有一种.
(1)写结构简式:A






(2)写出D与过量Br2的CCl4溶液反应的化学方程式:


(3)上述①~⑨的反应中,属于取代反应的是
⑥⑦⑨
⑥⑦⑨
.属于消去反应的是①③
①③
.(Ⅱ)有机物在氧气中充分燃烧后,产物只有二氧化碳和水.甲、乙两组同学分别用A、B两种方法测定它的组成,如下图,得到两组数据.

已知:CO2+2NaOH=Na2CO3+H2O;浓硫酸具有吸水性
| 燃烧有机物的质量 | 实验方法 | 实验前后①-④装置质量 | |||
| 实验前 | 实验后 | ||||
| 甲组 | 5.4g | A | ①150g | ①153.6g | |
| ②150g | ②165.4g | ||||
| 乙组 | 5.4g | B | ③150g | ③166.0g | |
| ④150g | ④154.2g | ||||
(1)要得出正确结论,选用的方法应是
A
A
(填A或B).(2)用正确方法推测出该有机物是由
C、H、O
C、H、O
元素组成,各元素的质量比为21:2:4
21:2:4
.(实验过程中气体均全部被吸收)