网址:http://m.1010jiajiao.com/timu3_id_404316[举报]
已知单质铁溶于―定浓度的硝酸溶液中反应的离子方程式为:
aFe+bNO3―+cH+=dFe2++fFe3++gNO↑+hN2O↑+kH2O(化学计量数a~k均为正整数)。回答下列问题:
(1)根据反应中氮、氢、氧三种元素的原子个数守恒,可得c、g、h的关系式是(用―个代数式表示。下同) 。
(2)根据反应中离子的电荷守恒,可得b、c、d、f的关系式是 。
(3)根据反应中电子转移的总数相等,可得d、f、g、h的关系式是 。
(4)若a=12,且铁和稀硝酸恰好完全反应,则b的取值范围是 ;
c的取值范围是 。
查看习题详情和答案>>aFe+bNO![]() +cH+
+cH+![]() dFe2++fFe3++g NO↑+hN2O↑+kH2O(化学计量数均为正整数)。回答下列问题:(1)根据反应中氮、氢、氧三种元素的原子个数守恒,可得c、g、h的关系式是 (用一个代数式表示。下同)。?
dFe2++fFe3++g NO↑+hN2O↑+kH2O(化学计量数均为正整数)。回答下列问题:(1)根据反应中氮、氢、氧三种元素的原子个数守恒,可得c、g、h的关系式是 (用一个代数式表示。下同)。?
(2)根据反应中离子电荷守恒,可得b、c、d、f的关系式是 。
(3)根据反应中电子转移的总数相等,可得d、f、g、h的关系式是 ,若a等于12,且铁和稀硝酸恰好完全反应,则b的取值范围是 ,c的取值范围是 。?
查看习题详情和答案>>已知单质铁溶于一定浓度的硝酸溶液中,反应的离子方程式为:?
aFe+bNO![]() +cH+
+cH+![]() dFe2++fFe3++g NO↑+hN2O↑+kH2O(化学计量数均为正整数)。回答下列问题:(1)根据反应中氮、氢、氧三种元素的原子个数守恒,可得c、g、h的关系式是 (用一个代数式表示。下同)。?
dFe2++fFe3++g NO↑+hN2O↑+kH2O(化学计量数均为正整数)。回答下列问题:(1)根据反应中氮、氢、氧三种元素的原子个数守恒,可得c、g、h的关系式是 (用一个代数式表示。下同)。?
(2)根据反应中离子电荷守恒,可得b、c、d、f的关系式是 。
(3)根据反应中电子转移的总数相等,可得d、f、g、h的关系式是 ,若a等于12,且铁和稀硝酸恰好完全反应,则b的取值范围是 ,c的取值范围是 。?
查看习题详情和答案>>aFe+bNO
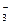 +cH+
+cH+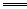 dFe2++fFe3++g NO↑+hN2O↑+kH2O(化学计量数均为正整数)。回答下列问题:(1)根据反应中氮、氢、氧三种元素的原子个数守恒,可得c、g、h的关系式是 (用一个代数式表示。下同)。?
dFe2++fFe3++g NO↑+hN2O↑+kH2O(化学计量数均为正整数)。回答下列问题:(1)根据反应中氮、氢、氧三种元素的原子个数守恒,可得c、g、h的关系式是 (用一个代数式表示。下同)。?(2)根据反应中离子电荷守恒,可得b、c、d、f的关系式是 。
(3)根据反应中电子转移的总数相等,可得d、f、g、h的关系式是 ,若a等于12,且铁和稀硝酸恰好完全反应,则b的取值范围是 ,c的取值范围是 。?
已知MOH为一元弱碱,25℃时,电离常数Kb= 1×10- 6mol·L-1,
(1)25℃时,将0.2 mol·L-1 HCl溶液与0.2 mol·L-1 MOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=6,此时混合溶液中由水电离出的c(H+)=Amol·L-1,若0.2 mol/L HCl溶液中由水电离出的c(H+)=Bmol·L-1,则:
①比较A B。(填“>”、“<”或“=”)
②根据电荷守恒,计算混合溶液中c(Cl-)-c(M+)=______ mol·L-1。 (精确计算,填具体数字)
(2)25℃时,0.01 mol·L-1MOH溶液的 pH=10,将其与等体积 pH = 4的盐酸溶液混合,则混合溶液的pH 7(填“>”、“<”或“=”),试求此时溶液中M Cl的水解平衡常数Kh= mol/L