摘要:10.如图是利用斜二测画法画出的的直观图,已知 =4,且的面积为16,过作轴,则的长为 .
网址:http://m.1010jiajiao.com/timu3_id_404281[举报]
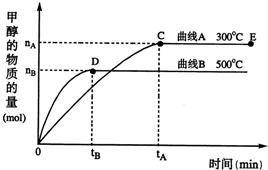 随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视.目前工业上有一种方法是用CO2来生产燃料甲醇.一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):
随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视.目前工业上有一种方法是用CO2来生产燃料甲醇.一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g)+2H2(g)
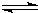 CH3OH(g)
CH3OH(g)根据题意完成下列各题:反应达到平衡时,
(1)平衡常数表达式K=
| c(CH3OH) |
| c(CO)?c2(H2) |
| c(CH3OH) |
| c(CO)?c2(H2) |
减小
减小
(填“增大”、“减小”或“不变”).(2)在500℃,从反应开始到平衡,氢气的平均反应速率v(H2)=
| 2nB |
| 3tB |
| 2nB |
| 3tB |
(3)在其他条件不变的情况下,对处于E点的体系体积压缩到原来的
| 1 |
| 2 |
bc
bc
a.氢气的浓度减少
b.正反应速率加快,逆反应速率也加快
c.甲醇的物质的量增加
d.重新平衡时
| n(H2) |
| n(CH3OH) |
(4)据研究,反应过程中起催化作用的为Cu2O,反应体系中含少量CO2有利于维持催化剂Cu2O的量不变,原因是:
Cu2O+CO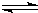 2Cu+CO2
2Cu+CO2
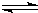 2Cu+CO2
2Cu+CO2Cu2O+CO 2Cu+CO2
2Cu+CO2
(用化学方程式表示). 2Cu+CO2
2Cu+CO2(5)使用燃料电池是节能减排的重要手段之一.CO和H2(俗称水煤气)燃料电池就是其中的一种,该电池的两极分别通入燃料气(水煤气)和氧气.电解质是掺杂了Y2O3的ZrO2晶体,它在高温下能传导O2-.水煤气在一定条件下可以合成二甲醚,同时还产生一种可以参与大气循环的无机化合物,3CO+3H2=CH3OCH3+CO2 或 2CO+4H2=CH3OCH3+H2O.上述水煤气燃料电池的负极反应方程式:(写1个)
CO+O2--2e-=CO2 H2+O2--2e-=2H2O
CO+O2--2e-=CO2 H2+O2--2e-=2H2O
.(6)如图是丙烷、二甲醚燃烧过程中能量变化图,其中x为各自反应中对应的系数.根据该图写出二甲醚燃烧的热化学方程式:
CH3OCH3(g)+3O2(g)
2CO2(g)+3H2O(l)△H=-1455kJ?mol-1
| 点燃 |
CH3OCH3(g)+3O2(g)
2CO2(g)+3H2O(l)△H=-1455kJ?mol-1
| 点燃 |

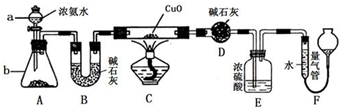 某课外活动小组欲利用氨气与CuO反应,研究氨气的性质并测其组成,设计了如图实验(夹持装置未画出)进行实验.请回答下列问题:
某课外活动小组欲利用氨气与CuO反应,研究氨气的性质并测其组成,设计了如图实验(夹持装置未画出)进行实验.请回答下列问题:(1)仪器a的名称为
(2)实验中,装置C中黑色CuO粉末全部转化为红色固体(已知Cu2O也为红色固体),量气管中有无色无味的气体.实验前称取黑色CuO 80g,实验后得到红色固体质量为68g.则红色固体成分的化学式为
(3)E装置中浓硫酸的作用是
(4)F中读取气体体积前,应对装置F进行的操作是:
(5)要想测得氨气分子中氮、氢原子个数比,实验中应至少测量或读取哪些数据
A.B装置实验前后质量差m g; B.F装置实验前后液面差V L;
C.D装置实验前后质量差m g; D.E装置实验前后质量差m g. 查看习题详情和答案>>
 (2013?焦作一模)开发新能源,使用清洁燃料,可以达到提高能效、减少污染的目的.
(2013?焦作一模)开发新能源,使用清洁燃料,可以达到提高能效、减少污染的目的.(1)由C、H、O三种元素中的两种和三种分别组成的燃料物质甲和乙,其分子中均有氧,且1个乙分子中含有18个电子,则甲和乙分别是
CO、CH3OH
CO、CH3OH
.乙是一种清洁燃料,工业上可用甲和氢气反应制得.
①T1温度时,在体积为2L的密闭容器中充入2mol甲和6mol H2,反应达到平衡后,测得c(甲)=0.2mol/L,则乙在平衡混合物中的物质的量分数是
| 1 |
| 3 |
| 1 |
| 3 |
②升高温度到T2时,反应的平衡常数为1,下列措施可以提高甲的转化率的是
C
C
(填字母).A.加入2mol甲 B.充入氮气 C.分离出乙 D.升高温度
(2)甲烷也是一种清洁燃料,但不完全燃烧时热效率降低并会产生有毒气体造成污染.
已知:
CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H1=-890.3kJ/mol
2CO (g)+O2(g)=2CO2(g)△H2=-566.0kJ/mol
则甲烷不完全燃烧生成一氧化碳和液态水时的热效率只是完全燃烧时的
0.7
0.7
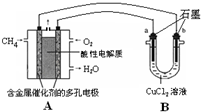
倍(计算结果保留1位小数).(3)甲烷燃料电池可以提升能量利用率.如图是利用甲烷燃料电池电解50mL 2mol/L的氯化铜溶液的装置示意图:
请回答:
①甲烷燃料电池的负极反应式是
CH4-8e-+2H2O=CO2+8H+
CH4-8e-+2H2O=CO2+8H+
.②当线路中有0.1mol电子通过时,
b
b
(填“a”或“b”)极增重0.32
0.32
g. 哥本哈根会议虽未能就减排问题达成有约束力的协议,但各国对于CO2对气候的影响达成了共识,都在积极研究方法循环利用CO2.CO2(g)与H2(g)反应可生成CH3OH(g)和H2O(g).某实验小组为研究该反应进行了如下实验.在某温度下,向容积为10L的恒温恒容容器中充入a mol CO2和a mol H2,测得不同时刻的c(H2)如右表.
哥本哈根会议虽未能就减排问题达成有约束力的协议,但各国对于CO2对气候的影响达成了共识,都在积极研究方法循环利用CO2.CO2(g)与H2(g)反应可生成CH3OH(g)和H2O(g).某实验小组为研究该反应进行了如下实验.在某温度下,向容积为10L的恒温恒容容器中充入a mol CO2和a mol H2,测得不同时刻的c(H2)如右表.| 时间/min | C(H2)/mol.L-1 |
| 0 | 0.40 |
| 2 | 0.28 |
| 4 | 0.19 |
| 6 | 0.13 |
| 8 | 0.08 |
| 10 | 0.04 |
| 12 | 0.04 |
CO2+3H2 CH3OH+H2O
CH3OH+H2O
 CH3OH+H2O
CH3OH+H2OCO2+3H2 CH3OH+H2O
CH3OH+H2O
.若达平衡状态时,放出的热量为58.8kJ,则上述反应的△H= CH3OH+H2O
CH3OH+H2O-49kJ/mol
-49kJ/mol
.0~10min内,CH3OH的平均反应速率v(CH3OH)=0.012mol/(L?min)
0.012mol/(L?min)
.(2)下列措施能使平衡体系中
| c(CH3OH) |
| c(CO2) |
CD
CD
(填字母).A、升高温度 B、充入Ar使压强增大
C、再充入0.5a mol CO2和0.5a mol H2D、将水从平衡体系中分离出来
(3)a=
4.0mol
4.0mol
,该温度下上述反应的平衡常数K=803.6
803.6
(精确到0.1).(4)在如图所示的坐标系中,画出CO2和H2的浓度随时间变化的图象.
哥本哈根会议虽未能就减排问题达成有约束力的协议,但各国对于CO2对气候的影响达成了共识,都在积极研究方法循环利用CO2.CO2(g)与H2(g)反应可生成CH3OH(g)和H2O(g).某实验小组为研究该反应进行了如下实验.在某温度下,向容积为10L的恒温恒容容器中充入a mol CO2和a mol H2,测得不同时刻的c(H2)如右表.
(1)写出生成CH3OH反应的化学方程式:______.若达平衡状态时,放出的热量为58.8kJ,则上述反应的△H=______.0~10min内,CH3OH的平均反应速率v(CH3OH)=______.
(2)下列措施能使平衡体系中
增大的是______(填字母).
A、升高温度 B、充入Ar使压强增大
C、再充入0.5a mol CO2和0.5a mol H2D、将水从平衡体系中分离出来
(3)a=______,该温度下上述反应的平衡常数K=______(精确到0.1).
(4)在如图所示的坐标系中,画出CO2和H2的浓度随时间变化的图象.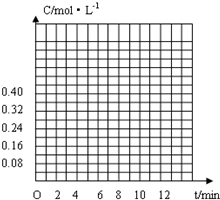
查看习题详情和答案>>
| 时间/min | C(H2)/mol.L-1 |
| 0 | 0.40 |
| 2 | 0.28 |
| 4 | 0.19 |
| 6 | 0.13 |
| 8 | 0.08 |
| 10 | 0.04 |
| 12 | 0.04 |
(2)下列措施能使平衡体系中
| c(CH3OH) |
| c(CO2) |
A、升高温度 B、充入Ar使压强增大
C、再充入0.5a mol CO2和0.5a mol H2D、将水从平衡体系中分离出来
(3)a=______,该温度下上述反应的平衡常数K=______(精确到0.1).
(4)在如图所示的坐标系中,画出CO2和H2的浓度随时间变化的图象.
