网址:http://m.1010jiajiao.com/timu3_id_403584[举报]
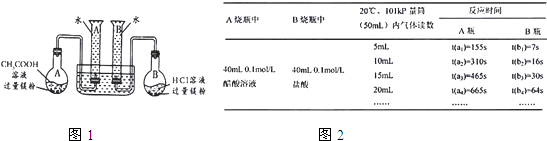
A烧瓶中 | B烧瓶中 | 反应时间 | ||||
A瓶 | B瓶 | |||||
CH3COOH 溶液 0.1 mol/L 40 Ml | 盐酸 0.1 mol/L 40 mL | 5 mL | t(a1)=155 s | t(b1)=7 s | ||
10 mL | t(a2)=310 s | t(b2)=16 s | ||||
15 mL | t(a3)=465 s | t(b3)=30 s | ||||
20 mL | t(a4)=665 s | t(b4)=54 s | ||||
…… | …… | …… | ||||

分析数据,观察装置图,回答下列问题:
(1)组装完成后,某同学发现该装置在设计上存在明显缺陷,根本无法完成实验,甚至存在危险。缺陷在于_____________________________________________________________。
(2)写出B烧瓶中反应的离子方程式:___________________________________________。
(3)欲配制100 mL实验所需浓度的盐酸,除需要烧杯、酸式滴定管之外,还需要用到的主要玻璃仪器是________________________________________________________________。
(4)在实验数据中①t(a1)远远大于t(b1)的原因为:____________________________;
②由__________________________________〔用有关t(a1)、t(a2)、t(a3)的代数式表示〕说明醋酸中存在电离平衡。
(5)该实验能得到什么结论:(最少答出两点)
①___________________________。②___________________________。
正确操作,记录得到下图2中部分实验数据.
分析数据,观察实验装置图,回答下列问题:
(1)组装完成后,某同学发现该装置在设计上存在明显缺陷:根本无法完成实验,甚至存在危险,其缺陷在于______;
经小组研究后,稍作改进就可继续实验了;
(2)欲配置100mL实验所需浓度的盐酸,除烧杯、酸式滴定管、胶头滴管之外,还需用到的主要玻璃仪器是______;
(3)在实验数据中
①t(a1)远远大于t(b1)的原因为:______;
②由______[用含t(b1)、t(b2)、t(b3)代数式表示]说明盐酸是强酸,不存在电离平衡;由______[用含t(a1)、t(a2)、t(a3)代数式表示]说明醋酸中存在电离平衡.
(4)该实验得到什么结论?(回答出两点即可)
①______;
②______.
(5)通过实验判断,锌与稀盐酸制氢气时,若要减慢反应速率而不影响产生氢气的量,可以加入______(填写两种不同作用原理的物质).
正确操作,记录得到下图2中部分实验数据.

分析数据,观察实验装置图,回答下列问题:
(1)组装完成后,某同学发现该装置在设计上存在明显缺陷:根本无法完成实验,甚至存在危险,其缺陷在于______;
经小组研究后,稍作改进就可继续实验了;
(2)欲配置100mL实验所需浓度的盐酸,除烧杯、酸式滴定管、胶头滴管之外,还需用到的主要玻璃仪器是______;
(3)在实验数据中
①t(a1)远远大于t(b1)的原因为:______;
②由______[用含t(b1)、t(b2)、t(b3)代数式表示]说明盐酸是强酸,不存在电离平衡;由______[用含t(a1)、t(a2)、t(a3)代数式表示]说明醋酸中存在电离平衡.
(4)该实验得到什么结论?(回答出两点即可)
①______;
②______.
(5)通过实验判断,锌与稀盐酸制氢气时,若要减慢反应速率而不影响产生氢气的量,可以加入______(填写两种不同作用原理的物质).
查看习题详情和答案>>
(1)组装完成后,某同学发现该装置在设计上存在明显缺陷:根本无法完成实验,甚至存在危险,其缺陷在于______,其改进方法是______.
(2)改进装置后,检查一侧装置的气密性的方法是______.
(3)欲配制100mL实验所需浓度的盐酸,除50mL量筒、烧杯、酸式滴定管、胶头滴管之外,还需用到的主要玻璃仪器是______.
正确操作,记录得到下表中部分实验数据.分析数据,观察实验装置图,回答下列问题:
| A烧瓶中 | B烧瓶中 | 20℃、101kPa 50mL量筒内气体读数 |
反应时间 | |
| A瓶 | B瓶 | |||
| 40mL0.1mol/L 醋酸溶液 |
40mL0.1mol/L 盐酸溶液 |
5mL | t(a1)=155s | t(b1)=7s |
| 10mL | t(a2)=310s | t(b2)=16s | ||
| 15mL | t(a3)=465s | t(b3)=30s | ||
| 20mL | t(a4)=565s | t(b4)=64s | ||
| … | … | … | ||
| 44.8mL | t(an)=865s | t(bn)=464s | ||
②由______[用含t(b1)、t(b2)、t(b3)代数式表示]说明盐酸是可能不存在电离平衡;由______[用含t(a1)、t(a2)、t(a3)代数式表示]说明醋酸中存在电离平衡.
(5)通过该实验可得到的结论是(回答出两点即可):①______;②______.
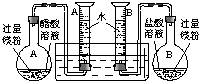
(1)组装完成后,某同学发现该装置在设计上存在明显缺陷:根本无法完成实验,甚至存在危险,其缺陷在于______,其改进方法是______.
(2)改进装置后,检查一侧装置的气密性的方法是______.
(3)欲配制100mL实验所需浓度的盐酸,除50mL量筒、烧杯、酸式滴定管、胶头滴管之外,还需用到的主要玻璃仪器是______.
正确操作,记录得到下表中部分实验数据.分析数据,观察实验装置图,回答下列问题:
| A烧瓶中 | B烧瓶中 | 20℃、101kPa 50mL量筒内气体读数 | 反应时间 | |
| A瓶 | B瓶 | |||
| 40mL0.1mol/L 醋酸溶液 | 40mL0.1mol/L 盐酸溶液 | 5mL | t(a1)=155s | t(b1)=7s |
| 10mL | t(a2)=310s | t(b2)=16s | ||
| 15mL | t(a3)=465s | t(b3)=30s | ||
| 20mL | t(a4)=565s | t(b4)=64s | ||
| … | … | … | ||
| 44.8mL | t(an)=865s | t(bn)=464s | ||
②由______[用含t(b1)、t(b2)、t(b3)代数式表示]说明盐酸是可能不存在电离平衡;由______[用含t(a1)、t(a2)、t(a3)代数式表示]说明醋酸中存在电离平衡.
(5)通过该实验可得到的结论是(回答出两点即可):①______;②______.
 查看习题详情和答案>>
查看习题详情和答案>>