网址:http://m.1010jiajiao.com/timu3_id_402838[举报]
(16分)Ⅰ.下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的某性质)


把与下面元素有关性质相符的曲线标号填入相应括号中:
⑴ⅡA族元素的最外层电子数 ( ) ⑵第三周期元素的最高化合价 ( )
⑶第三周期离子Na+、Mg2+、Al3+、P3-、S2-、Cl-的离子半径( )
⑷第二、三周期元素随原子序数递增原子半径的变化(不包括惰性气体) ( )
⑸碱金属的阳离子氧化能力(不包括钫)( )
Ⅱ.下图是元素周期表的一部分
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
⑴请在表中画出金属与非金属的交界线 ⑵请在表中标出第VIII的位置
⑶在表中标出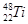 的位置
的位置
查看习题详情和答案>>
(16分)Ⅰ.下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的某性质)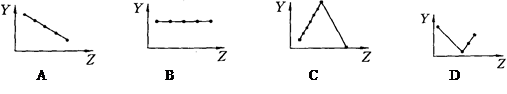
把与下面元素有关性质相符的曲线标号填入相应括号中:
⑴ⅡA族元素的最外层电子数 ( ) ⑵第三周期元素的最高化合价( )
⑶第三周期离子Na+、Mg2+、Al3+、P3-、S2-、Cl-的离子半径( )
⑷第二、三周期元素随原子序数递增原子半径的变化(不包括惰性气体) ( )
⑸碱金属的阳离子氧化能力(不包括钫)( )
Ⅱ.下图是元素周期表的一部分
| | | | |||||||||||||||
| |  | | | | | | | | |||||||||
| | | | | | | | | ||||||||||
| | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | ||||||||
⑴请在表中画出金属与非金属的交界线 ⑵请在表中标出第VIII的位置
⑶在表中标出
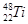 的位置
查看习题详情和答案>>
的位置
查看习题详情和答案>>
Ⅰ.下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y
为元素的某性质)

 |
把与下面元素有关性质相符的曲线标号填入相应括号中:
⑴ⅡA族元素的最外层电子数 ( ) ⑵第三周期元素的最高化合价 ( )
⑶第三周期离子Na+、Mg2+、Al3+、P3-、S2-、Cl-的离子半径( )
⑷第二、三周期元素随原子序数递增原子半径的变化(不包括惰性气体) ( )
⑸碱金属的阳离子氧化能力(不包括钫)( )
Ⅱ.下图是元素周期表的一部分
|
| |||||||||||||||||
| |||||||||||||||||
⑴请在表中画出金属与非金属的交界线 ⑵请在表中标出第VIII的位置
⑶在表中标出![]() 的位置
的位置

请把与下面元素有关性质相符的曲线标号(a、b、c、d)填入相应的空格中:
①ⅡA族元素的最外层电子数
②第3周期元素的最高化合价
③F-、Na+、Mg2+、Al3+的离子半径
(2)元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大.已知Y原子最外层电子数与核外电子总数之比为3:4;M原子的最外层电子数与次外电子数之比为3:4;N-、Z+、X+离子半径逐渐减小;化合物XN常温下为气体,据此回答:
①N的最高价氧化物的水化物的化学式是
②化合物A、B均为由上述五种元素中的任意三种元素组成的强电解质,且两种物质水溶液的酸碱性相同,组成元素的原子数目之比均为1:1:1,A溶液中水的电离程度最小,则化合物A中的化学键类型为
③Z与M形成的稳定固体化合物的电子式为


④X与Y、X与M均可形成18电子分子,写出这两种分子在水溶液中反应生成一种单质的化学方程式

①A族元素的价电子数
②第3周期元素的最高化合价
③F-、Na+、Mg2+、Al3+的离子半径
(2)元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大.已知Y元素原子最外层电子数与核外电子总数之比为3:4;M元素原子的最外层电子数与电子层数之比为4:3;N-、Z+、X+的半径逐渐减小;化合物XN常温下为气体.据此回答:
①Z的最高价氧化物对应的水化物的电子式为


③工业上制取单质M的化学方程式为
| ||
| ||