摘要: 目前半导体生产展开了一场“铜芯片 革命─在硅心片上用铜代替铝布线.古老的金属铜在现代科技应用上取得了突破.铜的冶炼方法是先用热还原法得到粗铜.然后用电解法精制. (1)用黄铜矿(主要成分CuFeS2)生产粗铜.其反应原理是 2 CuFeS2 +4O2 C2S+3SO2+2FeO 产物C2S在1200℃时继续反应 2C2S+3O2 2Cu2O+2 SO2 2Cu2O+C2S6Cu+SO2 ↑ 假如上述各步都能完全反应.1000t含杂质8%的黄铜矿最多可得到含铜96%的粗铜为 t. (2)将粗铜精炼成精铜.在电解糟中.应将粗铜作 极.通常使用 作电解液.电解时阴极反应式为 .
网址:http://m.1010jiajiao.com/timu3_id_40168[举报]
2009年3月,我国在世界上首先用二氧化碳作原料生产出了一种无毒、阻气、透明、全降解塑料--二氧化碳聚合物.有关其生产和使用的说法错误的是( )
| A、该塑料的生产和使用可减少温室效应 | B、该塑料的使用可减少对臭氧层的破坏 | C、可以充分利用廉价的资源生产塑料 | D、该塑料可广泛用于医药、食品包装和一次性餐具等方面 |
目前,科学家提出了一种经济而且理想的获得氢能源的循环体系(如右图) 。关于此循环体系,下列说法中错误的是
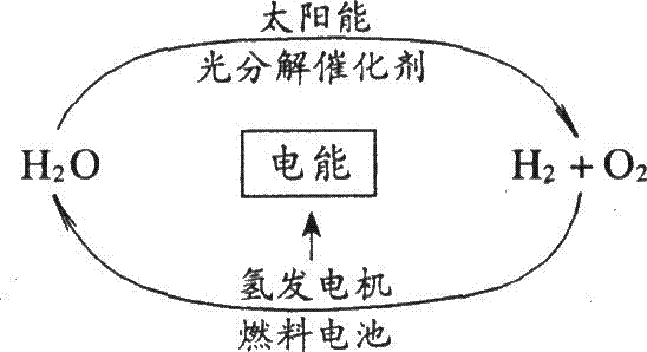 A.燃料电池能够使化学反应产生的能量转化为电能
A.燃料电池能够使化学反应产生的能量转化为电能
B.在此循环中发生了反应:2H2O![]() H2↑+O2↑
H2↑+O2↑
C.该氢能源的循环体系能够实现太阳能转化为电能
D.目前化学家急需解决的问题是寻找合适的光照条件下
分解水的催化剂
查看习题详情和答案>>
 氯气是氯碱工业的主要产品之一,是一种常用的消毒剂,其消毒原理是与水反应生成了次氯酸:
氯气是氯碱工业的主要产品之一,是一种常用的消毒剂,其消毒原理是与水反应生成了次氯酸:Cl2+H2O?HCl+HC10K=4.5×10-4
次氯酸的强氧化性能杀死水中的病菌(不直接用次氯酸为自来水消毒是因为次氯酸易分解,且毒性较大).但是,由于氯气贮运不方便,且具有一定的危险性,目前正逐渐被其他性能优越的消毒产品所替代.请回答:
(1)氯碱工业生产氯气的化学方程式为
2NaCl+2H2O
2NaOH+Cl2↑+H2↑
| ||
2NaCl+2H2O
2NaOH+Cl2↑+H2↑
.
| ||
(2)84消毒液与氯气相比具有贮运方便等优点,用氯气与烧碱溶液反应制备84消毒液的离子方程式为
Cl2+2OH-═Cl-+ClO-+H2O
Cl2+2OH-═Cl-+ClO-+H2O
.(3)二氧化氯是目前国际上公认的最新一代的高效、广谱、安全的杀菌、保鲜剂.我国科学家研发了用氯气氧化亚氯酸钠(NaClO2)固体制备二氧化氯的方法,其化学方程式为
Cl2+2NaClO2═2ClO2+2NaCl
Cl2+2NaClO2═2ClO2+2NaCl
.(4)一位同学设计了一套用浓盐酸和KMnO4固体制取少量氯气并比较氯气与碘单质的氧化性强弱的微型装置(如图).
①下列溶液能吸收Cl2的是
BC
BC
(填字母序号).A.饱和食盐水 B.饱和Na2SO3溶液
C.饱和NaOH溶液 D.浓硫酸
②能说明Cl2的氧化性强于I2的实验现象是
湿润淀粉碘化钾试纸变蓝
湿润淀粉碘化钾试纸变蓝
.③Cl2中含有少量HCl气体,可用
饱和食盐水
饱和食盐水
试剂除去HCl,请用平衡移动的原理解释原因:增大Cl-浓度,Cl2+H2O?HCl+HClO平衡会逆向移动,有效降低Cl2在饱和食盐水中的溶解度
增大Cl-浓度,Cl2+H2O?HCl+HClO平衡会逆向移动,有效降低Cl2在饱和食盐水中的溶解度
.目前世界上60%的镁是从海水中提取的.学生就这个课题展开了讨论的.已知海水提镁的主要步骤如图所示:

学生就这个课题提出了以下问题:
(一)在海水提镁的过程中如何实现对镁离子的富集?有三个学生提出自己的观点.
学生1的观点:直接往海水中加入沉淀剂.
学生2的观点:高温加热蒸发海水后,再加入沉淀剂.
学生3的观点:利用晒盐后的苦卤水,再加入沉淀剂.
请你评价三个学生提出的观点是否正确(填是或否),并简述理由.
(二)在海水提镁的过程中如何实现对镁离子的分离?
(1)为了使镁离子沉淀下来,加入的足量试剂①是
(2)试从节约能源,提高金属镁的纯度分析,适宜冶炼镁的方法是(用化学方程式表示)
查看习题详情和答案>>

学生就这个课题提出了以下问题:
(一)在海水提镁的过程中如何实现对镁离子的富集?有三个学生提出自己的观点.
学生1的观点:直接往海水中加入沉淀剂.
学生2的观点:高温加热蒸发海水后,再加入沉淀剂.
学生3的观点:利用晒盐后的苦卤水,再加入沉淀剂.
请你评价三个学生提出的观点是否正确(填是或否),并简述理由.
| 是否正确 | 简述理由 | |
| 学生1的观点 | 否 否 |
海水中镁离子浓度小,沉淀剂的用量大,不利于镁离子的沉淀 海水中镁离子浓度小,沉淀剂的用量大,不利于镁离子的沉淀 |
| 学生2的观点 | 否 否 |
能源消耗大,海水的综合利用低,成本高 能源消耗大,海水的综合利用低,成本高 |
| 学生3的观点 | 是 是 |
镁离子富集浓度高,成本低 镁离子富集浓度高,成本低 |
(1)为了使镁离子沉淀下来,加入的足量试剂①是
NaOH
NaOH
(填化学式).(2)试从节约能源,提高金属镁的纯度分析,适宜冶炼镁的方法是(用化学方程式表示)
Mg(OH)2+2HCl=MgCl2+2H2O、MgCl2(熔融)
Mg+Cl2↑
| ||
Mg(OH)2+2HCl=MgCl2+2H2O、MgCl2(熔融)
Mg+Cl2↑
.
| ||
海水占地球总储水量的97.2%.若把海水淡化和化工生产结合起来,既可以解决淡水资源缺乏的问题,又可以充分利用海洋资源.请回答下列问题:
(1)目前,以下“技术”中,可用于“海水淡化”的是 (填序号).
①蒸馏法 ②膜分离法(电渗析、反渗透) ③冷冻法 ④离子交换法
(2)海水晒盐利用的化学原理是 ;分离食盐晶体后的母液中含有 ,经过分离、提纯后,可用于 .
(3)工业上利用电解饱和食盐水可制得重要化工产品,反应的离子方程式为: ;电解所用的食盐水
需要精制,其原因是 ;精制时所用试剂为:盐酸、BaCl2溶液、NaOH溶液、Na2CO3溶液.加入试剂时,Na2CO3溶液必须在加入 之后加入.
(4)近年来有人提出了一种利用氯碱工业产品及氯化钠循环治理含二氧化硫废气并回收二氧化硫的方法,该方法的流程如下:

写出反应②的化学方程式: .
查看习题详情和答案>>
(1)目前,以下“技术”中,可用于“海水淡化”的是
①蒸馏法 ②膜分离法(电渗析、反渗透) ③冷冻法 ④离子交换法
(2)海水晒盐利用的化学原理是
(3)工业上利用电解饱和食盐水可制得重要化工产品,反应的离子方程式为:
需要精制,其原因是
(4)近年来有人提出了一种利用氯碱工业产品及氯化钠循环治理含二氧化硫废气并回收二氧化硫的方法,该方法的流程如下:

写出反应②的化学方程式: