摘要:某同学用久置的绿矾配制纯净的FeSO4溶液.所选用的试剂有:蒸馏水.铁粉.稀硫酸.请回答下列问题: (1)写出绿矾中FeSO4变质的化学反应方程式 . (2)铁粉.稀硫酸的作用和有关的离子反应方程式分别是:铁粉 .稀硫酸 . (3)配制过程中试剂的加入顺序为 .
网址:http://m.1010jiajiao.com/timu3_id_400825[举报]
某同学用10mol/L的浓盐酸配制250mL 1mol/L的稀盐酸,并进行有关实验.请回答下列问题:
(1)需要量取浓盐酸
(2)配制该稀盐酸时使用的仪器除量筒、烧杯、玻璃棒外,还必须用到的仪器有
(3)取所配制的稀盐酸100mL,与一定质量的锌充分反应,锌全部溶解后,生成的气体在标准状况下的体积为0.896L,则参加反应的锌的质量为
查看习题详情和答案>>
(1)需要量取浓盐酸
25
25
mL.(2)配制该稀盐酸时使用的仪器除量筒、烧杯、玻璃棒外,还必须用到的仪器有
胶头滴管
胶头滴管
、250mL容量瓶
250mL容量瓶
等.(3)取所配制的稀盐酸100mL,与一定质量的锌充分反应,锌全部溶解后,生成的气体在标准状况下的体积为0.896L,则参加反应的锌的质量为
2.6
2.6
g,设反应后溶液的体积仍为100mL,则反应后溶液中H+的物质的量浓度为0.2mol/L
0.2mol/L
.某同学用18mol/L的浓硫酸配制200mL 0.9mol/L的稀硫酸,并进行有关实验.请回答下列问题:
(1)需要量取浓硫酸
(2)配制该稀硫酸时使用的仪器除量筒、烧杯、200mL容量瓶外,还必须用到的仪器有
(3)容量瓶是一种颈部细长的梨形瓶,由于其颈部细长,所以在向容量瓶中移入液体时,需要一定的耐心和技巧.有人建议将容量瓶的瓶颈改粗,对该建议的正确评价是
A.可以按此建议改进,便于使用容量瓶
B.不能按此建议改进,因为会降低容量瓶的精确度
C.如果加粗瓶颈,可将原来刻在容量瓶瓶颈上的刻度线改刻在容量瓶的瓶身上
D.不必加粗瓶颈,因为向容量瓶中转移液体时,有少量液体倒出瓶外,不会对溶液的浓度产生太大影响
(4)在配制过程中,下列因素对所配制的稀硫酸的物质的量浓度有何影响?
若容量瓶未干燥即用来配制溶液,则所得溶液浓度
(5)取所配制的稀硫酸100mL,与一定质量的锌充分反应,锌全部溶解后,生成的气体在标准状况下的体积为0.448L,则参加反应的锌的质量为
查看习题详情和答案>>
(1)需要量取浓硫酸
10.0
10.0
mL.(准确到小数点后一位)(2)配制该稀硫酸时使用的仪器除量筒、烧杯、200mL容量瓶外,还必须用到的仪器有
胶头滴管
胶头滴管
、玻璃棒
玻璃棒
等.(3)容量瓶是一种颈部细长的梨形瓶,由于其颈部细长,所以在向容量瓶中移入液体时,需要一定的耐心和技巧.有人建议将容量瓶的瓶颈改粗,对该建议的正确评价是
B
B
A.可以按此建议改进,便于使用容量瓶
B.不能按此建议改进,因为会降低容量瓶的精确度
C.如果加粗瓶颈,可将原来刻在容量瓶瓶颈上的刻度线改刻在容量瓶的瓶身上
D.不必加粗瓶颈,因为向容量瓶中转移液体时,有少量液体倒出瓶外,不会对溶液的浓度产生太大影响
(4)在配制过程中,下列因素对所配制的稀硫酸的物质的量浓度有何影响?
若容量瓶未干燥即用来配制溶液,则所得溶液浓度
等于
等于
0.9mol?L-1(填“大于”、“等于”或“小于”,下同);若定容时俯视刻度线,则所得溶液浓度大于
大于
0.9mol?L-1.(5)取所配制的稀硫酸100mL,与一定质量的锌充分反应,锌全部溶解后,生成的气体在标准状况下的体积为0.448L,则参加反应的锌的质量为
1.3
1.3
g;设反应后溶液的体积仍为100mL,则反应后溶液中H+的物质的量浓度为1.4
1.4
mol/L.(8分)某同学用10mol/L的浓盐酸配制250mL 1mol/L的稀盐酸,并进行有关实验。请回答下列问题:
(1)需要量取浓盐酸___________mL。
(2)配制该稀盐酸时使用的仪器除量筒、烧杯、玻璃棒、250 mL容量瓶外,还必须用到的仪器有________等。
(3)取所配制的稀盐酸100mL,与一定质量的锌充分反应,锌全部溶解后,生成的气体在标准状况下的体积为0.896L,设反应后溶液的体积仍为100mL,则反应后溶液中H+的物质的量浓度为______________。
(4)有一瓶质量分数为14℅的KOH溶液,加热蒸发掉200g H2O后,得到160 mL质量分数为28℅的KOH溶液,则所得溶液中KOH物质的量浓度为______________。
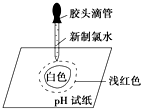 某同学在一张pH试纸上滴几滴新制的氯水,现象如图所示,下列有关该实验的说法中正确的是( )
某同学在一张pH试纸上滴几滴新制的氯水,现象如图所示,下列有关该实验的说法中正确的是( )