摘要:(一)制取氨气 (1)写出实验制取氨气的化学方程式 , (2)有同学模仿排饱和食盐水收集氯气的方法.想用排饱和氯化铵溶液的方法收集氨气.你认为他能否达到目的? . (二)该小组中某同学设计了下图所示的实验装置(夹持及尾气入理装置未画出).探究氨气的还原性: (1)该装置在设计上有一定缺陷.为保证实验结果的准确性.对该装置的改进措施是 . (2)利用改进后的装置进行实验.观察到CuO变为红色物质.无水CuSO4变蓝色.同时生成一种无污染的气体.写出氨气与CuO反应的化学方程式 .
网址:http://m.1010jiajiao.com/timu3_id_400127[举报]
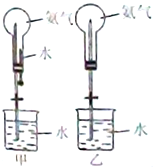 制取氨气并完成喷泉实验(图中夹持装置均已略去)
制取氨气并完成喷泉实验(图中夹持装置均已略去)(1)写出实验室制取氨气的化学方程式:
(2)收集氨气就使用
(3)用甲装置进行喷泉实验,上部烧瓶已装满干燥氨气,引发水上喷的操作是
(4)若烧瓶内的气体为CO2,则烧杯及胶头滴管内的溶液应是
(5)如果只提供乙图装置,请设计引发喷泉的方法:
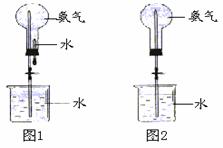 制取氨气并完成喷泉实验(图中夹持装置均已略去)。
制取氨气并完成喷泉实验(图中夹持装置均已略去)。
(1)写出实验室制取氨气的化学方程式:
(2)收集氨气应使用 法,要得到干燥的氨气可选用 干燥剂。
(3)如何检验烧瓶内的氨气已经收集满?
。
用图1装置进行喷泉实验,上部烧瓶已装满干燥的氨气,引发水上喷的操作是:挤压胶头滴管,打开止水夹。该实验的原理是 。
一般做喷泉实验时,水都不可能将烧瓶充满,其主要原因是
如果只提供如图2的装置,请说明引发喷泉的方法:
。
查看习题详情和答案>> 实验室制取氨气有几种方法,
实验室制取氨气有几种方法,(1)当用NH4Cl和Ca(OH)2来制取氨气时应选用装置是
A
A
,其反应的化学方程式为2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O
| ||
2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O
.
| ||
(2)收集氨气时应选用
向下排气
向下排气
法.(3)写出检验氨气是否已经收集满的方法.
用一张湿润的红色石蕊试纸接近试管口,试纸变蓝说明已收集满
用一张湿润的红色石蕊试纸接近试管口,试纸变蓝说明已收集满
(4)为了得到干燥的NH3,用
A
A
干燥剂.A、碱石灰 B、浓H2SO4 C、无水CaCl2 D、P2O5.
 氨气是一种重要的化工原料,但随着工业化进程的加快,氨气也逐渐变成居室里一种重要的污染性气体.
氨气是一种重要的化工原料,但随着工业化进程的加快,氨气也逐渐变成居室里一种重要的污染性气体.(1)液氨和水类似,也能发生电离:NH3+NH3=NH4++NH2-,其离子积常数为l.0×l0-30.现将2.3g金属钠投入1.0L液氨中,则液氨电离平衡
正方向
正方向
移动(填“不”、“正方向”、“逆方向”);待反应结束后,假设溶液的体积不变,所得溶液中NH4+的浓度为1×10-29mol/L
1×10-29mol/L
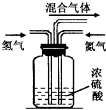
.(2)实验室模拟工业上用氮气和氢气合成氨气时,在反应前将两种气体通过如图装置,该装置的作用有三个:
①将氮气和氢气干燥:
②使氮气和氢气充分混合;
③
通过观察气泡控制氮气和氢气的流量,使氮气和氢气的量达到最佳比例
通过观察气泡控制氮气和氢气的流量,使氮气和氢气的量达到最佳比例
,从而提高氮气和氢气的利用率.(3)实验室可用氨气通过红热的氧化铜制取氮气,写出该反应的化学方程式:
2NH3+3CuO
3Cu+N2+3H2O
| ||
2NH3+3CuO
3Cu+N2+3H2O
.
| ||
(4)家庭空气中的氨主要来自建筑施工中使用的混凝土外加剂,如混凝土防冻剂尿素会和水缓慢发生反应:CO(NH2)2(s)+H2O(g) 2NH3(g)+CO2(g),该反应的平衡常数表达式为K=
| C2(NH3)?C(CO2) |
| C(H2O) |
| C2(NH3)?C(CO2) |
| C(H2O) |
(5)已知:N2(g)+O2(g)=2NO(g);△H=180Kj?mol-l4NH3(g)+5O2(g)=4NO(g)+6H2O(g);△H=-908Kj?mol-l请写出氨气被一氧化氮氧化生成氮气和气态水的热化学方程式:
4NH3(g)+6NO(g)=5N2(g)+6H2O(g)△H=-1808KJ/mol
4NH3(g)+6NO(g)=5N2(g)+6H2O(g)△H=-1808KJ/mol
.实验室模拟合成氨和氨催化氧化的流程如下:
(1)已知实验室可用饱和亚硝酸钠(NaNO2)溶液与饱和氯化铵溶液经加热后反应制取氮气,该反应中只有氮元素发生变价,写出该反应的化学方程式
从图1中选择制取氮气的合适装置
(2)如图2氮气和氢气通过甲装置,甲装置的作用除了将气体混合外,还有
(3)如图2用乙装置吸收一段时间氨后,再通入空气,同时将经加热的铂丝插入乙装置的锥形瓶内,能使铂丝保持红热的原因是:
(4)反应结束后锥形瓶内的溶液中含有H+、OH-、
查看习题详情和答案>>

(1)已知实验室可用饱和亚硝酸钠(NaNO2)溶液与饱和氯化铵溶液经加热后反应制取氮气,该反应中只有氮元素发生变价,写出该反应的化学方程式
NaNO2+NH4Cl
N2↑+2H20+NaCl
| ||
NaNO2+NH4Cl
N2↑+2H20+NaCl
.
| ||
从图1中选择制取氮气的合适装置
a
a
.
(2)如图2氮气和氢气通过甲装置,甲装置的作用除了将气体混合外,还有
控制氢气和氮气的流速
控制氢气和氮气的流速
干燥气体
干燥气体
.(3)如图2用乙装置吸收一段时间氨后,再通入空气,同时将经加热的铂丝插入乙装置的锥形瓶内,能使铂丝保持红热的原因是:
氨的氧化反应是一个放热反应,放出的热使铂丝保持红热
氨的氧化反应是一个放热反应,放出的热使铂丝保持红热
,锥形瓶中还可观察到的现象是:有红棕色气体产生
有红棕色气体产生
.(4)反应结束后锥形瓶内的溶液中含有H+、OH-、
NH4+、NO3-
NH4+、NO3-
离子.