摘要:11.硫酸是一种重要的化工原料.下列对硫酸的有关叙述不正确的是( ) A.敞口放置的浓硫酸质量会增加 B.因为浓硫酸有脱水性所以可以作为干燥剂 C.稀释浓硫酸时必须将浓硫酸沿容器壁缓慢倒入水中.并不断搅拌 D.皮肤上不小心沾了浓硫酸.应立即用布拭去.再用大量水冲洗
网址:http://m.1010jiajiao.com/timu3_id_3989945[举报]
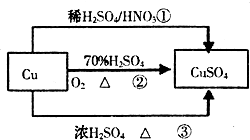 CuSO4是一种重要的化工原料,有关制备途径及性质如图所示.下列说法错误的是( )
CuSO4是一种重要的化工原料,有关制备途径及性质如图所示.下列说法错误的是( )| A、途径①所用混酸中H2SO4与HNO3物质的量之比最好为3:2 | B、相对于途径①、③,途径②更好地体现了绿色化学思想 | C、生成等量的硫酸铜,三个途径中参加反应的硫酸的物质的量:①=②<③ | D、利用途径②制备16g硫酸铜,被还原的硫酸的物质的量为0.1mol |
CuSO4是一种重要的化工原料,其有关制备途径如图所示。下列说法不正确的是
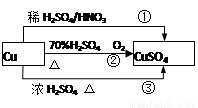
(已知:2Cu O2
O2 2H2SO4=2CuSO4
2H2SO4=2CuSO4 2H2O)
2H2O)
A.相对于途径①、③,途径②更好地体现了绿色化学思想
B.途径③中,1mol Cu与足量浓硫酸反应会产生64g SO2气体
C.途径①所用混酸中H2SO4与HNO3物质的量之比最好为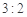
D.1mol Cu分别按照途径②、③中,被还原的H2SO4的质量之比为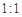
查看习题详情和答案>>
CuSO4是一种重要的化工原料,其有关制备途径如图所示。下列说法不正确的是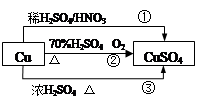
(已知:2Cu O2
O2 2H2SO4=2CuSO4
2H2SO4=2CuSO4 2H2O)
2H2O)
| A.相对于途径①、③,途径②更好地体现了绿色化学思想 |
| B.途径③中,1mol Cu与足量浓硫酸反应会产生64g SO2气体 |
C.途径①所用混酸中H2SO4与HNO3物质的量之比最好为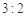 |
D.1mol Cu分别按照途径②、③中,被还原的H2SO4的质量之比为 |
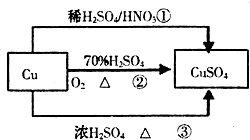 CuSO4是一种重要的化工原料,有关制备途径及性质如图所示.下列说法错误的是
CuSO4是一种重要的化工原料,有关制备途径及性质如图所示.下列说法错误的是
- A.途径①所用混酸中H2SO4与HNO3物质的量之比最好为3:2
- B.相对于途径①、③,途径②更好地体现了绿色化学思想
- C.生成等量的硫酸铜,三个途径中参加反应的硫酸的物质的量:①=②<③
- D.利用途径②制备16g硫酸铜,被还原的硫酸的物质的量为0.1mol
| |||||||||||||||||||||||||||||||||||